广西贵港市2021年中考化学试卷
试卷更新日期:2021-07-09 类型:中考真卷
一、单选题
-
1. 下列变化中,属于化学变化的是( )A、消化食物 B、火柴折断 C、水蒸发 D、铁丝受热熔化2. 空气是人类生产活动的重要资源。下列有关空气的说法错误的是( )A、氧气可供给动植物呼吸 B、食品包装袋填充氮气可延长食品的保质期 C、稀有气体可制造电光源 D、空气污染指数越高,空气质量越好3. 下列图示实验操作中,正确的是( )A、称量NaOH固体
 B、蒸发
B、蒸发  C、倾倒液体
C、倾倒液体  D、量取液体
D、量取液体  4. 下列物质在氧气中燃烧,生成黑色固体的是( )A、铁丝 B、硫 C、镁 D、红磷5. 下列物质的主要成分不属于盐的是( )A、生活中用作调味品的食盐 B、用于改良酸性土壤的熟石灰 C、用于治疗胃酸过多的小苏打 D、作为建筑材料的大理石6. 化学与人体健康密切相关。下列说法中正确的是( )A、均衡营养,少吃蔬菜多吃肉 B、霉变的花生,油炸后可食用 C、长期饮用蒸馏水,有利于健康 D、预防缺铁性贫血,推荐食用加铁酱油7. 振兴乡村,发展农业生产,化肥起着重要作用。某农作物出现叶色发黄、倒伏现象,需施加的化肥是( )A、KCl B、CO(NH2)2 C、KNO3 D、NH4H2PO48. 生活中处处蕴含着化学知识。下列说法错误的是( )A、在铁制品表面刷油漆可防止铁制品生锈 B、炒菜时,油锅着火可用锅盖盖灭 C、发现煤气泄漏,立即打开排气扇排气 D、可用食醋除去水壶中的水垢9. 建设美丽家园,人人有责。下列做法不利于环境保护的是( )A、大量燃放烟花 B、生活污水经集中处理后排放 C、垃圾分类处理 D、生活中减少塑料袋的使用10. 铜能与浓硝酸反应,反应的化学方程式为: ,则X的化学式是( )A、N2O4 B、NO2 C、NO D、N2O11. 甲、乙两种固体物质的溶解度曲线如图所示。下列说法错误的是( )
4. 下列物质在氧气中燃烧,生成黑色固体的是( )A、铁丝 B、硫 C、镁 D、红磷5. 下列物质的主要成分不属于盐的是( )A、生活中用作调味品的食盐 B、用于改良酸性土壤的熟石灰 C、用于治疗胃酸过多的小苏打 D、作为建筑材料的大理石6. 化学与人体健康密切相关。下列说法中正确的是( )A、均衡营养,少吃蔬菜多吃肉 B、霉变的花生,油炸后可食用 C、长期饮用蒸馏水,有利于健康 D、预防缺铁性贫血,推荐食用加铁酱油7. 振兴乡村,发展农业生产,化肥起着重要作用。某农作物出现叶色发黄、倒伏现象,需施加的化肥是( )A、KCl B、CO(NH2)2 C、KNO3 D、NH4H2PO48. 生活中处处蕴含着化学知识。下列说法错误的是( )A、在铁制品表面刷油漆可防止铁制品生锈 B、炒菜时,油锅着火可用锅盖盖灭 C、发现煤气泄漏,立即打开排气扇排气 D、可用食醋除去水壶中的水垢9. 建设美丽家园,人人有责。下列做法不利于环境保护的是( )A、大量燃放烟花 B、生活污水经集中处理后排放 C、垃圾分类处理 D、生活中减少塑料袋的使用10. 铜能与浓硝酸反应,反应的化学方程式为: ,则X的化学式是( )A、N2O4 B、NO2 C、NO D、N2O11. 甲、乙两种固体物质的溶解度曲线如图所示。下列说法错误的是( )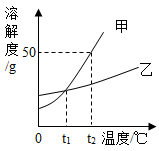 A、甲中混有少量的乙,可用降温结晶的方法提纯甲 B、当温度大于t1℃时,甲的溶解度大于乙的溶解度 C、t1℃时,甲、乙两物质的溶液的溶质质量分数一定相等 D、t2℃时,向30g甲中加入50g水,充分溶解,所得溶液质量为75g12. 下列实验方案不能达到实验目的的是( )
A、甲中混有少量的乙,可用降温结晶的方法提纯甲 B、当温度大于t1℃时,甲的溶解度大于乙的溶解度 C、t1℃时,甲、乙两物质的溶液的溶质质量分数一定相等 D、t2℃时,向30g甲中加入50g水,充分溶解,所得溶液质量为75g12. 下列实验方案不能达到实验目的的是( )选项
实验目的
实验方案
A
鉴别C、CuO、Fe三种粉末
分别加入稀硫酸,观察现象
B
除去NaCl固体中混有少量的Na2CO3
加入过量稀盐酸,蒸发
C
验证Fe、Cu、Ag三种金属的活动性强弱
将铁丝放入硫酸铜溶液中,将铜丝放入硝酸银溶液中,观察现象
D
分离KCl和MnO2的固体混合物
加适量水溶解,过滤
A、A B、B C、C D、D13. 下列图像能正确反映其对应变化关系的是( )A、电解水 B、向饱和Ca(OH)2溶液中加入少量的CaO固体
B、向饱和Ca(OH)2溶液中加入少量的CaO固体  C、向一定质量的镁粉和锌粉的固体混合物中逐滴滴入硝酸铜溶液
C、向一定质量的镁粉和锌粉的固体混合物中逐滴滴入硝酸铜溶液  D、向一定质量的CuSO4和H2SO4的混合液中逐滴滴入NaOH溶液
D、向一定质量的CuSO4和H2SO4的混合液中逐滴滴入NaOH溶液  14. 现有一包金属粉末,可能是由Al、Mg、Zn、Fe、Ag中的一种或几种组成。取该样品2.4g,向其加入100g一定溶质质量分数的稀硫酸,恰好完全反应,产生0.2g H2 , 溶液呈无色,无固体剩余。则下列结论正确的是( )A、该样品的组成仅有两种可能 B、所用稀硫酸的溶质质量分数为19.6% C、该样品中一定含有Mg D、所得溶液中溶质的总质量为12g
14. 现有一包金属粉末,可能是由Al、Mg、Zn、Fe、Ag中的一种或几种组成。取该样品2.4g,向其加入100g一定溶质质量分数的稀硫酸,恰好完全反应,产生0.2g H2 , 溶液呈无色,无固体剩余。则下列结论正确的是( )A、该样品的组成仅有两种可能 B、所用稀硫酸的溶质质量分数为19.6% C、该样品中一定含有Mg D、所得溶液中溶质的总质量为12g二、填空题
-
15. 请用数字和化学符号填空:(1)、氖气。(2)、三个汞原子。(3)、两个铁离子。(4)、葡萄糖。16. 化学源于生活。请回答:(1)、水是生命之源。生活中可以通过的方法,降低水的硬度。下列水的净化方法中,净化程度最高的是(填序号)。
①静置 ②吸附 ③过滤 ④蒸馏
(2)、桂平市木乐镇是运动服的主要生产基地之一。氨纶是制作运动服的一种材料,它属于(填“天然纤维”或“合成纤维”)。(3)、化石燃料包括、石油和天然气。燃油汽车所用燃料是由石油分离出来的,其排放的尾气中含有NO、CO等污染物。为了减少污染,我市投入使用磷酸亚铁锂电池的新能源公交车,该公交车在充电时是将能转化为能。17. “宏观辨识与微观探析”是化学的核心素养之一。(1)、核废水中含有大量具有放射性的氘,排放到海洋中会造成严重的污染。氘是氢元素的一种原子,含有1个中子。如图是氢元素在元素周期表中的部分信息和原子结构示意图,氘的质子数是 , 氢元素位于元素周期表中的第周期。 (2)、如图是某个化学反应的微观模拟示意图。请根据图中的信息回答:
(2)、如图是某个化学反应的微观模拟示意图。请根据图中的信息回答:
①反应前后,没有发生变化的微粒是(填微粒符号)。
②该反应的化学方程式为 , 属于(填基本反应类型)。
三、综合题
-
18. “太阳能光伏发电”能有效推进“碳中和”,发展“低碳经济”,其关键的材料是高纯硅。以下是高纯硅的简易生产流程。

请回答:
(1)、石英砂的主要成分是。四氯化硅(SiCl4)中硅元素的化合价为。(2)、“精馏”是蒸馏的一种,其原理是利用混合物各成分的不同,将物质分离出来。(3)、上述流程中可循环使用的物质是。(4)、流程⑤中发生反应的化学方程式为。19. 有一包固体样品可能是由NaOH、CaCO3、K2SO4、CuSO4、MgSO4中的一种或几种组成。某兴趣小组同学为了确定其成分,进行如下实验:
请回答:
(1)、白色固体a的成分是。(2)、固体样品中一定没有。(3)、生成白色沉淀b的反应的化学方程式为。20. 根据下列装置回答问题。
 (1)、写出标号仪器的名称:①;②。(2)、用高锰酸钾制取并收集较纯净的氧气,应选用的装置是(填字母)。(3)、实验室制取二氧化碳,反应的化学方程式为 , 发生装置可选用A或C,装置C的优点是;若用装置G收集二氧化碳,气体应从(填“a”或“b”)端通入。21. 某校甲、乙兴趣小组的同学在“探究纯碱的性质”实验中,分别做了下图所示的四组实验,并将四支试管中的所有物质分别倒入洁净的A、B烧杯中、实验结束后,甲、乙小组同学都观察到烧杯底部有固体不溶物,上层溶液呈红色。
(1)、写出标号仪器的名称:①;②。(2)、用高锰酸钾制取并收集较纯净的氧气,应选用的装置是(填字母)。(3)、实验室制取二氧化碳,反应的化学方程式为 , 发生装置可选用A或C,装置C的优点是;若用装置G收集二氧化碳,气体应从(填“a”或“b”)端通入。21. 某校甲、乙兴趣小组的同学在“探究纯碱的性质”实验中,分别做了下图所示的四组实验,并将四支试管中的所有物质分别倒入洁净的A、B烧杯中、实验结束后,甲、乙小组同学都观察到烧杯底部有固体不溶物,上层溶液呈红色。 (1)、(提出问题)烧杯中的上层溶液的溶质除酚酞外,还含有哪些?
(1)、(提出问题)烧杯中的上层溶液的溶质除酚酞外,还含有哪些?(猜想假设)一定含有NaCl,可能还含有NaOH、Na2CO3、Ba(OH)2、BaCl2、Na2SO4中的一种或几种。小明同学猜想溶液中的溶质是酚酞、NaCl、Ba(OH)2、Na2SO4小红同学认为小明同学的猜想是错误的,理由是。
(2)、(查阅资料)①HNO3与Na2CO3反应是分步进行的: (先), (后)。
②BaCl2溶液呈中性。
(实验探究)
甲组同学:
往A烧杯中逐滴滴入稀HNO3 , 一段时间后,才观察到有气泡产生,溶液变无色。烧杯中固体不溶物的质量,随滴入稀HNO3的质量变化关系如图所示。请写出固体不溶物质量增加的反应的化学方程式:。由此得出溶液中的溶质是酚酞、NaCl、NaOH、。
 (3)、乙组同学:
(3)、乙组同学:实验操作
实验现象
实验结论
取B烧杯中的少量溶液于试管中,滴入足量的BaCl2溶液
生成白色沉淀,
溶液中的溶质是酚酞、NaCl、NaOH、Na2CO3
继续往上述试管中滴入足量的稀HNO3
(4)、(交流反思)乙组同学经讨论后,一致认为:根据甲组同学所做实验的现象,无法确定溶液中的溶质是否存在NaOH,理由是(用文字叙述)。
四、计算题
-
22. 请根据所示的实验过程和提供的信息作答:
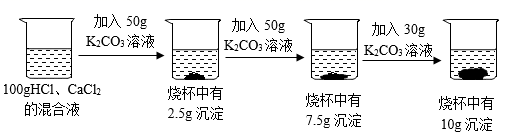 (1)、K2CO3中钾、碳、氧元素的质量比为(写最简比)。(2)、实验结束后溶液中的溶质为。(3)、实验所用K2CO3溶液的溶质质量分数为(精确至0.1%)。(4)、计算原混合液中CaCl2的质量分数。(写出计算过程,精确至0.1%)。
(1)、K2CO3中钾、碳、氧元素的质量比为(写最简比)。(2)、实验结束后溶液中的溶质为。(3)、实验所用K2CO3溶液的溶质质量分数为(精确至0.1%)。(4)、计算原混合液中CaCl2的质量分数。(写出计算过程,精确至0.1%)。