华师大版初中科学九上第一章第3节用分解反应制取氧气同步练习
试卷更新日期:2021-07-08 类型:同步测试
一、单选题
-
1. 能使带火星木条复燃的气体是( )A、氧气 B、稀有气体 C、氮气 D、二氧化碳2. 关于催化剂在化学反应中的作用说法正确的是( )A、一定加快反应速度 B、会减慢反应速度 C、加快或减慢反应速度 D、不改变反应速度3. 如图是实验室制取、收集、验满、验证氧气性质的装置或操作,其中正确的是( )A、制取氧气
 B、收集氧气
B、收集氧气  C、验满
C、验满 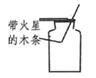 D、性质检验
D、性质检验 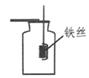 4. 有一份纯氯酸钾固体a,另有一份 混有少量二氧化锰的氯酸钾固体b,两份固体质量相等。分别同时加热a和b,能正确表示生成氧气的质量随反应时间而变化的图象是( )A、
4. 有一份纯氯酸钾固体a,另有一份 混有少量二氧化锰的氯酸钾固体b,两份固体质量相等。分别同时加热a和b,能正确表示生成氧气的质量随反应时间而变化的图象是( )A、 B、
B、 C、
C、 D、
D、 5. 现有a、b两份质量相等的固体氯酸钾,a加入少量二氧化锰,b是纯净的氯酸钾,将a、b放入两支试管中同时加热。放出氧气的质量和反应时间的关系图象正确的是( )A、
5. 现有a、b两份质量相等的固体氯酸钾,a加入少量二氧化锰,b是纯净的氯酸钾,将a、b放入两支试管中同时加热。放出氧气的质量和反应时间的关系图象正确的是( )A、 B、
B、 C、
C、 D、
D、 6. 某化学兴趣小组用如图所示的装置来制取干燥的氧气,并测定实验中生成的氧气体积。装置气密性良好,图Ⅰ中的燃烧匙内装有二氧化锰,燃烧匙可以上下移动,干燥管内装有足量碱石灰(可以吸收水蒸气)。下列说法正确的是( )
6. 某化学兴趣小组用如图所示的装置来制取干燥的氧气,并测定实验中生成的氧气体积。装置气密性良好,图Ⅰ中的燃烧匙内装有二氧化锰,燃烧匙可以上下移动,干燥管内装有足量碱石灰(可以吸收水蒸气)。下列说法正确的是( ) A、将装置Ⅰ分别与装置Ⅱ、Ⅲ、Ⅳ、V连接,均能达到测定氧气体积的目的 B、若用装置V测量生成氧气的体积,集气瓶上方原有的空气会使测量结果偏大 C、若用装置Ⅳ收集氧气,可将带火星的木条放置在b处导管口验满 D、若用装置Ⅰ与装置V量组合测量生成氧气的体积,实验时先连接装置Ⅰ和V,后将燃烧匙伸到液面以下7. 小金需收集一瓶约混有四分之一体积空气的氧气,下列操作正确的是( )
A、将装置Ⅰ分别与装置Ⅱ、Ⅲ、Ⅳ、V连接,均能达到测定氧气体积的目的 B、若用装置V测量生成氧气的体积,集气瓶上方原有的空气会使测量结果偏大 C、若用装置Ⅳ收集氧气,可将带火星的木条放置在b处导管口验满 D、若用装置Ⅰ与装置V量组合测量生成氧气的体积,实验时先连接装置Ⅰ和V,后将燃烧匙伸到液面以下7. 小金需收集一瓶约混有四分之一体积空气的氧气,下列操作正确的是( )A
B
C
D
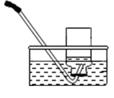



集气瓶中灌 的
水
集气瓶中灌 的水
导管伸入到集气瓶体积的 处
导管伸入到集气瓶体积的 处
A、A B、B C、C D、D8. 如图所示,①为制取氧气的发生装置(气密性良好),其中的燃烧匙可以上下移动。②和③为氧气的收集装置。小金欲制取一瓶干燥的氧气,下列分析正确的是( ) A、在①中,将MnO2浸入H2O2溶液,MnO2可分解产生氧气 B、若用装置②的方法收集氧气,需等到导管口气泡均匀并连续冒出时才可收集 C、若用装置③的方法收集氧气,可将带火星的木条放入瓶中进行验满 D、将装置①分别与装置②或③连接,均能达到实验目的9. 科学实验要规范操作。下列用高锰酸钾制取氧气的实验操作正确的是( )A、装高锰酸钾
A、在①中,将MnO2浸入H2O2溶液,MnO2可分解产生氧气 B、若用装置②的方法收集氧气,需等到导管口气泡均匀并连续冒出时才可收集 C、若用装置③的方法收集氧气,可将带火星的木条放入瓶中进行验满 D、将装置①分别与装置②或③连接,均能达到实验目的9. 科学实验要规范操作。下列用高锰酸钾制取氧气的实验操作正确的是( )A、装高锰酸钾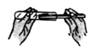 B、点燃酒精灯
B、点燃酒精灯  C、加热高锰酸钾
C、加热高锰酸钾  D、收集氧气
D、收集氧气  10. 实验室常用加热高锰酸钾固体制取氧气,反应的文字表达式为:高锰酸钾→锰酸钾+二氧化锰+氧气,现对一定量的高锰酸钾固体进行加热,加热过程中涉及的相关量随时间变化的图象正确的是( )A、
10. 实验室常用加热高锰酸钾固体制取氧气,反应的文字表达式为:高锰酸钾→锰酸钾+二氧化锰+氧气,现对一定量的高锰酸钾固体进行加热,加热过程中涉及的相关量随时间变化的图象正确的是( )A、 B、
B、 C、
C、 D、
D、 11. 如图所示的演示实验中,集气瓶中的气体为( )
11. 如图所示的演示实验中,集气瓶中的气体为( ) A、二氧化碳 B、氧气 C、氢气 D、氮气12. 下列关于实验装置用法错误的是( )。
A、二氧化碳 B、氧气 C、氢气 D、氮气12. 下列关于实验装置用法错误的是( )。 A、装置①可用于制二氧化碳 B、装置②可用于制氧气 C、装置③可用于收集二氧化碳 D、装置④可用于收集氢气13. 如图是实验室制备、收集、验满、验证性质的操作,其中正确的是( )A、制备
A、装置①可用于制二氧化碳 B、装置②可用于制氧气 C、装置③可用于收集二氧化碳 D、装置④可用于收集氢气13. 如图是实验室制备、收集、验满、验证性质的操作,其中正确的是( )A、制备 B、收集
B、收集  C、
C、 验满
D、验证性质
验满
D、验证性质  14. 下列关于催化剂的叙述正确的是( )A、能加快化学反应速度 B、能减慢化学反应速度 C、能改变化学反应速度 D、能使任何物质间都发生化学反应15. 实验室用过氧化氢制取氧气的装置,如图 所示,当过氧化氢滴入锥形瓶中时,锥形瓶中气体的压强( )
14. 下列关于催化剂的叙述正确的是( )A、能加快化学反应速度 B、能减慢化学反应速度 C、能改变化学反应速度 D、能使任何物质间都发生化学反应15. 实验室用过氧化氢制取氧气的装置,如图 所示,当过氧化氢滴入锥形瓶中时,锥形瓶中气体的压强( ) A、大于大气压 B、小于大气压 C、等于大气压 D、无法确定16. 用排水法收集氧气时,不正确的操作是 ( )A、集气瓶装满水,不留空气泡,以使所得氧气纯净 B、瓶口向下,直立水槽中,以使集气瓶中的水能被氧气充分排出 C、当导管口开始有气泡冒出时,应立刻收集,以免造成氧气的浪费 D、当气泡连续均匀地冒出后,再收集17. 区别空气和氧气两瓶气体的方法是 ( )A、比较气体的颜色 B、闻气味 C、用带火星的木条试验 D、分别倒入澄清的石灰水18. 在利用一定质量的双氧水和二氧化锰制取氧气的实验过程中,相关量的变化与时间的对应关系如图所示,则纵坐标可能表示( )
A、大于大气压 B、小于大气压 C、等于大气压 D、无法确定16. 用排水法收集氧气时,不正确的操作是 ( )A、集气瓶装满水,不留空气泡,以使所得氧气纯净 B、瓶口向下,直立水槽中,以使集气瓶中的水能被氧气充分排出 C、当导管口开始有气泡冒出时,应立刻收集,以免造成氧气的浪费 D、当气泡连续均匀地冒出后,再收集17. 区别空气和氧气两瓶气体的方法是 ( )A、比较气体的颜色 B、闻气味 C、用带火星的木条试验 D、分别倒入澄清的石灰水18. 在利用一定质量的双氧水和二氧化锰制取氧气的实验过程中,相关量的变化与时间的对应关系如图所示,则纵坐标可能表示( ) A、水的质量 B、氧气的质量 C、双氧水的质量 D、二氧化锰的质量19. 实验室加热氯酸钾和二氧化锰混合物制取氧气的过程中,二氧化锰的质量与反应时间的关系图像正确的是( )A、
A、水的质量 B、氧气的质量 C、双氧水的质量 D、二氧化锰的质量19. 实验室加热氯酸钾和二氧化锰混合物制取氧气的过程中,二氧化锰的质量与反应时间的关系图像正确的是( )A、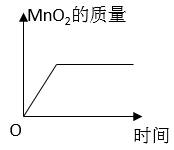 B、
B、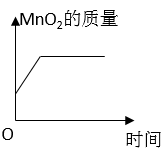 C、
C、 D、
D、 20. 为了保证长时间(节能)潜航,潜水艇里要配备氧气发生装置,下列反应最适于潜水艇里供给氧气的是( )A、2KClO3 2KCl+3O2↑ B、2H2O 2H2↑+O2↑ C、2Na2O2+2CO2=2Na2CO3+O2 D、4HNO3 2H2O+4NO2↑+O2↑
20. 为了保证长时间(节能)潜航,潜水艇里要配备氧气发生装置,下列反应最适于潜水艇里供给氧气的是( )A、2KClO3 2KCl+3O2↑ B、2H2O 2H2↑+O2↑ C、2Na2O2+2CO2=2Na2CO3+O2 D、4HNO3 2H2O+4NO2↑+O2↑二、填空题
-
21. 实验室提供H2O2溶液、二氧化锰、KClO3和KMnO4四种药品及下列装置

根据要求完成下列问题:
(1)、根据提供的药品,写出一种实验室制取O2的化学方程式;(2)、选择装置B和C制取氧气的主要步骤有:①将导气管移出水槽;②加热;③装药品;④收集;⑤熄灭酒精灯;⑥检查装置气密性。正确的操作顺序为。22. 如图是常见的气体发生装置和收集装置。 (1)、写出下列指定序号所指仪器的名称:④;(2)、实验室用氯酸钾和二氧化锰制取氧气的发生装置可以选用(填代号);(3)、在 O2、CO2 中,可以用 C 装置收集的气体是;(4)、制取气体前应先检查装置的气密性,若按 F 图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是(填序号)。
(1)、写出下列指定序号所指仪器的名称:④;(2)、实验室用氯酸钾和二氧化锰制取氧气的发生装置可以选用(填代号);(3)、在 O2、CO2 中,可以用 C 装置收集的气体是;(4)、制取气体前应先检查装置的气密性,若按 F 图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是(填序号)。a.将烧杯换成液面高度相同水槽
b.导管伸入水中位置过深,气体无法逸出
c.先用手捂住试管壁,再将导管另一端插入水中
c.可能是塞子未塞紧
23. 根据表中五种气体在标准状况下的密度和溶解性,回答下列问题:1
空气
NH3
CH4
HCl
O2
密度/g•L-1
1.293
0.771
0.717
1.629
1.43
溶解性
——
极易溶
难溶
极易溶
难溶
(1)、既能用排水法,又能用向上排空气法收集的气体是。(2)、用如图所示盛满水的集气瓶收集 CH4 , 气体应从端进入。 24. 过氧化氢溶液分解反应的催化剂很多。化学兴趣小组的同学设计如上图方案一和方案二实验,比较两种物质的催化效果,其中观察效果较差的是 ,(选填“方案一”或“方案二”)为什么?。
24. 过氧化氢溶液分解反应的催化剂很多。化学兴趣小组的同学设计如上图方案一和方案二实验,比较两种物质的催化效果,其中观察效果较差的是 ,(选填“方案一”或“方案二”)为什么?。
 25. 如图是实验室常用的气体收集装置,据图回答下列问题。
25. 如图是实验室常用的气体收集装置,据图回答下列问题。 (1)、图甲装置收集氧气,操作的正确顺序为(填编号)
(1)、图甲装置收集氧气,操作的正确顺序为(填编号)①当气泡连续均匀地冒出时,将导管伸入集气瓶口
②将装满水的集气瓶倒置在水槽中
③当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面放置
④熄灭酒精灯
⑤导管移出水面
(2)、若用乙装置进行排空气法收集氧气,气体应从(填“a”或“b”)端通入。26. 以下是小明在做“加热高锰酸钾制取氧气”实验时的过程,请据图回答: (1)、装配加热高锰酸钾制取氧气的发生装置时,需用到图甲中仪器的有 (填数字序号)(2)、若高锰酸钾里有杂质(杂质加热不分解),为了测定高锰酸钾的纯度,小明用图乙所示的量筒来测量产生氧气的体积。为了使得到的实验数据准确,他开始收集气体的时间点应该是 。A、检验产生的气体纯度之后 B、导管口有气泡刚冒出时 C、冒出气泡连续且均匀时27. 某兴趣小组加热一定量的氯酸钾和二氧化锰的混合物制取氧气,用如图所示的装置连接,粗略测量生成氧气的体积。
(1)、装配加热高锰酸钾制取氧气的发生装置时,需用到图甲中仪器的有 (填数字序号)(2)、若高锰酸钾里有杂质(杂质加热不分解),为了测定高锰酸钾的纯度,小明用图乙所示的量筒来测量产生氧气的体积。为了使得到的实验数据准确,他开始收集气体的时间点应该是 。A、检验产生的气体纯度之后 B、导管口有气泡刚冒出时 C、冒出气泡连续且均匀时27. 某兴趣小组加热一定量的氯酸钾和二氧化锰的混合物制取氧气,用如图所示的装置连接,粗略测量生成氧气的体积。 (1)、B和C装置中收集氧气的装置是 。(2)、A装置试管中原有空气也会被收集到集气瓶中,这对测量生成的氧气体积的影响是(选填“偏大”“偏小”或者“不影响”)。(3)、充分加热反应后,反应结束,小科同学想回收二氧化锰,于是他将回收的固体溶解,那么,他下一步进行的操作应该是。28. 如图A~E是实验室制取气体的常用装置。请根据要求回答下列问题。
(1)、B和C装置中收集氧气的装置是 。(2)、A装置试管中原有空气也会被收集到集气瓶中,这对测量生成的氧气体积的影响是(选填“偏大”“偏小”或者“不影响”)。(3)、充分加热反应后,反应结束,小科同学想回收二氧化锰,于是他将回收的固体溶解,那么,他下一步进行的操作应该是。28. 如图A~E是实验室制取气体的常用装置。请根据要求回答下列问题。 (1)、图中的五种物质是教材中出现的物质,在一定条件下,都可以产生氧气。请你写出图中物质X制取氧气的化学方程式 。
(1)、图中的五种物质是教材中出现的物质,在一定条件下,都可以产生氧气。请你写出图中物质X制取氧气的化学方程式 。 (2)、实验室用装置B或C来做为制取氧气的发生装置,装置B与C比较,装置B的优点是。(3)、若选用装置F收集氧气,氧气应从(填“能够控制反应速率”或“b”)进入F中。29. 如图是“加热高锰酸钾制取氧气”实验的部分仪器或装置。
(2)、实验室用装置B或C来做为制取氧气的发生装置,装置B与C比较,装置B的优点是。(3)、若选用装置F收集氧气,氧气应从(填“能够控制反应速率”或“b”)进入F中。29. 如图是“加热高锰酸钾制取氧气”实验的部分仪器或装置。
 (1)、连接发生装置时,需要用到图甲中的仪器有(填数字序号)。(2)、若高锰酸钾里有杂质(杂质受热不分解),为了测定高锰酸钾的纯度,通过图乙装置收集并测量氧气的体积。为了使实验数据准确,开始收集气体的时间应该是( )A、检验氧气的纯度后 B、导管口有气泡冒出时 C、冒出的气泡连续均匀时30. 如图所示装置可用于收集氧气,请回答下列问题。
(1)、连接发生装置时,需要用到图甲中的仪器有(填数字序号)。(2)、若高锰酸钾里有杂质(杂质受热不分解),为了测定高锰酸钾的纯度,通过图乙装置收集并测量氧气的体积。为了使实验数据准确,开始收集气体的时间应该是( )A、检验氧气的纯度后 B、导管口有气泡冒出时 C、冒出的气泡连续均匀时30. 如图所示装置可用于收集氧气,请回答下列问题。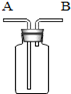 (1)、用向上排空气法收集氧气,则氧气应从端导管通入。若要检查已收集满氧气,可将带火星的木条放在端导管口处;(2)、若用排水法收集氧气,可使集气瓶中装满水,氧气从端导管通入。
(1)、用向上排空气法收集氧气,则氧气应从端导管通入。若要检查已收集满氧气,可将带火星的木条放在端导管口处;(2)、若用排水法收集氧气,可使集气瓶中装满水,氧气从端导管通入。三、解答题
-
31. 由实验测知:取3.5gKMnO4晶体加热到220℃,分解放出的氧气多于按下式计算的理论量。按下式计算的理论量为放出氧气0.354g。
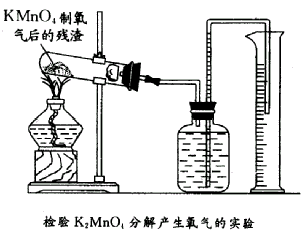
换算成标准状况下的体积为248 mL,而实际测得的氧气为308 mL(标准状况),超过理论量为:(308一248)mL=60mL。试回答:
(1)、怎样用实验证明:超理论量的氧气不是来自MnO2(2)、怎样用实验证明超理论量的氧气是由K2MnO4分解产生的?(要求用KMnO4制取氧气后的残渣实验,如所示。)(3)、怎样从“最后残渣”中分离出MnO2?32. 在流感高发时期,医院里常用过氧化氢(H2O2)作为消毒液。(1)、下列有关过氧化氢的说法正确的是。①它是由氢气和氧气组成的 ②它是由氢元素和氧元素组成的
③它是由一个氢分子和一个氧分子构成的 ④它由两个氢元素和两个氧元素组成
(2)、若用质量分数为10%的H2O2溶液(密度已知),配制680g质量分数为5%的H2O2溶液做消毒液。现提供下列器材:酒精灯、量筒、胶头滴管、烧杯、漏斗,配制过程中一定不需要的是。(3)、若用配制好的5%的过氧化氢溶液制取干燥的氧气,按气体流向,图中导管编号的连接顺序依次是(填写图中的数字序号)。
 33. 图是电解水的简易装置,试回答下列问题:
33. 图是电解水的简易装置,试回答下列问题:
 (1)、实验反应的文字表达式是;(2)、实验中,A、B试管中气体的体积与时间的关系如图所示。由图可知A气体是 , 直流电源的左侧是极;(3)、为了加快电解水的速度,常在水中加入一定量的稀硫酸。若实验前加入20克9.8%的稀硫酸,实验结束后测得剩余溶液的质量刚好为100克,则剩余溶液中溶质的质量分数为多少?
(1)、实验反应的文字表达式是;(2)、实验中,A、B试管中气体的体积与时间的关系如图所示。由图可知A气体是 , 直流电源的左侧是极;(3)、为了加快电解水的速度,常在水中加入一定量的稀硫酸。若实验前加入20克9.8%的稀硫酸,实验结束后测得剩余溶液的质量刚好为100克,则剩余溶液中溶质的质量分数为多少?
四、实验探究题
-
34. 小嘉用H2O2溶液制取氧气时,在烧瓶中加入50毫升水及0.5克MnO2 , 再往分液漏斗中加入30毫升15%的H2O2溶液。为什么要加入50毫升水呢?查阅资料发现:在不加入水时,若注入H2O2溶液速度过快,反应会过于刷烈而引发事故。
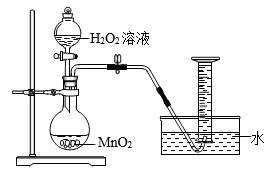
【提出问题】水是如何减缓该反应速度的呢?
【建立假设】水可以降低H2O2溶液浓度,从而减缓反应速度
【实验方案】他利用如图装置,在相同条件下,分别用30毫升的1%、3%和7%的H2O2溶液进行实验, 观察并比较。
【实验结论】加水降低了H2O2溶液的浓度, 使反应速度变慢。
【交流反思】
(1)、为了更好地比较反应的快慢,需控制三次实验中滴加H2O2溶液的相同。(2)、判断产生氧气的速度时,可以通过观察产生气泡的快慢,还可以比较。(3)、【继续探究】针对提出的问题,他又利用如图装置,用3%的H2O2溶液分别在0℃、20℃和60℃的条件下进行实验。进行该实验所基于的假设是。35. 某同学为了探究二氧化锰对H2O2分解速率的影响,利用下图所示装置(夹持装置略去)进行实验,其中实验1、实验2加入二氧化锰,实验3不加,实验数据记录如下:
实验1
实验2
实验3
2%的H2O2溶液体积/毫升
20
20
20
温度/摄氏度
20
80
20
相同时间集气瓶内气体体积
较多
最多
最少
(1)、三组实验中,分解速率最快的是 , 你的判断依据是。(2)、实验2中测定的反应速率往往相比真实值会偏大,其原因是。36. 某兴趣小组同学对“双氧水分解产生氧气的速率与哪些因素有关”这一问题展开探究。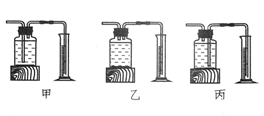
双氧水的质量
双氧水的浓度
?
Ⅰ
50.0g
1%
Ⅱ
50.0g
2%
Ⅲ
50.0g
4%
(1)、上述表格中?处应填的内容是。(2)、根据表格的设计,实验探究的问题是:。(3)、本实验中,测量O2体积的装置是图。五、综合说理题
-
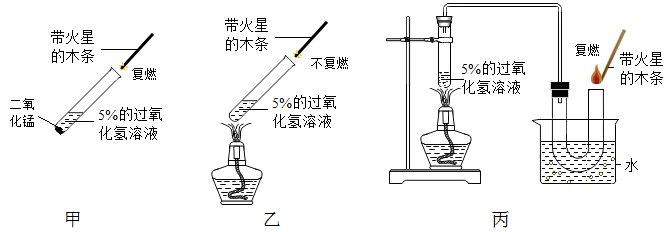
37. 过氧化氢(H2O2)俗称双氧水,常温下是一种无色液体,如图甲过氧化氢在二氧化锰催化作用下,可分解得到氧气,使带火星的木条复燃。如图乙在加热的条件下,它能分解生成氧气和水。研究表明,将新制的5%的双氧水溶液加热到65℃时就有氧气产生,加热到80℃时就有较多氧气生成.某同学用如图乙所示的装置用上述方法制得氧气,用带火星的木条直接在试管口检验,结果木条不能复燃。他查阅资料知,氧气浓度低于一定值时,不能使带火星的木条复燃。于是将实验装置改成如图丙,结果木条复燃。请对上述现象作出合理解释。
 38. 某同学在实验室里用高锰酸钾和二氧化锰加热制取氧气,实验结束时发现大试管已破裂,请你帮他分析造成试管破裂的可能原因是什么?(写出三条即可)
38. 某同学在实验室里用高锰酸钾和二氧化锰加热制取氧气,实验结束时发现大试管已破裂,请你帮他分析造成试管破裂的可能原因是什么?(写出三条即可)