高中化学人教版(2019)必修第一册第二章第一节 钠及其化合物
试卷更新日期:2021-07-07 类型:同步测试
一、单选题
-
1. 在溶液中加入足量 Na2O2 后仍能大量共存的离子组是( )A、 、Ba2+、Cl-、 B、Na+、Cl-、S2−、I- C、Ca2+、Mg2+、 、Cl- D、K+、 、Cl-、2. 下列关于钠的说法不正确的是( )A、金属钠和氧气反应,条件不同,产物不同 B、少量金属钠通常保存在煤油中 C、钠与水反应时,钠熔成小球在水面四处游动 D、由于钠比较活泼,所以它能从溶液中置换出金属活动性顺序表中钠后面的金属3. 在钠的下列用途中,利用的是钠的物理性质的是( )
①制取过氧化钠等化合物 ②制钠钾合金,作快中子反应堆的热交换剂 ③还原钛等金属 ④制高压钠灯
A、①② B、①③ C、②④ D、④4. 化学与生产、生活密切相关。下列说法错误的是:( )A、活性炭可用于净水 B、碳酸钠可用作糕点膨松剂 C、过氧化钠可用作呼吸面具供氧剂 D、氧化钙可用作食品干燥剂5. 下列关于钠的说法中正确的是( )A、金属钠保存在煤油中,所以钠着火时,可用煤油来灭火 B、金属钠久置空气中最终转变为Na2O2 C、钠可以将钛、铌等金属从其氯化物中水溶液中置换出来 D、氧化钠可以转化为过氧化钠,过氧化钠更稳定6. 下列金属化合物中最方便用于潜水艇舱内供氧的是( )A、KMnO4 B、KClO3 C、KNO3 D、Na2O27. 下列有关 Na2CO3 和 NaHCO3 比较中,错误的是( )A、相同条件下在水中的溶解度:Na2CO3>NaHCO3 B、相同条件下与等浓度的盐酸反应的剧烈程度:Na2CO3>NaHCO3 C、热稳定性:Na2CO3>NaHCO3 D、等质量的碳酸钠和碳酸氢钠与足量盐酸反应放出气体的量:Na2CO3<NaHCO38. 下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )选项
陈述Ⅰ
陈述Ⅱ
判断
A
碳酸钠溶液可用于治疗胃病
Na2CO3可与盐酸反应
Ⅰ对,Ⅱ对,有
B
向Na2O2的水溶液中滴入酚酞变红色
Na2O2与水反应生成氢氧化钠
Ⅰ对,Ⅱ错,无
C
金属钠保存在煤油中,以隔绝空气
常温下,金属钠在空气中会生成过氧化钠
Ⅰ对,Ⅱ对,有
D
过氧化钠可用于航天员的供氧剂
Na2O2能和CO2、H2O反应生成O2
Ⅰ对,Ⅱ对,有
A、A B、B C、C D、D9. 用光洁的铂丝蘸取无色溶液,在酒精灯上灼烧时观察到黄色火焰,则下列叙述正确的是( )A、只含有Na+ B、一定含有Na+ ,也可能含有K+ C、既含有Na+ , 又含有K+ D、可能含有Na+或K+中一种10. 下列关于Na2CO3、NaHCO3的说法正确的是( )A、受热时Na2CO3较NaHCO3更不稳定,更易分解产生CO2 B、等质量的Na2CO3、NaHCO3与足量盐酸反应,前者产生的CO2更多 C、CaCl2溶液无法鉴别Na2CO3溶液和NaHCO3溶液 D、等物质的量的两种盐与足量盐酸完全反应,Na2CO3所消耗HCl的物质的量是NaHCO3的两倍11. 下列有关Na2CO3和NaHCO3的性质,叙述错误的是( )A、鉴别Na2CO3和NaHCO3可用Ba(OH)2溶液 B、除去Na2CO3固体中混有的少量NaHCO3 , 用加热法 C、向Na2CO3饱和溶液中通入足量CO2 , 有NaHCO3晶体析出 D、分别向等浓度的Na2CO3和NaHCO3溶液中滴加酚酞,前者红色更深12. 探究Na2O2与水的反应,实验如图:
已知:H2O2⇌H++HO 、HO ⇌H++O
下列分析错误的是( )
A、①、⑤中产生的气体能使带火星的木条复燃 B、①、④中均发生了氧化还原反应和复分解反应 C、②、⑤中KMnO4与MnO2的作用不同,产生气体的量也不同 D、沉淀经过滤、洗涤、干燥后称量:④中反应后的沉淀质量小于③中所得沉淀的质量二、多选题
-
13. 下列说法错误的是( )A、钠是电和热的良导体 B、在水中的溶解性:NaHCO3大于Na2CO3 C、明矾净水是由于明矾在水中形成Al(OH)3胶体具有吸附作用 D、某溶液焰色反应时,火焰呈黄色就说明该溶液一定有钠元素,一定没有钾元素14. 将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中,如图所示,2min后,分别取袋内和烧杯内液体进行实验。下列说法正确的是( )
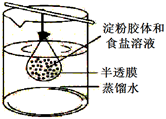 A、烧杯内液体加入硝酸银溶液后产生白色沉淀 B、袋内液体加入硝酸银溶液后产生白色沉淀 C、袋内液体加入碘水后不变蓝 D、烧杯内液体加入碘水后变蓝15. 下列各组中的两种物质作用时,反应条件或反应物的用量比改变,不会引起产物种类改变的是( )A、Na与O2 B、NaOH与CO2 C、Na2O与CO2 D、Na2O2与H2O16.
A、烧杯内液体加入硝酸银溶液后产生白色沉淀 B、袋内液体加入硝酸银溶液后产生白色沉淀 C、袋内液体加入碘水后不变蓝 D、烧杯内液体加入碘水后变蓝15. 下列各组中的两种物质作用时,反应条件或反应物的用量比改变,不会引起产物种类改变的是( )A、Na与O2 B、NaOH与CO2 C、Na2O与CO2 D、Na2O2与H2O16.如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水,已知,过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将发生的现象是( )
 A、U形管内红色褪去 B、试管内溶液变红 C、气球a被吹大 D、U形管水位d<c
A、U形管内红色褪去 B、试管内溶液变红 C、气球a被吹大 D、U形管水位d<c三、填空题
-
17. 钠是一种重要的金属。请回答:将一小块金属钠投入水中,发生反应的离子方程式为;可观察到的实验现象是 。18. 运用分类的方法,可以发现物质及其变化的规律。Na2O与CaO都属于氧化物(填“酸性”或“碱性”)。Na2O可以分别与H2O、CO2、HCl反应,任选两个反应,写出其化学方程式、。19. 按要求填空:
⑴ 钠与水反应(离方程式)
⑵ 除去碳酸氢钠容液中少量碳酸钠<离子方程式)
⑶ 除去碳酸钠固体混有的碳酸氢钠(化学方程式)
⑷ 镁在二氧化碳中燃烧(化学方程式)
⑸ 二氧化碳中混有少量氯化氢(离子方程式)
四、实验探究题
-
20. 某实验小组对Na与水反应产生的H2进行探究,为点燃反应生成的H2 , 他们设计了如图所示的装置。请回答下列问题:
 (1)、写出Na与H2O反应的化学方程式:。(2)、①中反应的现象是。(3)、实验小组在点燃利用①装置制得的H2时,实验失败了。他们认为失败的原因是Na的用量太少,Na与H2O的反应速率太快。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是。(4)、已知钠、煤油、水的密度分别为0.97g·cm-3、0.80g·cm-3、1.00g·cm-3。在②装置中H2的生成速率减慢,原因。21.(1)、钠及其化合物在人类生产生活中有着重大的作用。金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应) 、。(2)、I.加热条件下,Na可以在氧气中燃烧,反应的化学方程式为; 现象是。某课外活动小组设计了如图装置,证实二氧化碳跟过氧化钠反应时需要与水接触。
(1)、写出Na与H2O反应的化学方程式:。(2)、①中反应的现象是。(3)、实验小组在点燃利用①装置制得的H2时,实验失败了。他们认为失败的原因是Na的用量太少,Na与H2O的反应速率太快。于是他们准备增加钠的用量,可老师说太危险,你认为产生危险的原因是。(4)、已知钠、煤油、水的密度分别为0.97g·cm-3、0.80g·cm-3、1.00g·cm-3。在②装置中H2的生成速率减慢,原因。21.(1)、钠及其化合物在人类生产生活中有着重大的作用。金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应) 、。(2)、I.加热条件下,Na可以在氧气中燃烧,反应的化学方程式为; 现象是。某课外活动小组设计了如图装置,证实二氧化碳跟过氧化钠反应时需要与水接触。 (3)、(装置分析)
(3)、(装置分析)装置①中反应的离子方程式是。
装置②中的试剂是为了除去CO2中混有的HCl,则可选用的试剂为。
a.饱和NaOH溶液 b. 饱和Na2CO3溶液 c.饱和NaHCO3溶液
装置③中的试剂是。
(4)、(进行实验)步骤1:打开弹簧夹K2 , 关闭K1 , 打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。
步骤2:打开弹簧夹K1 , 关闭K2 , 打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。
步骤1和步骤2中,a处带火星的木条产生的实验现象分别是、。
(5)、过氧化钠跟二氧化碳反应的化学方程式并用双线桥标出电子转移:。(6)、若要证明CO2和Na2O2发生了反应,需要取出少量反应后的固体,(请补全实验方案)。(7)、Ⅱ.面粉发酵时会产生有机酸(用HA表示其化学式,HA酸性强于碳酸),影响口感。我们可以加入膨松剂(主要含NaHCO3),那么蒸出来的馒头蓬松柔软,且口感好。若加入过量的膨松剂,请写出蒸馒头时反应的化学方程式 , 。该过程能体现出Na2CO3和NaHCO3的热稳定性>。五、综合题
-
22. 钠、碳及它们的化合物在生产、生活中有着重要的用途。(1)、某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
① KClO4的名称是 , 具有(填“还原性”或“氧化性”)。
② Fe2O3可处理产生的Na,反应为6Na+Fe2O3 =3Na2O+2Fe,反应中Na作(填“还原剂”或“氧化剂”)。
反应过程中氧化产物与还原产物的个数比为:。
(2)、Na2O2可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装置探究Na2O2与CO2的反应。请回答下列问题: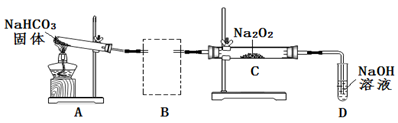
①根据实验目的,虚线框中的装置所用的试剂为。
②装置C中观察到的现象是 , 反应的化学方程式是。
③装置A的作用是制备CO2 , 写出A中发生反应的化学方程式是。
六、推断题
-
23. A~H为中学化学中常见物质,其转化关系如图所示,其中“O”代表化合物,“口”代表单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体,F为金属单质。请回答下列问题:
 (1)、G的化学式为 , G中阴、阳离子个数比为 , 每生成1 mol G转移电子的物质的量为。(2)、A、D的水溶液均呈(填“酸性”“碱性”或“中性”)。反应①②③④中属于氧化还原反应的有个。A~H中焰色呈黄色的物质有种。(3)、写出下列反应的化学方程式。
(1)、G的化学式为 , G中阴、阳离子个数比为 , 每生成1 mol G转移电子的物质的量为。(2)、A、D的水溶液均呈(填“酸性”“碱性”或“中性”)。反应①②③④中属于氧化还原反应的有个。A~H中焰色呈黄色的物质有种。(3)、写出下列反应的化学方程式。: , :。
24. 已知A、F为金属单质,C是淡黄色粉末,回答下题。 (1)、实验室中A常常保存在中,若将0.1mol C直接转化成D,转移电子数为个。(2)、写出E转化为G的离子反应方程式。(3)、写出D与J混合的离子反应方程式。(4)、用化学方程式表示沉淀H转化成I颜色发生变化的原因:。(5)、直接向K溶液中加入C固体,写出可能出现的现象:。(6)、向盛有L溶液的水槽中加入一小块金属A,下列现象描述不符合实际情况的是。
(1)、实验室中A常常保存在中,若将0.1mol C直接转化成D,转移电子数为个。(2)、写出E转化为G的离子反应方程式。(3)、写出D与J混合的离子反应方程式。(4)、用化学方程式表示沉淀H转化成I颜色发生变化的原因:。(5)、直接向K溶液中加入C固体,写出可能出现的现象:。(6)、向盛有L溶液的水槽中加入一小块金属A,下列现象描述不符合实际情况的是。a.金属A浮在液面,并四处游动
b.金属A会熔化成一个小球
c.反应开始后,溶液由无色变成红色
d.恢复到室温时,烧杯底部有固体物质析出
-