浙教版科学八下专题复习之微粒的模型与符号(优生加练)
试卷更新日期:2021-07-07 类型:复习试卷
一、单选题
-
1. X元素1个原子的质量是m克,Y元素的相对原子质量为A;化合物XY2的相对分子质量是M,则W克XY2中含有Y的原子数是( )A、 B、 C、 D、2. 由Na2SO4和CaSO4组成的混合物中,测知氧元素的质量分数为46%.若再计算混合物中的下列各项:①硫元素的质量分数 ②钠元素的质量分数 ③CaSO4的质量分数 ④Na2SO4和CaSO4的质量比 ⑤CaSO4的质量,以下判断正确的是( )A、都能确定 B、都不能确定 C、只有①能确定 D、只有⑤不能确定3. 目前农村正在推广“测土配方施肥”技术,农技员对某土地检测后给出了施肥配方,该土壤施加NH4NO3 , K2CO3;若测定该混合化肥中氮元素的质量分数为28%,则固体混合物中K2CO3的质量分数为( )A、85% B、20% C、25% D、80%4. 小智和小临在校实验室发现一锥形瓶内盛有盐酸和氯化铜的混合溶液100克,他们向其中加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量m1与加入的氢氧化钠溶液质量m2的变化关系如图所示。他们展开讨论正确的是( )
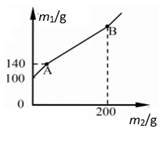 A、反应至A点时,所加NaOH溶液的质量为60克 B、反应至B点时,锥形瓶内溶液中NaCl的质量为29.25克 C、反应至B点时,锥形瓶内溶液的质量为300克 D、反应至A点时,锥形瓶内溶液中NaCl的质量为11.7克5. 已知FeSO4、Fe2(SO4)3混合物中铁元素的质量分数为a%,则硫元素的质量分数为( )A、1-a% B、 C、 D、无法计算6. 某无色气体可能含有CH4、CO、H2中的一种或几种,依次进行以下实验(假设每一步反应或吸收均完全):①将无色气体充分燃烧;②燃烧后生成的气体通过盛浓硫酸的装置,装置的质量增加7.2g;③再将剩余气体通过盛NaOH溶液的装置。装置的质量增加8.8g。下列推断错误的是( )A、原无色气体中可能只含H2和CH4 B、原无色气体中可能只含CH4 C、原无色气体中可能只含CO和H2 D、原无色气体中一定含有碳元素、氢元素7. 某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每一步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g。下列关于气体X成分的分析中,错误的是( )
A、反应至A点时,所加NaOH溶液的质量为60克 B、反应至B点时,锥形瓶内溶液中NaCl的质量为29.25克 C、反应至B点时,锥形瓶内溶液的质量为300克 D、反应至A点时,锥形瓶内溶液中NaCl的质量为11.7克5. 已知FeSO4、Fe2(SO4)3混合物中铁元素的质量分数为a%,则硫元素的质量分数为( )A、1-a% B、 C、 D、无法计算6. 某无色气体可能含有CH4、CO、H2中的一种或几种,依次进行以下实验(假设每一步反应或吸收均完全):①将无色气体充分燃烧;②燃烧后生成的气体通过盛浓硫酸的装置,装置的质量增加7.2g;③再将剩余气体通过盛NaOH溶液的装置。装置的质量增加8.8g。下列推断错误的是( )A、原无色气体中可能只含H2和CH4 B、原无色气体中可能只含CH4 C、原无色气体中可能只含CO和H2 D、原无色气体中一定含有碳元素、氢元素7. 某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每一步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g。下列关于气体X成分的分析中,错误的是( )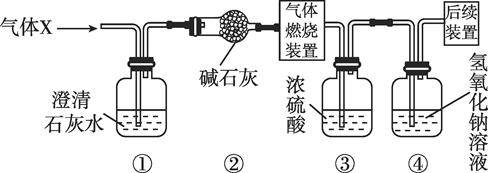
小资料:碱石灰的主要成分是氧化钙和氢氧化钠
A、一定没有二氧化碳 B、可能含有甲烷和氢气 C、可能只有甲烷 D、可能含有氢气和一氧化碳8. 为测定某含有氧化铁、四氧化三铁和氧化亚铁的混合物的组成,现取2.9g该混合物与足量CO充分反应,测得生成铁的质量为2.1g,则混合物中氧化亚铁的质量可能为( )A、0.7g B、1.1g C、1.5g D、1.9g9. 某混合气体可能含有CO、CO2、CH4和HCl中的一种或几种,为了确定其成分,将混合气体按如图所示装置进行实验(假设各步均充分反应或吸收),结果装置A中的石灰水不变浑浊,但混合气体的体积明显减小;装置D增重1.8g;装置E增重2.4g,下列分析正确的是( ) A、装置A中石灰水不变浑浊,所以气体中一定不含二氧化碳 B、装置C对实验结果不产生影响,所以可以去掉装置C以简化实验方案 C、后续装置的目的是阻止空气中的二氧化碳进入装置E中,干扰CO的检验 D、该混合气体成分可能是CH4 和CO10. 实验室用氯酸钾和二氧化锰制取氧气,加热一段时间后剩余固体混合物 10g,继续加热至完全反应后固体变为 9.04g,再将固体加水充分溶解过滤、干燥得到 1.59g 黑色固体。求 10g 剩余固体混合物中氯元素的质量分数为( )A、7.1% B、17.75% C、35.5% D、42.6%11. 某无色气体 X 可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,小科同学取一定量该气体按下图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中一直无明显变化,装置③增重 1.8 g,装置④增重 2.2 g。下列关于气体 x 成分的分析中, 错误的是( )
A、装置A中石灰水不变浑浊,所以气体中一定不含二氧化碳 B、装置C对实验结果不产生影响,所以可以去掉装置C以简化实验方案 C、后续装置的目的是阻止空气中的二氧化碳进入装置E中,干扰CO的检验 D、该混合气体成分可能是CH4 和CO10. 实验室用氯酸钾和二氧化锰制取氧气,加热一段时间后剩余固体混合物 10g,继续加热至完全反应后固体变为 9.04g,再将固体加水充分溶解过滤、干燥得到 1.59g 黑色固体。求 10g 剩余固体混合物中氯元素的质量分数为( )A、7.1% B、17.75% C、35.5% D、42.6%11. 某无色气体 X 可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,小科同学取一定量该气体按下图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中一直无明显变化,装置③增重 1.8 g,装置④增重 2.2 g。下列关于气体 x 成分的分析中, 错误的是( )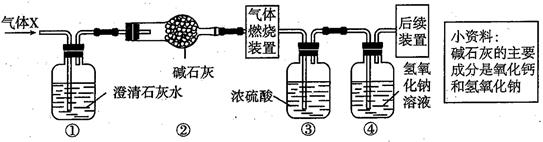 A、一定没有二氧化碳 B、可能含有甲烷和氢气 C、可能只有甲烷 D、可能是氢气和一氧化碳12. 现有一份氧元素质量分数为90%的过氧化氢溶液,加入MnO2充分反应,得到液体的质量为90g(不考虑操作过程中液体的损失),则生成氧气的质量是( )A、4.8 B、5.2g C、10g D、10.8g13. 某物质可能含有铁的氧化物中的一种或两种,实验测得其中铁元素的质量分数为75%,则该物质可能为( )A、FeO B、Fe3O4和Fe2O3的混合物 C、Fe2O3 D、FeO和Fe2O3的混合物14. 某农场需要购置NH4NO3和CO(NH2)2两种化肥,总质量为100kg,经测得其中含氢元素的质量分数为6%,则两种化肥中含氮元素的总质量为( )A、36kg B、40kg C、42kg D、50kg15. 在O2和CO2的混合气体中,碳元素的质量分数是24%,则O2和CO2的质量比是( )A、2∶5 B、3∶1 C、3∶22 D、8∶1116. 某有机物在空气中完全燃烧时生成二氧化碳和水的质量比为11∶9,则该有机物可能是( )A、C2H2 B、C2H5OH C、CH3COOH D、CH3OH17. 取一定质量的CaCO3固体高温加热一段时间后,冷却,测得剩余固体的质量为8.0g,其中钙元素质量分数为50.0%。下列判断正确的是( )A、生成2.0gCO2气体 B、原来CaCO3的质量为14.5g C、剩余8.0g固体为纯净物 D、剩余8.0g固体中加入稀盐酸无明显现象18. 一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成物只有CO、CO2和H2O,且总质量为20.8g,其中H2O的质量为10.8g,则CO2的质量为( )A、5.6g B、8.8g C、4.4g D、4.8g19. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量变化情况如图所示,下列说法错误的是( )
A、一定没有二氧化碳 B、可能含有甲烷和氢气 C、可能只有甲烷 D、可能是氢气和一氧化碳12. 现有一份氧元素质量分数为90%的过氧化氢溶液,加入MnO2充分反应,得到液体的质量为90g(不考虑操作过程中液体的损失),则生成氧气的质量是( )A、4.8 B、5.2g C、10g D、10.8g13. 某物质可能含有铁的氧化物中的一种或两种,实验测得其中铁元素的质量分数为75%,则该物质可能为( )A、FeO B、Fe3O4和Fe2O3的混合物 C、Fe2O3 D、FeO和Fe2O3的混合物14. 某农场需要购置NH4NO3和CO(NH2)2两种化肥,总质量为100kg,经测得其中含氢元素的质量分数为6%,则两种化肥中含氮元素的总质量为( )A、36kg B、40kg C、42kg D、50kg15. 在O2和CO2的混合气体中,碳元素的质量分数是24%,则O2和CO2的质量比是( )A、2∶5 B、3∶1 C、3∶22 D、8∶1116. 某有机物在空气中完全燃烧时生成二氧化碳和水的质量比为11∶9,则该有机物可能是( )A、C2H2 B、C2H5OH C、CH3COOH D、CH3OH17. 取一定质量的CaCO3固体高温加热一段时间后,冷却,测得剩余固体的质量为8.0g,其中钙元素质量分数为50.0%。下列判断正确的是( )A、生成2.0gCO2气体 B、原来CaCO3的质量为14.5g C、剩余8.0g固体为纯净物 D、剩余8.0g固体中加入稀盐酸无明显现象18. 一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成物只有CO、CO2和H2O,且总质量为20.8g,其中H2O的质量为10.8g,则CO2的质量为( )A、5.6g B、8.8g C、4.4g D、4.8g19. 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量变化情况如图所示,下列说法错误的是( ) A、该反应中,丁是生成物 B、丙可能是该反应的催化剂 C、该化学反应中甲、丁的质量变化之比为5∶7 D、该化学反应中乙、丁的质量变化之比为1∶420. 实验室常用燃烧的方法测定有机物的组成。现取3.2g某有机物在足量氧气中充分燃烧,生成4.4g二氧化碳和3.6g水,则该有机物中( )A、一定含有C、H、O三种元素 B、只含有C、H两种元素,不含有O元素 C、C、H两种元素的质量比为11∶9 D、一定含有C、H两种元素,可能含有O元素
A、该反应中,丁是生成物 B、丙可能是该反应的催化剂 C、该化学反应中甲、丁的质量变化之比为5∶7 D、该化学反应中乙、丁的质量变化之比为1∶420. 实验室常用燃烧的方法测定有机物的组成。现取3.2g某有机物在足量氧气中充分燃烧,生成4.4g二氧化碳和3.6g水,则该有机物中( )A、一定含有C、H、O三种元素 B、只含有C、H两种元素,不含有O元素 C、C、H两种元素的质量比为11∶9 D、一定含有C、H两种元素,可能含有O元素二、填空题
-
21. 下列分别盛有不同物质的容器中,所盛物质属于单质的是 , 属于混合物的是 , 属于化合物的是(均填容器下的字母)。若C瓶中CO2和CO所含的氧元素的质量相等,则CO2和CO中碳元素的质量比为 , CO2和CO的质量比为。D瓶中保持冰化学性质的最小粒子是(填化学式)。
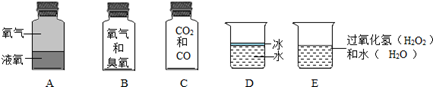 22. 回答下列问题。(1)、下表是元素周期表的一部分,请回答有关问题:
22. 回答下列问题。(1)、下表是元素周期表的一部分,请回答有关问题: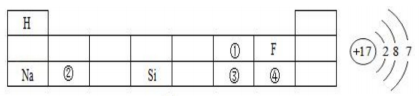
右图表示左表中(填表中序号)的原子结构示意图;得电子后形成的离子符号为;①处元素和②处元素形成常见化合物的化学式为;
(2)、X、Y两种元素的相对原子质量之比为7∶2,X与Y形成的化合物中,X、Y两种元素的质量之比为21∶8,则该化合物的化学式可表示为。若X、Y两种元素的相对原子质量之比为2∶1,由这两种元素形成的化合物中,X、Y的质量之比为2∶3,其中X的化合价为+a。则在该化合物中Y的化合价为。23.(1)、X、Y两种元素组成的化合物甲和乙,甲的化学式为X2Y3 , 其中Y元素的质量分数为50%,乙中X元素的质量分数为60%,则乙的化学式为;(2)、元素X的原子失去1个电子,元素Y的原子得到2个电子后,所形成的离子所带电子数均与氖原子相同,由X、Y两元素的离子形成的化合物的相对分子质量为;(3)、相同质量的H2O2和D2O(D即2H)中氢元素的质量比为。(4)、某样品可能由铁、氧化亚铁、氧化铁和四氧化三铁中的一种或几种组成,现测得该样品中铁元素与氧元素的质量比是21:8;若该样品由两种物质混合而成,则一定不含;若该样品由三种物质混合而成,则一定含有。24. 赤铁矿的主要成分为Fe2O3 , 可用于冶炼铁.某赤铁矿,其中Fe2O3的质量分数为64%,该赤铁矿中铁元素的质量分数是(保留到小数点后面一位)。若以杂质含量为42%的磁铁矿(主要成分四氧化三铁,杂质不含铁元素)为原料代替该赤铁矿炼铁,若要得到相同质量的铁,则磁铁矿与赤铁矿的质量比为。参考答案:44.8%;16:15
25.(1)、某三价金属与氧元素形成的化合物中氧元素质量分数为30%,则该金属的相对原子质量为。(2)、A、B两元素相对原子质量之比为2∶1,仅由这两种元素组成的化合物里,A、B两元素质量比为2∶3,若其中B为-n价,则此化合物中A元素的化合价为。(3)、元素R可与氧形成多种化合物,其中RO中含氧53.33%,那么相对分子质量为76,含氧量为63.16%的R与氧元素形成的化合物的化学式是。(4)、要使CO2和CO中含有相同质量的氧元素,则CO2和CO的质量比是。26. 镁、铝、锌的混合物40g与足量的稀硫酸完全反应,蒸发水后得到136g固体,则反应过程中放出氢气的质量为g。27. 定量研究是重要的研究方法,因此我们应该掌握好有关质量守恒定律的相关知识。(1)、在验证质量守恒定律时,下列A、B、C三个实验设计中能达到实验目的是(选填序号) (2)、氧烛是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域,其主要成分为NaClO3还含有适量的催化剂、成型剂等。氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,主要反应原理为2NaClO3 2X+3O2↑,则X的化学式为。(3)、一定条件下,在一个密闭容器内发生某反应测得反应前后各物质的质量如图所示。下列说法正确的有。
(2)、氧烛是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域,其主要成分为NaClO3还含有适量的催化剂、成型剂等。氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,主要反应原理为2NaClO3 2X+3O2↑,则X的化学式为。(3)、一定条件下,在一个密闭容器内发生某反应测得反应前后各物质的质量如图所示。下列说法正确的有。
A.x的值为11 B.该反应中氧气与水的质量变化之比为6:5
C.w由碳、氢两种元素组成 D.w中碳、氢元素原子个数比为1:4
28. 在研究植物光合作用的实验中,某研究小组在密封的容器A中充入足量的含有同位素14C的14C O2。随着时间的推移,他们发现该植物的不同器官相继出现了同位素14C(如图甲,黑色部分表示检测到同位素14C的部位)。据此回答: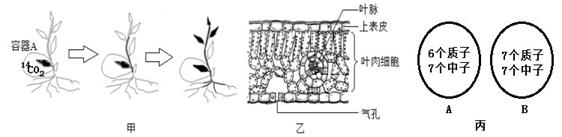 (1)、写出14CO2参加光合作用的场所。(2)、14CO2主要通过图乙中结构进入叶片中;说说14C与图丙中哪个原子是同位素原子。(3)、叶片中的14C主要是通过茎中的哪一部分结构送到该植物的根部。(选填“导管”或“筛管”)29. 某市自来水曾出现过一股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚。将30g邻叔丁基苯酚完全燃烧,生成88g CO2和25.2g H2O(无其他产物)。已知邻叔丁基苯酚的式量为150,求:(1)、CO2中碳、氧元素的质量比为。(2)、30g邻叔丁基苯酚中含碳元素质量是g。(3)、邻叔丁基苯酚的化学式为。30. 现有50g镁、锌、铁的混合物与足量的稀硫酸反应,将混合溶液蒸干后可得218g固体(已换算成无水硫酸盐),则反应生成的氢气质量是。
(1)、写出14CO2参加光合作用的场所。(2)、14CO2主要通过图乙中结构进入叶片中;说说14C与图丙中哪个原子是同位素原子。(3)、叶片中的14C主要是通过茎中的哪一部分结构送到该植物的根部。(选填“导管”或“筛管”)29. 某市自来水曾出现过一股奇怪的味道,经专家多轮综合检测,基本认定引起此次异味的主要物质是邻叔丁基苯酚。将30g邻叔丁基苯酚完全燃烧,生成88g CO2和25.2g H2O(无其他产物)。已知邻叔丁基苯酚的式量为150,求:(1)、CO2中碳、氧元素的质量比为。(2)、30g邻叔丁基苯酚中含碳元素质量是g。(3)、邻叔丁基苯酚的化学式为。30. 现有50g镁、锌、铁的混合物与足量的稀硫酸反应,将混合溶液蒸干后可得218g固体(已换算成无水硫酸盐),则反应生成的氢气质量是。三、解答题
-
31. “珍爱生命,拒绝毒品”是每个公民的责任,但是在某些娱乐场所,还有人服用俗称“摇头丸”的毒品。该毒品能使人手舞足蹈,呈癫狂状态,严重危害人的身心健康和社会稳定,有一种“摇头丸”的化学式为C12HxO2N,相对分子质量为209。试回答下列问题:(1)、该物质的一个分子中含氢原子个。(2)、碳元素与氧元素的质量比为。(3)、418g“摇头丸”中含克氮元素。32. 已知在C2H4、C2H4O和C2H4O6组成的混合物中,经分析发现含氧元素的质量分数为M%,则混合物中氢元素的质量分数是多少?面对这类的题目,我们可以对抽象的问题进行理想化处理。我们把此混合物放入一容器,那么在此容器中便存在大量构成这三种物质的分子:a个C2H4分子,b个C2H4O分子,c个C2H4O6分子。现在我们需取出三个分子,随机的结果有:
①一个C2H4分子,一个C2H4O分子,一个C2H4O6分子;
②一个C2H4分子,二个C2H4O分子;
③一个C2H4O分子,二个C2H4O6分子……
(1)、我们来看这三种情况,我们发现,无论怎么组合(填两种元素名 称)的原子个数比为一定值,且这两种元素所占总物质的质量分数可表示为 , 且碳元素的质量分数可表示为。(2)、拓展:已知在NaHS、MgSO4和NaHSO3组成的混合物中,含硫40%,则氧元素的质量分数为。33. 请根据题目条件进行计算:(1)、X、Y 两元素的相对原子质量之比为 7∶2 ,X 与 Y 形成的化合物中,X、Y 两元素的质量之比为 21∶8 ,则该化合物的化学式可表示为 。(2)、已知 X、Y 两元素的相对原子质量之比是 2∶1,由这两种元素形成的化合物中,X、Y 的质量之比是 2∶3,其中 X 的化合价为+a 。则在化合物中 Y 的化合价为 。(3)、已知有 Na2S、Na2SO3、Na2SO4 三种物质的混合物 100g,测得硫的质量分数为 32%,则混合 物中含氧元素的质量为 .34. 元素周期表是学习和研究化学的重要工具。如图是元素周期表部分内容,请根据表中信息完成相关问题。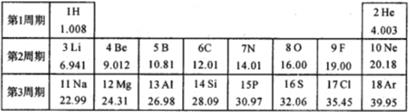 (1)、第三周期中的稀有气体元素的质子数是。(2)、元素周期表的纵行叫做族,分为主族、副族、VⅢ族和0族。主族用字母“A”来表示,共有七个主族,依次用IA族、ⅡA族、ⅢA族、ⅣA族、VA族、ⅥA族、VⅡA族表示。同主族元素化学性质相似。X²+的核外电子数目为18,则X在第四周期第族。(3)、下列各组中的两种元素具有相似化学性质的是 。A、N C B、F Cl C、Mg Al D、Ne Na(4)、核电荷数1-18的非金属元素A和B,可形成原子个数比1:1和2∶1的两种常温下的化合物,写出这两种化合物的化学式。35. 中国是一个人口众多的发展中国家,人们注意到:西方国家的发展模式不完全适用于中国。例如:设想以植物性食物为主的中国人,平均食用牛肉的水平若与美国人相当。则每年需增加粮食3.4 亿吨(这相当于美国一年的粮食产量)如果每吨粮食生产需提供0.1吨氮元素,则:中国每年将需要多供应多少吨尿素(CO(NH2)2)?36. 已知钙是一种非常活泼的金属,易与氧气、水反应,钙与水反应生成氢氧化钙和氢气;加热条件下钙与氮气反应生成CaxNy。小金设计如图装置让钙与氮气反应,并确定其组成CaxNy。
(1)、第三周期中的稀有气体元素的质子数是。(2)、元素周期表的纵行叫做族,分为主族、副族、VⅢ族和0族。主族用字母“A”来表示,共有七个主族,依次用IA族、ⅡA族、ⅢA族、ⅣA族、VA族、ⅥA族、VⅡA族表示。同主族元素化学性质相似。X²+的核外电子数目为18,则X在第四周期第族。(3)、下列各组中的两种元素具有相似化学性质的是 。A、N C B、F Cl C、Mg Al D、Ne Na(4)、核电荷数1-18的非金属元素A和B,可形成原子个数比1:1和2∶1的两种常温下的化合物,写出这两种化合物的化学式。35. 中国是一个人口众多的发展中国家,人们注意到:西方国家的发展模式不完全适用于中国。例如:设想以植物性食物为主的中国人,平均食用牛肉的水平若与美国人相当。则每年需增加粮食3.4 亿吨(这相当于美国一年的粮食产量)如果每吨粮食生产需提供0.1吨氮元素,则:中国每年将需要多供应多少吨尿素(CO(NH2)2)?36. 已知钙是一种非常活泼的金属,易与氧气、水反应,钙与水反应生成氢氧化钙和氢气;加热条件下钙与氮气反应生成CaxNy。小金设计如图装置让钙与氮气反应,并确定其组成CaxNy。
 (1)、连接好装置后检查气密性:关闭活塞K,点燃酒精灯微微加热硬质玻璃管,看到现象说明装置气密性良好。(2)、制备氮化钙的操作步骤是:①打开活塞K通入氮气;②点燃酒精灯,进行反应;③反应结束…④拆除装置,提取产物,测量质量。
(1)、连接好装置后检查气密性:关闭活塞K,点燃酒精灯微微加热硬质玻璃管,看到现象说明装置气密性良好。(2)、制备氮化钙的操作步骤是:①打开活塞K通入氮气;②点燃酒精灯,进行反应;③反应结束…④拆除装置,提取产物,测量质量。请选择步骤③中操作:反应结束后;
A.先熄灭酒精灯, 待玻璃管恢复到室温后,关闭活塞K
B.熄灭酒精灯后直接关闭活塞K
(3)、按上述操作进行实验,若测得硬质玻璃管内产物的质量为4.7克,则x:y=。37. 氢气的储存是科学研究热点之一。X是一种储存氢气的材料,取11.2gX在O2中完全燃烧后只生成8.0gCuO、8.0gMgO(1)、上述燃烧过程中消耗O2的质量为克。(2)、通过计算求X中各元素的原子个数比。(写出计算过程)四、实验探究题
-
38. 只含铜和氧两种元素的固体样品18g,测得铜元素的质量为16g。已知铜的氧化物有CuO和Cu2O。请通过分析或计算回答下列问题:(1)、该样品的组成情况有。(写出所有可能的组成);(2)、若固体样品由两种物质组成,则质量偏少的那种物质在样品中的质量分数为。(用分数表示)39. 俗话说“骨头的精髓在汤里”。有人认为骨头中钙、磷含量雄厚,骨头汤必然钙含量很高,是补钙的好材料。为了验证骨头汤能否有效补钙,某科研小组将猪排骨 500g、蒸馏水 1500mL、食用醋 70mL,加热煮沸后维持 70 分钟,得到骨头汤 1243mL,用仪器检测结果:每 100mL 骨头汤含有 2mg 钙(而每 100mL 牛奶约含有 105mg 钙)。
查阅资料:人体骨骼中的钙存在形式是羟基磷酸钙[Ca10(PO4)6(OH)2],该物质难溶于水。人体平均每天需要补钙 800mg。
(1)、“骨头汤能补钙”中的钙是指 (填字母编号);A、钙离子 B、单质钙 C、钙元素 D、羟基磷酸钙(2)、羟基磷酸钙中磷元素的化合价是价 ;(3)、假设某人只能从骨头汤中获取钙,则此人每天需要喝L 骨 头 汤 ;(4)、某品牌钙片每片的规格是:维生素 D3100IU(相当于 2.5 微克),碳酸钙 1000mg,若某人只从钙片中获取钙,则每天需要服用此品牌钙片片。40. 科学理论的建立要有一个又一个的证据。在研究原子结构的历史进程中,卢瑟福揭开了原子世界一个又一个的奥秘。请回答:(1)、1911年,卢瑟福等人进行了α粒子(α粒子是带两个单位正电荷的氦原子核)散射实验,用一些高速运动的α粒子轰击金箔,发现多数α粒子穿过金箔后仍保持原来的运动方向,但有少数α粒子发生了较大角度的偏转,而极少数α粒子发生反弹。下列说法正确的有 。A、多数α粒子保持原来的运动方向,说明原子核的体积很小 B、少数α粒子发生较大角度偏转,说明原子核带负电 C、极少数α粒子发生反弹,说明原子核的质量很大(2)、1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是。