浙教版科学八下专题复习之微粒的模型与符号(基础巩固)
试卷更新日期:2021-07-07 类型:复习试卷
一、单选题
-
1. 如果用”
 ”表示氧原子,用”
”表示氧原子,用”  ”表示硫原子,则下列模型可以表示二氧化硫分子(SO2)的是( ) A、
”表示硫原子,则下列模型可以表示二氧化硫分子(SO2)的是( ) A、 B、
B、 C、
C、 D、
D、 2. 氮化锶(Sr3N2)是生产高端荧光粉的主要原料。已知Sr3N2中N的化合价为-3,则Sr的化合价为( )A、-3 B、-2 C、+2 D、+33. 2021年4月,我国科学家首次合成的铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数是92。则铀-214原子的核外电子数为( )A、92 B、122 C、214 D、3064. 模型常常可以帮助人们认识和理解一些不能直接观察到的或复杂的事物。仔细观察 下列四幅图片,不属于模型的是( )A、
2. 氮化锶(Sr3N2)是生产高端荧光粉的主要原料。已知Sr3N2中N的化合价为-3,则Sr的化合价为( )A、-3 B、-2 C、+2 D、+33. 2021年4月,我国科学家首次合成的铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数是92。则铀-214原子的核外电子数为( )A、92 B、122 C、214 D、3064. 模型常常可以帮助人们认识和理解一些不能直接观察到的或复杂的事物。仔细观察 下列四幅图片,不属于模型的是( )A、 B、
B、 C、
C、 D、
D、 5. 下列选项不属于模型的是( )A、一种原子结构
5. 下列选项不属于模型的是( )A、一种原子结构 B、氧分子
B、氧分子  C、镁元素Mg
D、U=IR
6. 了解物理规律的发现过程,学会像科学家那样观察和思考,往往比掌握知识本身更重要。下列描述与事实不相符的是( )A、汤姆生发现了比原子小的多的电子 B、法拉第发现了电流周围存在磁场 C、卢瑟福提出原子核式结构模型 D、拉瓦锡通过实验测定了空气中氧气的大致含量7. CeCu2Si2是一种高温超导材料.其中铜元素化合价为+2价,硅元素为-4价,则铈(Ce)元素化合价为( )A、-4 B、-2 C、+2 D、+48. 仔细观察下列四幅图片,不属于模型的是( )A、
C、镁元素Mg
D、U=IR
6. 了解物理规律的发现过程,学会像科学家那样观察和思考,往往比掌握知识本身更重要。下列描述与事实不相符的是( )A、汤姆生发现了比原子小的多的电子 B、法拉第发现了电流周围存在磁场 C、卢瑟福提出原子核式结构模型 D、拉瓦锡通过实验测定了空气中氧气的大致含量7. CeCu2Si2是一种高温超导材料.其中铜元素化合价为+2价,硅元素为-4价,则铈(Ce)元素化合价为( )A、-4 B、-2 C、+2 D、+48. 仔细观察下列四幅图片,不属于模型的是( )A、 B、
B、 C、
C、 D、
D、 9. 地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2 , 主要用于饮用水消毒。实验测得该氧化物中R与O的质量比为71:64,则RO2的化学式为( )A、CO2 B、NO2 C、SO2 D、ClO210. 假设1个甲原子的质量为Akg,1个标准的碳原子的实际质量Bkg,则甲原子的相对原子质量可以表示为( )A、 千克 B、12 C、 D、11. 下列元素分类正确的是( )A、金属元素:钙、镁、钡、铜、铁、汞 B、非金属元素:碳、氢、氧、氮、磷、金 C、稀有元素:氦、氖、氩、氪、氯、氡 D、人体必需的微量元素:铁、碘、氟、硒、钙、铅12. 铀-235是制造原子弹的一种原料,其原子的原子核内有92个质子和143个中子,该原子的核外电子数为( )A、51 B、92 C、143 D、23513. 人们常说豆制品含有丰富的蛋白质,菠菜中含有丰富的铁质,这里的“铁”是指( )A、铁单质 B、铁分子 C、铁原子 D、铁元素14. 模型常常可以帮助人们认识和理解一些不能直接观察的或复杂的事物,仔细观察下列四幅图片:不属于模型的是( )A、
9. 地震过后,防疫部门常用到一种高效安全灭菌消毒剂,该消毒剂可表示为RO2 , 主要用于饮用水消毒。实验测得该氧化物中R与O的质量比为71:64,则RO2的化学式为( )A、CO2 B、NO2 C、SO2 D、ClO210. 假设1个甲原子的质量为Akg,1个标准的碳原子的实际质量Bkg,则甲原子的相对原子质量可以表示为( )A、 千克 B、12 C、 D、11. 下列元素分类正确的是( )A、金属元素:钙、镁、钡、铜、铁、汞 B、非金属元素:碳、氢、氧、氮、磷、金 C、稀有元素:氦、氖、氩、氪、氯、氡 D、人体必需的微量元素:铁、碘、氟、硒、钙、铅12. 铀-235是制造原子弹的一种原料,其原子的原子核内有92个质子和143个中子,该原子的核外电子数为( )A、51 B、92 C、143 D、23513. 人们常说豆制品含有丰富的蛋白质,菠菜中含有丰富的铁质,这里的“铁”是指( )A、铁单质 B、铁分子 C、铁原子 D、铁元素14. 模型常常可以帮助人们认识和理解一些不能直接观察的或复杂的事物,仔细观察下列四幅图片:不属于模型的是( )A、 B、
B、 C、
C、 D、
D、 15. X、Y两元素的相对原子质量之比为7∶2 ,X与Y形成的化合物中,X、Y两元素的质量之比为21∶8 ,则该化合物的化学式可表示为( )A、X3Y2 B、X3Y4 C、X2Y3 D、XY16. 据媒体报道,“金星快车”号探测器发现金星大气中存在15N2。构成15N2的15N具有7个质子和8个中子,则15N的核外电子数为( )A、1 B、7 C、8 D、1517. 高铁酸钠(Na2FeO4)是一种绿色环保高效的水处理剂。高铁酸钠中铁元素的化合价为( )A、+2 B、+3 C、+4 D、+618. 模型方法是学习科学的重要方法。仔细观察下列不属于模型的是( )A、 欧姆定律 B、眼球结构
15. X、Y两元素的相对原子质量之比为7∶2 ,X与Y形成的化合物中,X、Y两元素的质量之比为21∶8 ,则该化合物的化学式可表示为( )A、X3Y2 B、X3Y4 C、X2Y3 D、XY16. 据媒体报道,“金星快车”号探测器发现金星大气中存在15N2。构成15N2的15N具有7个质子和8个中子,则15N的核外电子数为( )A、1 B、7 C、8 D、1517. 高铁酸钠(Na2FeO4)是一种绿色环保高效的水处理剂。高铁酸钠中铁元素的化合价为( )A、+2 B、+3 C、+4 D、+618. 模型方法是学习科学的重要方法。仔细观察下列不属于模型的是( )A、 欧姆定律 B、眼球结构 C、
C、 注意行人
D、
注意行人
D、 一条光线
一条光线
二、填空题
-
19. 写出下列符号中数字“2”的含义。(1)、2H:。(2)、H2O:。20. 右表微粒中,属于同种元素的是。互为同位素原子的是。
组别
质子
中子
电子
A
14
14
14
B
17
18
17
C
17
20
17
D
17
18
18
21. 写出下列符号中数字2的意义。(1)、Cl2。(2)、2H。(3)、Ca2+。22. 写出相应的物质名称或化学式:(1)、硫酸铁;(2)、氢氧化钠;(3)、SO2;(4)、Al2O3;(5)、CaCO3;(6)、硝酸铵.23. 断血流滴丸中含有木犀草素(化学式为C13H2Ox)等黄酮类活性成分,具有止血、抗菌、抗炎及免疫等药理活性。已知木犀草素的相対分子质量为254,请计算:(1)、x的值为。(2)、木犀草素中碳元素的质量分数为(结果精确到0.1%)。24. 下列元素符号书写上都有错误,请改正。(1)、钙CA:(2)、氯CL:(3)、镁Ma:(4)、钠Ne:(5)、汞HG:(6)、氦Hi:25. 根据所给的元素名称填写元素符号①镁 ②铝 ③锂 ④氧 ⑤钙
⑥氩 ⑦氟 ⑧碳 ⑨氯 ⑩磷
26. 根据所给的元素符号填写元素名称①H ②K ③Si ④N ⑤Ne
⑥S ⑦B ⑧Na ⑨Be ⑩He
27. 有机物的命名与它的构成规律紧密相关。如有机物甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8),按此规律,丁烷的化学式为28. 空气中含量最多的元素为 , 地壳中含量最多的元素为 , 地核中含量最多的元素为 , 太阳中含量最多的元素为 , 海水中含量最多的元素为;人体中含量最多的元素为。(均填元素符号)29. H表示的意义有:①;②。30. 原子不是构成物质的最小微粒,它还能再分,原子是由带正电荷的和带负电荷的构成的。原子核在原子中所占的体积 , 核外电子在核外空间做。通过实验,科学家们最终发现,原子核是由更小的两种粒子——和构成。31. 砷(As)是一种非金属元素,它有+3价和+5价,因此可以形成两种含氧酸——砷酸和亚砷酸。砷酸的化学式为。三、解答题
-
32. 如图为某牙膏的部分标签,活性成分单氟磷酸钠的化学式为Na2PO3F,请计算下列问题:
 (1)、单氟磷酸钠中氟元素的质量分数(结果精确到0.1%)。(2)、若牙膏中其它成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为多少克?(结果保留小数点后一位)33. 新装修房间中往往会含有较多的甲醛,人体长期摄人超标的甲醛会对健康造成影响。甲醛的化学式为HCHO,请回答下列问题:(1)、甲醛由种元素组成。(2)、甲醛中碳、氢、氧元素的质量比为。(写最简整数比)(3)、计算甲醛中氢元素的质量分数。(保留两位小数)34. 维生素C(化学式:C6H8O6)对人体皮肤和牙龈健康有重要作用,缺乏维生素C,会引起坏血病,中学生每天需要补充60mg维生素C,请阅读信息后回答:(1)、维生素C中有种元素组成(2)、维生素C分子的相对分子质量是。35. 我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。回答下列问题。(1)、一个青蒿素分子中含有个原子。(2)、青蒿素中的氢元素与氧元素的质量比是。36. 2017年5月18日,国土资源部发布消息,在南海北部1266米深的神狐海域,中国首次海域“可燃冰”试采成功。
(1)、单氟磷酸钠中氟元素的质量分数(结果精确到0.1%)。(2)、若牙膏中其它成分不含氟,则每支这种牙膏中,含Na2PO3F的质量为多少克?(结果保留小数点后一位)33. 新装修房间中往往会含有较多的甲醛,人体长期摄人超标的甲醛会对健康造成影响。甲醛的化学式为HCHO,请回答下列问题:(1)、甲醛由种元素组成。(2)、甲醛中碳、氢、氧元素的质量比为。(写最简整数比)(3)、计算甲醛中氢元素的质量分数。(保留两位小数)34. 维生素C(化学式:C6H8O6)对人体皮肤和牙龈健康有重要作用,缺乏维生素C,会引起坏血病,中学生每天需要补充60mg维生素C,请阅读信息后回答:(1)、维生素C中有种元素组成(2)、维生素C分子的相对分子质量是。35. 我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。回答下列问题。(1)、一个青蒿素分子中含有个原子。(2)、青蒿素中的氢元素与氧元素的质量比是。36. 2017年5月18日,国土资源部发布消息,在南海北部1266米深的神狐海域,中国首次海域“可燃冰”试采成功。查阅资料发现,古代低等生物遗骸大量沉积,经过漫长的地质年代形成石油及天然气,海底的天然气与水在高压低温条件下形成的类冰状的固体物质即“可燃冰”。“可燃冰”为甲烷的水合物,遇火即可燃烧且热值高,是一种环保、高效的新能源。
(1)、若甲烷的水合物化学式为CH4•8H2O,它的相对分子量是160,则CH4•8H2O中CH4的质量分数为;
(2)、可燃冰储存的巨大的化学能量终来自于古代绿色植物通过固定的太阳能;
(3)、可燃冰燃烧时把自己的热量释放出去,就不会再次自动聚集起来供人类重新利用,这说明能量转化具有性;
(4)、人类正面临常规能源枯竭的危机,下列有关能源的认识正确的是 。
A、提高能源利用效率 B、积极寻找替代常规能源的新能源 C、自然界的能量虽然守恒,但还是要节约能源四、实验探究题
-
37. 征服原子——揭开原子的神秘面纱
伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是——一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。
(1)、1803年,近代化学之父,英国科学家道尔顿(Dalton J)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。1811年,意大利化学家阿伏加德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
1897年,汤姆森通过实验发现了 , 进一步发展了原子、分子论。汤姆森主要是纠正了“道尔顿原子论”中的观点。
1911年,卢瑟福又通过实验,推测原子是由构成,并提出了沿用至今的现代原子结构理论。
(2)、原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这三位科学家都运用了来表达他们的理论成果。38.卢瑟福用a粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础,但通过该实验的下述三种现象(如图),不能获得核外电子带有负电荷的结论。
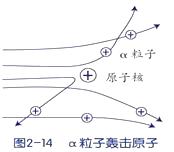
现象1:大多数α粒子能穿透金箔而不改变原来运动方向。
现象2:一小部分α粒子改变原来的运动方向。
现象3:极少数α粒子被弹了回来。
(1)、请你根据原子结构知识分析以上现象产生的原因。①现象1的原因:
②现象2的原因:
(2)、1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是 。