上海市杨浦区2021年中考化学三模试卷
试卷更新日期:2021-07-05 类型:中考模拟
一、单选题
-
1. 元素符号正确的是( )A、mg B、SI C、H D、2O2. 空气中含量最多的气体( )A、二氧化碳 B、氧气 C、水蒸气 D、氮气3. 属于纯净物的是( )A、矿泉水 B、石灰水 C、蒸馏水 D、汽水4. 关于硫酸铜的描述中,错误的是( )A、俗称:胆矾 B、类别:盐 C、式量:160 D、用途:检验水5. 能使紫色石蕊试液变红的是( )A、干冰 B、生石灰 C、大理石 D、纯碱6. 在氧气中燃烧,产生明亮蓝紫色火焰的是()A、硫 B、红磷 C、铁丝 D、氢气7. 由分子构成的物质是( )A、汞 B、氧气 C、氧化铜 D、金刚石8. 分类正确的是( )A、水、铁是单质 B、CO、CH4是可燃性气体 C、酒精、食盐是有机物 D、SO2、CO2是空气污染物9. 使水净化程度最高的是( )A、蒸馏 B、吸附 C、过滤 D、沉淀10. 能鉴别稀硫酸和稀盐酸的试剂是( )A、石蕊试液 B、硝酸银溶液 C、硝酸钡溶液 D、碳酸钠溶液11. 有关置换反应的说法,正确的是( )A、有金属单质生成 B、有化合物生成 C、反应都在常温下进行 D、反应物的化合价都会改变12. 实验设计不合理的是( )




A.探究可燃物燃烧的条件
B.探究Fe、Cu、Ag的活动性
C.探究稀盐酸和氢氧化钠溶液反应是否放热
D.验证质量守恒定律
A、A B、B C、C D、D13. 将一定质量的Zn加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,滤液为无色。下列判断正确的是( )A、滤渣是Ag、Cu B、滤液中最多含有三种溶质 C、反应前后金属固体的质量可能不变 D、向滤液中滴加稀盐酸,产生白色沉淀14. 向盛有铜和氧化铜的烧杯中滴加稀盐酸,反应过程中剩余固体的质量与加入稀盐酸的质量关系如图所示。下列说法错误的是( )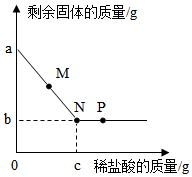 A、M点时,溶液中的溶质是CuCl2 B、N点时,剩余固体是铜 C、P点时,溶液的pH<7 D、混合物中铜的质量为(a-b)g15. 下列叙述正确的是( )A、分子可以构成物质,所以物质一定都是由分子构成的 B、单质只含有一种元素,所以含一种元素的纯净物都是单质 C、碱的溶液呈碱性,所以呈碱性的溶液一定是碱的溶液 D、同素异形体含有相同的元素,所以含相同元素的物质是同素异形体16. 下列物质间的转化,通过一步化学反应不能实现的是( )A、C→CO→CO2 B、Mg→MgO→MgCl2 C、CuO→Cu(OH)2→CuCl2 D、NaOH→NaNO3→NaCl17. 某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取该固体粉末按下列流程进行实验(各步均完全反应)。下列推断正确的是( )
A、M点时,溶液中的溶质是CuCl2 B、N点时,剩余固体是铜 C、P点时,溶液的pH<7 D、混合物中铜的质量为(a-b)g15. 下列叙述正确的是( )A、分子可以构成物质,所以物质一定都是由分子构成的 B、单质只含有一种元素,所以含一种元素的纯净物都是单质 C、碱的溶液呈碱性,所以呈碱性的溶液一定是碱的溶液 D、同素异形体含有相同的元素,所以含相同元素的物质是同素异形体16. 下列物质间的转化,通过一步化学反应不能实现的是( )A、C→CO→CO2 B、Mg→MgO→MgCl2 C、CuO→Cu(OH)2→CuCl2 D、NaOH→NaNO3→NaCl17. 某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取该固体粉末按下列流程进行实验(各步均完全反应)。下列推断正确的是( ) A、固体X可能是混合物 B、溶液Z中只含一种溶质 C、气体M和气体Y都是二氧化碳 D、原固体粉末中没有氧化铜,可能有碳酸钙
A、固体X可能是混合物 B、溶液Z中只含一种溶质 C、气体M和气体Y都是二氧化碳 D、原固体粉末中没有氧化铜,可能有碳酸钙二、填空题
-
18. 二氧化碳与人类的生产、生活密切相关。
①化石燃料是指煤、、天然气;化石燃料燃烧产生过多的CO2 , 会导致的环境问题是。
②利用太阳能转化CO2的工艺如图所示。

I.反应1的反应类型是。
II.此工艺的最终产物是。
③科学家利用新型催化剂,将二氧化碳转化为甲醇(CH4O),反应的微观示意图如下。

I.上述四种物质中属于氧化物的是(填编号)。
II.反应中甲与乙的分子个数比为。
III.将8.8g二氧化碳完全转化,可生成甲醇mol,约含个甲醇分子。
19. 下表是KNO3在不同温度时的溶解度。温度(℃)
0
20
40
60
80
100
溶解度(g/100g水)
13.3
31.6
63.9
110
169
246
①20℃,KNO3的溶解度是。
②60℃时,KNO3的饱和溶液中溶质与溶剂的质量比为。
③将XgKNO3固体投入盛有100g水的烧杯中,搅拌、加热,测不同温度下烧杯中溶液的质量,如图所示。

I.a点溶液的溶质质量分数(只需列比例式)。
II.溶液一定处于饱和状态的点是(填字母编号)。
III.b点时的溶液质量比a点时多g。
IV.X的取值范围是。
三、综合题
-
20. 为探究氢气的化学性质,进行如下实验(浓硫酸具有吸水性)。

①装置A中对多孔塑料板的要求是。
②装置D处硬质玻璃管内反应的化学方程式是。
③能证明氢气具有还原性的实验现象是。
④能否省略装置E,说明理由。
⑤在不改变装置的条件下,用最简单的方法验证氢气具有可燃性。
⑥实验结束,关闭弹簧夹同时熄灭酒精灯,装置F中可能发生的反应是(任写其中一条化学方程式)。
21. 某纯碱样品中含有少量NaCl,为测定该样品中Na2CO3的质量分数,设计如下实验方案。(1)、(方案一)
①“操作”的名称是。
②加入“过量”CaCl2溶液的原因是。
③判断白色沉淀Y是纯净物的方法:取最后一次洗涤液,(填所用的试剂及实验现象)。
④纯碱样品中Na2CO3的质量分数是(精确到0.1%)。
(2)、(方案二)
⑤装置A中反应的化学方程式为。
⑥为了减少实验误差,理论上装置C中NaOH溶液必须过量。设计实验证明装置C中NaOH溶液可能存在的两种情况。
实验目的
实验方案
实验现象
证明NaOH溶液过量
取装置C中反应后的溶液于烧杯中,滴入
证明NaOH溶液的量不足
取装置D中反应后的固体于烧杯中,滴入