江苏省扬州市邗江区2021年中考化学二模试卷
试卷更新日期:2021-07-05 类型:中考模拟
一、单选题
-
1. 2022年北京和张家口联合举办冬奥会,为办成绿色奥运,下列措施不可行的是( )A、大力发展公共交通,提倡绿色出行 B、实施太阳能灯亮化,发展新型能源 C、大量燃放烟花鞭炮,增强奥运气氛 D、开展垃圾分类收集,积极回收利用2. 下列物质中,属于纯净物的是( )A、洁净的空气 B、水泥砂浆 C、液氮 D、红糖水3. 2020年12月17日,“嫦娥五号”探测器完成任务,安全返航。下列环节中主要涉及化学变化的是( )A、点火升空 B、钻土采样 C、展开国旗 D、密封样品4. 分类法是一种行之有效、简单易行的科学方法。从组成分类来看,KNO3 不属于( )A、化合物 B、氧化物 C、硝酸盐 D、钾盐5. 下列常见物质中,由原子直接构成的是( )A、水 B、氯化钠 C、汞 D、二氧化碳6. 一些食物的pH 如下,其中酸性最强的是( )A、菠菜:5.1~5.7 B、牛奶:6.3~6.6 C、玉米粥:6.8~8.0 D、鸡蛋清:7.6~8.07. 人们曾把氧气叫做“养气”,可见氧气的重要性。下列关于氧气性质的描述正确的是( )A、工业制氧气是利用了液氮、液氧的沸点不同 B、用向上排空气法收集氧气,其依据是氧气的密度小于空气的密度 C、氧气可使带火星的木条复燃,是因为氧气具有可燃性 D、物质跟氧气反应都要发光、放热8. 在校园的洗手间内应该粘贴的图标是( )A、
 B、
B、 C、
C、 D、
D、 9. 下列化学反应属于化合反应的是( )A、 B、 C、 D、10. 我国第一艘自主建造的航母“山东舰”在建造时用到了大量钛合金,工业制钛的反应为: ,则X的化学式为( )A、SO2 B、SO3 C、H2SO3 D、H2O11. 水是生产生活中不可缺少的物质,下列关于水的说法中正确的是( )A、明矾溶液可以区分硬水和软水 B、在自来水厂净化水的过程中,发生的变化都是物理变化 C、洗米后的水,可以用于浇花 D、为了节约用水,可以用工业废水直接浇灌农田12. 色氨酸(C11H12N2O2)是一种氨基酸,下列有关色氨酸的叙述正确的是( )A、C11H12N2O2 的相对分子质量为 204g B、色氨酸中碳、氢、氮、氧元素质量之比为 11:12:2:2 C、色氨酸中共有 27 个原子 D、色氨酸中氢元素的质量分数最小13. 化学式书写错误的是( )A、氧化铝—AlO B、氯化铁—FeCl3 C、硫酸铜—CuSO4 D、氢氧化钙—Ca(OH)214. 下列关于实验现象的描述正确的是( )A、红磷在氧气中燃烧发出耀眼的白光,并产生大量的白雾 B、细铁丝在氧气中燃烧火星四射,生成黑色固体四氧化三铁 C、打开浓盐酸的试剂瓶盖,一会儿瓶口会产生白烟 D、向淀粉溶液中滴加碘水,溶液变蓝15. 以甲为原料合成化工产品丁的微观过程如下图。下列说法正确的是( )
9. 下列化学反应属于化合反应的是( )A、 B、 C、 D、10. 我国第一艘自主建造的航母“山东舰”在建造时用到了大量钛合金,工业制钛的反应为: ,则X的化学式为( )A、SO2 B、SO3 C、H2SO3 D、H2O11. 水是生产生活中不可缺少的物质,下列关于水的说法中正确的是( )A、明矾溶液可以区分硬水和软水 B、在自来水厂净化水的过程中,发生的变化都是物理变化 C、洗米后的水,可以用于浇花 D、为了节约用水,可以用工业废水直接浇灌农田12. 色氨酸(C11H12N2O2)是一种氨基酸,下列有关色氨酸的叙述正确的是( )A、C11H12N2O2 的相对分子质量为 204g B、色氨酸中碳、氢、氮、氧元素质量之比为 11:12:2:2 C、色氨酸中共有 27 个原子 D、色氨酸中氢元素的质量分数最小13. 化学式书写错误的是( )A、氧化铝—AlO B、氯化铁—FeCl3 C、硫酸铜—CuSO4 D、氢氧化钙—Ca(OH)214. 下列关于实验现象的描述正确的是( )A、红磷在氧气中燃烧发出耀眼的白光,并产生大量的白雾 B、细铁丝在氧气中燃烧火星四射,生成黑色固体四氧化三铁 C、打开浓盐酸的试剂瓶盖,一会儿瓶口会产生白烟 D、向淀粉溶液中滴加碘水,溶液变蓝15. 以甲为原料合成化工产品丁的微观过程如下图。下列说法正确的是( ) A、乙、丁为氧化物 B、转化①中乙和丙的分子个数之比为1:1 C、甲中氢元素的质量分数小于丁 D、该过程体现无机物与有机物可相互转化16. 下列实验操作规范的是()A、
A、乙、丁为氧化物 B、转化①中乙和丙的分子个数之比为1:1 C、甲中氢元素的质量分数小于丁 D、该过程体现无机物与有机物可相互转化16. 下列实验操作规范的是()A、 量取液体
B、
量取液体
B、 引燃酒精灯
C、
引燃酒精灯
C、 滴加试剂
D、
滴加试剂
D、 稀浓硫酸
17. 下列说法正确的是( )A、酸碱中和反应生成盐和水,生成盐和水的反应一定是中和反应 B、向碳酸盐滴加稀盐酸,有气泡产生,滴加盐酸有气体生成一定是碳酸盐 C、墙内开花,墙外可以嗅到花香,说明分子在不断的运动 D、农作物生长需要 N,P,K 等元素,为增加肥效,可把 NH4H2PO4 与草木灰混合施用18. 下列物质的性质与用途均符合题意并相对应的是( )A、碳酸氢铵易分解,可用作化肥 B、钨的熔点高,用于制作灯泡里的灯丝 C、Ca(OH)2 微溶于水,可用于改良酸性土壤 D、氢氧化钠能够与酸反应,用于治疗胃酸过多
稀浓硫酸
17. 下列说法正确的是( )A、酸碱中和反应生成盐和水,生成盐和水的反应一定是中和反应 B、向碳酸盐滴加稀盐酸,有气泡产生,滴加盐酸有气体生成一定是碳酸盐 C、墙内开花,墙外可以嗅到花香,说明分子在不断的运动 D、农作物生长需要 N,P,K 等元素,为增加肥效,可把 NH4H2PO4 与草木灰混合施用18. 下列物质的性质与用途均符合题意并相对应的是( )A、碳酸氢铵易分解,可用作化肥 B、钨的熔点高,用于制作灯泡里的灯丝 C、Ca(OH)2 微溶于水,可用于改良酸性土壤 D、氢氧化钠能够与酸反应,用于治疗胃酸过多二、多选题
-
19. 将 30g 固体物质 X(不含结晶水)投入盛有 20g 水的烧杯中,搅拌,测得 0℃、t1℃、t2℃、t3℃时烧杯中溶液的质量分别如图中 A、B、C、D 点所示。根据图示判断下列说法正确的是( )
 A、0℃时,物质 X 的溶解度为 24g B、A,B 两点对应的溶液一定是饱和溶液 C、t1℃时,若向 B 点对应的烧杯中再加入 30g 水,搅拌, 所得溶液为不饱和溶液 D、C,D 点对应的溶液溶质质量分数相同20. 以氧化镁矿粉(主要成分氧化镁,还含有少量氧化铁等杂质)和浓硫酸为原料,生产MgSO4 的部分生产流程如图所示。分析制备过程,下列说法正确的是:( )
A、0℃时,物质 X 的溶解度为 24g B、A,B 两点对应的溶液一定是饱和溶液 C、t1℃时,若向 B 点对应的烧杯中再加入 30g 水,搅拌, 所得溶液为不饱和溶液 D、C,D 点对应的溶液溶质质量分数相同20. 以氧化镁矿粉(主要成分氧化镁,还含有少量氧化铁等杂质)和浓硫酸为原料,生产MgSO4 的部分生产流程如图所示。分析制备过程,下列说法正确的是:( ) A、图中,石墨配酸塔由石墨制成,利用了石墨的导电性 B、混合器中,发生反应的其中一个化学方程式为 C、回转化成室中发生的化学反应会放出热量 D、生产过程无废物排放,符合绿色化学要求,其中可循环利用的物质只有水
A、图中,石墨配酸塔由石墨制成,利用了石墨的导电性 B、混合器中,发生反应的其中一个化学方程式为 C、回转化成室中发生的化学反应会放出热量 D、生产过程无废物排放,符合绿色化学要求,其中可循环利用的物质只有水三、填空题
-
21. 2021 年扬州世界园艺博览会以“绿色城市、健康生活”为主题。(1)、世园会采用很多碳化木。木材的主要成分是纤维素 (C6H10O5)n,纤维素由 种元素组成,其中碳元素的质量分数为(精确到 0.1%)。(2)、世博园区内使用电动车,有效减少了大气污染物的排放,其中会导致酸雨的气体是(填一种化学式即可)。(3)、“康康”和“乐乐”是世园会的吉祥物玩偶,表面为羊毛,填充物为聚酯纤维,鉴别二者的方法为 。聚酯纤维属于(填字母)。
a 无机材料 b 合成材料 c 复合材料
(4)、世博园区内用“活性炭+超滤膜+紫外线”组合工艺获得直饮水。其中用紫外线代替氯气对水进行处理,其作用是 , 该净化工艺流程( “能”或“不能”) 降低水的硬度。我们每个人都要爱护水资源。(5)、园博会栽种了很多花草树木,绿色植物通过光合作用将和水转化为氧气,让园区变成大氧吧,同时将能转化为化学能。园艺种植经常施用一种复合肥料。A、NH4HCO3B、KCl C、KNO3
(6)、游客携带了自热米饭进行了简单的午餐,自热米饭中加热包中含有生石灰,使用时打开包装加水即可使用。其反应原理的化学方程式是 , 该反应(填“放热”或“吸热”)。22. 2021 年 4 月 29 日,中国首个空间站核心舱“天和”发射成功。(1)、太空服除了要隔热、散热外,还要有通讯系统、动力系统、输送养料系统和废气处理系统。其中废气处理包括两个步骤:第一步:将废气通过装有活性炭的盒子除去臭气,这一过程利用了活性炭的。
第二步:再用氢氧化锂(LiOH)作吸收剂除去二氧化碳(氢氧化锂和氢氧化钠都是碱, 具有相似的化学性质),写出该反应的化学反应方程式。
(2)、宇航员易骨质疏松,是由于航天飞行会导致宇航员体内流失。平常饮食中可添加豆制品加强营养,豆腐中含有人们生活所需的各类营养素,每 100 g豆腐中含各种营养成分如表:成分
X
蛋白质
油脂
糖类
钙
磷
铁
维生素B1
维生素B2
质量
89.3
4.7
1.3
2.8
0.24
0.064
0.014
0.00006
0.00003
①其中 X 代表六大营养素中的。
②钙、磷、铁元素中属于人体必需微量元素的是(填元素符号)。
③蛋白质、油脂和葡萄糖中属于有机高分子化合物的是。
④成年人若食用了 500g 豆腐,相当于补充了g 的钙元素。
(3)、航天飞行器座舱内空气更新过程如图所示:
①装置Ⅱ是 CO2和 H2的反应装置,该反应的化学方程式为。装置Ⅱ消耗 99g CO2 , 生时成水 H2Og。
②从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是 CO2和 H2O,若产生 96g O2 , 消耗 99g CO2 , 则同时消耗 H2Og。
23. 如图所示为实验室常用的实验装置。据图回答下列问题:
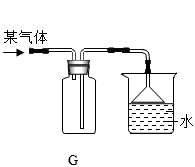 (1)、写出图中①②的仪器名称:① ②。(2)、实验室用氯酸钾制取氧气的化学方程式为 , 应 选 择 的 发生和收集装置是(填字母序号)。(3)、若用装置 B 作为实验室锌和稀硫酸制取氢气的发生装置,写出该反应的化学方程式。装置 B 相对于装置 C 的优点是 , 夹 紧 弹 簧夹后,液面应最终位于(填“1”、“2”或“3”)处。(4)、实验室常用氯化铵与熟石灰固体共热来制取氨气,装置G 可以用来收集氨气,还可以防倒吸。请你推测该氨气的密度(填“大于”或“小于”)空气的密度, 该气体在水中的溶解性是(填“极易溶”或“难溶”)。24. 立德粉(ZnS 和 BaSO4)是一种常用白色颜料。以重晶石(BaSO4)为原料生产立德粉的主要工艺流程如图:
(1)、写出图中①②的仪器名称:① ②。(2)、实验室用氯酸钾制取氧气的化学方程式为 , 应 选 择 的 发生和收集装置是(填字母序号)。(3)、若用装置 B 作为实验室锌和稀硫酸制取氢气的发生装置,写出该反应的化学方程式。装置 B 相对于装置 C 的优点是 , 夹 紧 弹 簧夹后,液面应最终位于(填“1”、“2”或“3”)处。(4)、实验室常用氯化铵与熟石灰固体共热来制取氨气,装置G 可以用来收集氨气,还可以防倒吸。请你推测该氨气的密度(填“大于”或“小于”)空气的密度, 该气体在水中的溶解性是(填“极易溶”或“难溶”)。24. 立德粉(ZnS 和 BaSO4)是一种常用白色颜料。以重晶石(BaSO4)为原料生产立德粉的主要工艺流程如图:
资料:BaS 可溶于水,ZnS 和 BaSO4均难溶于水。
(1)、原料进入回转炉之前先进行粉碎的目的 , 焦炭需过量,其目的是:①;②。(2)、回转炉中,重晶石(BaSO4)与焦炭在高温下焙烧制得 BaS,同时还生成一种可燃性气体,该反应的化学方程式是 , 这个反应中,化合价发生变化的元素有。(3)、上述流程中,主要用于分离、提纯的设备有、过滤器和洗涤槽。(4)、反应器中发生的复分解反应化学方程式是。25. 以菱锌矿(主要成分是 ZnCO3 , 杂质为 Fe2O3、FeO、CuO)为原料制备七水硫酸锌(ZnSO4•7H2O),同时得到铁红副产品,其工艺流程如图,回答下列问题: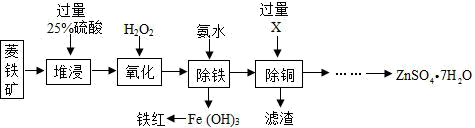 (1)、若实验室用质量分数为 98%的硫酸配制 200g 质量分数为 24.5%的稀硫酸,需要水(密度1g/mL)的体积为mL,需要用到的玻璃仪器有胶头滴管、玻璃棒、烧杯和 。(2)、物质 X 是 确定除铜完成的实验现象是。(3)、“氧化”中加入 H2O2的目的是在硫酸的作用下将溶液中的 FeSO4转化成 Fe2(SO4)3 , 反应的化学方程式:。(4)、除铁过程中,反应温度、溶液 pH 对除铁效果均有影响,为探究除铁的最佳效果,某同学做了以下的实验并记录了相关数据,请回答问题:
(1)、若实验室用质量分数为 98%的硫酸配制 200g 质量分数为 24.5%的稀硫酸,需要水(密度1g/mL)的体积为mL,需要用到的玻璃仪器有胶头滴管、玻璃棒、烧杯和 。(2)、物质 X 是 确定除铜完成的实验现象是。(3)、“氧化”中加入 H2O2的目的是在硫酸的作用下将溶液中的 FeSO4转化成 Fe2(SO4)3 , 反应的化学方程式:。(4)、除铁过程中,反应温度、溶液 pH 对除铁效果均有影响,为探究除铁的最佳效果,某同学做了以下的实验并记录了相关数据,请回答问题:编号
反应温度/℃
溶液 pH
除铁率/%
a
30
2
91.5
b
30
2.5
93.3
c
40
2.5
95.1
d
40
3.1
Y
e
50
3.1
99.5
①实验对比,得到的结论为其他条件不变时,反应温度增大,除铁率提高。
②实验 a 和实验 b 对比,得到结论是。
③最佳的除铁条件为反应温度℃,溶液 pH。
(5)、流程中获得七水硫酸锌前省略的操作是 、冷却结晶、过滤、洗涤和低温烘干;洗涤经常选用 95%的乙醇,优点是(填一个答案);烘干操作需在低温条件下进行,其原因是。(6)、取 28.70g ZnSO4•7H2O 加热至不同温度,剩余固体的质量变化如图所示。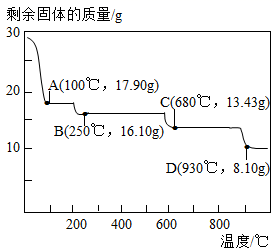
ZnSO4•7H2O 加热到 100℃时所得固体的化学式为是(写出计算过程)。