江苏省常州市金坛区2021年中考化学二模试卷
试卷更新日期:2021-07-05 类型:中考模拟
一、单选题
-
1. 下列现象属于化学变化的是( )A、沙尘飞扬 B、光合作用 C、电灯发光 D、冰雪消融2. 空气中下列气体的体积分数最大的是( )A、氮气 B、氧气 C、二氧化碳 D、稀有气体3. 下列各组物质的名称、俗名对应一致的是( )A、氧化钙(熟石灰) B、碳酸钠(小苏打) C、汞(水银) D、氢氧化钠(纯碱)4. 人体缺少钙元素会引起( )A、大脖子病 B、侏儒症 C、贫血 D、骨骼疏松5. 2021年3月,在四川三星堆遗址,发掘出一张独特的金面具。距今三四千年,仍能保存完好,体现了黄金具有的性质是( )A、熔点高 B、延展性好 C、金属光泽 D、耐腐蚀6. 今年世界地球日的主题是“修复我们的地球”,我国也将“碳达峰”、“碳中和”纳入生态文明建设整体布局。以下做法不利于降低空气中二氧化碳含量的是( )A、夏天尽可能将空调温度调到最低 B、发展新能源汽车产业 C、交通出行选择公共自行车 D、植树造林7. 下列物质可用作复合肥的是( )A、CO(NH2)2 B、NH4H2PO4 C、K2CO3 D、Ca3(PO4)28. 下列关于化学史的叙述正确的是( )A、拉瓦锡发表了元素周期表 B、侯德榜发明了联合制碱法 C、诺贝尔发现了钋和镭 D、波义耳发现了质量守恒定律9. 以下各类物质中一定含有氧元素的是( )A、酸 B、碱 C、有机物 D、盐10. 下列关于实验现象的描述,正确的是( )A、镁条在空气中燃烧,发出耀眼的白光,生成氧化镁 B、硫在氧气中燃烧,产生黄色火焰 C、铁锈和稀盐酸反应,溶液由无色变为浅绿色 D、铝箔在空气中加热,熔化而不滴落,冷却后表面光泽变暗淡11. 下列实验都用到了水,其中水的作用和另外三个实验不同的是( )A、检查气密性
 B、测定空气中氧气的含量
B、测定空气中氧气的含量  C、收集气体
C、收集气体  D、铁丝燃烧
D、铁丝燃烧  12. 灭活疫苗是指先对病毒或细菌进行培养,然后用化学方法使其蛋白质失去生理活性。以下物质或措施不能使蛋白质“灭活”的是( )A、加热 B、乙酸铅溶液 C、生理盐水 D、甲醛13. 碳酸乙烯酯( )可用作锂电池电解液,下列有关碳酸乙烯酯的说法正确的是( )A、碳酸乙烯酯是有机高分子化合物 B、碳元素和氧元素的质量比为1:1 C、一个碳酸乙烯酯分子中有2个氢分子 D、碳酸乙烯酯中氢元素质量分数约为4.5%14. 为了达到相应的实验目的,下列实验设计不合理的是( )A、
12. 灭活疫苗是指先对病毒或细菌进行培养,然后用化学方法使其蛋白质失去生理活性。以下物质或措施不能使蛋白质“灭活”的是( )A、加热 B、乙酸铅溶液 C、生理盐水 D、甲醛13. 碳酸乙烯酯( )可用作锂电池电解液,下列有关碳酸乙烯酯的说法正确的是( )A、碳酸乙烯酯是有机高分子化合物 B、碳元素和氧元素的质量比为1:1 C、一个碳酸乙烯酯分子中有2个氢分子 D、碳酸乙烯酯中氢元素质量分数约为4.5%14. 为了达到相应的实验目的,下列实验设计不合理的是( )A、 分离H2O2和MnO2制O2后的固液混合物
B、
分离H2O2和MnO2制O2后的固液混合物
B、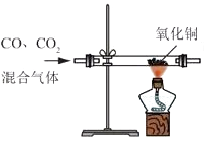 除去CO中的CO2气体
C、
除去CO中的CO2气体
C、 区分NaCl、NH4NO3、NaOH三种固体
D、
区分NaCl、NH4NO3、NaOH三种固体
D、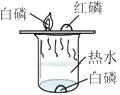 探究可燃物燃烧的条件
15. 下列是某无色溶液中可能大量存在的溶质,合理的是( )A、NaCl Ca(NO3)2 NaOH B、FeSO4 MgSO4 H2SO4 C、HCl NaHCO3 NaCl D、CaCl2 K2CO3 KNO316. ABC三种固体物质在水中的溶解度曲线如下图所示,下列说法中正确的是( )
探究可燃物燃烧的条件
15. 下列是某无色溶液中可能大量存在的溶质,合理的是( )A、NaCl Ca(NO3)2 NaOH B、FeSO4 MgSO4 H2SO4 C、HCl NaHCO3 NaCl D、CaCl2 K2CO3 KNO316. ABC三种固体物质在水中的溶解度曲线如下图所示,下列说法中正确的是( ) A、t1℃时,8gA加入50g水中,得到不饱和溶液 B、t3℃时,恰好完全溶解等质量的ABC三种物质,需要加水的质量A>B>C C、将t3℃时ABC的饱和溶液降温至t2℃,所得溶液中C的溶质质量分数最小 D、A中混有少量B,可以采用蒸发结晶的方法提纯A17. 在给定条件下,下列各组物质通过一步转化能实现的是( )A、 B、 C、 D、18. 下列除杂方法正确的是( )
A、t1℃时,8gA加入50g水中,得到不饱和溶液 B、t3℃时,恰好完全溶解等质量的ABC三种物质,需要加水的质量A>B>C C、将t3℃时ABC的饱和溶液降温至t2℃,所得溶液中C的溶质质量分数最小 D、A中混有少量B,可以采用蒸发结晶的方法提纯A17. 在给定条件下,下列各组物质通过一步转化能实现的是( )A、 B、 C、 D、18. 下列除杂方法正确的是( )选项
物质(括号内为杂质)
除杂方法
A
H2(HCl)
依次通过饱和碳酸氢钠溶液和浓硫酸
B
CaO(CaCO3)
高温煅烧
C
NaOH溶液(Na2CO3)
加足量稀盐酸
D
NaCl溶液(MgCl2)
加适量氢氧化钾溶液,充分反应后过滤
A、A B、B C、C D、D19. A-E为初中化学常见物质,分别属于单质、氧化物、酸、碱、盐中的一种,其中有一种物质的溶液为蓝色。它们之间存在如下图所示的反应和转化关系,“一”表示两种物质之间能发生反应,“→”表示能一步转化,所涉及的均为初中化学常见反应,下列说法错误的是( ) A、图中所涉及的反应同时包含了四种基本反应类型 B、若A溶液为蓝色,则E可能是一种白色固体 C、若B溶液为蓝色,则E可能是一种无色无味的气体 D、C和D的溶液不可能是蓝色20. 酒精(C2H5OH)的水溶液常用来消毒,现有某种酒精的水溶液,经测定溶液中氢元素的质量分数为12%,则该溶液中酒精的质量分数为( )A、75% B、92% C、23% D、46%
A、图中所涉及的反应同时包含了四种基本反应类型 B、若A溶液为蓝色,则E可能是一种白色固体 C、若B溶液为蓝色,则E可能是一种无色无味的气体 D、C和D的溶液不可能是蓝色20. 酒精(C2H5OH)的水溶液常用来消毒,现有某种酒精的水溶液,经测定溶液中氢元素的质量分数为12%,则该溶液中酒精的质量分数为( )A、75% B、92% C、23% D、46%二、填空题
-
21. 选择H、O、Ca、S、Cl五种元素,写出符合下列要求的化学式。(1)、胃液的中含有的酸;(2)、用于改良酸性土壤的碱;(3)、电解水时负极产生的气体;(4)、能使高锰酸钾溶液褪色的气体。22. 选择合适的序号填空。
①干馏 ②分馏 ③氧化 ④乳化 ⑤挥发 ⑥催化
(1)、沾有水的铁器在空气中因而生锈。(2)、石油经过 , 可以得到汽油、煤油、航空煤油和柴油等。(3)、洗洁精洗油污属于现象。(4)、在双氧水制氧气的反应中,二氧化锰起作用。23. 图1是某反应的微观示意图,请回答下列问题。 (1)、该反应属于反应(填一种基本反应类型)。(2)、
(1)、该反应属于反应(填一种基本反应类型)。(2)、 属于(选填“单质”、“氧化物”或“有机物”),该物质是由(选填“分子”、“原子”、“离子”)直接构成。 (3)、参加反应的
属于(选填“单质”、“氧化物”或“有机物”),该物质是由(选填“分子”、“原子”、“离子”)直接构成。 (3)、参加反应的 和
和  的质量比为(最简整数比)。 (4)、空气中
的质量比为(最简整数比)。 (4)、空气中 的来源是(答一种即可)。 24. 爱劳动是美德。小宁同学在家帮妈妈烧粥时,发现了许多与化学有关的知识,请根据信息回答下列问题。
的来源是(答一种即可)。 24. 爱劳动是美德。小宁同学在家帮妈妈烧粥时,发现了许多与化学有关的知识,请根据信息回答下列问题。 (1)、烧粥用的钢由不锈钢制成,不锈钢属于___________材料。A、合成 B、复合 C、无机非金属 D、金属(2)、小宁家使用的是天然气(主要成分为甲烷),属于(选填“可再生”或“不可再生”)能源,刚点火加热时,发现锅的底部有一些小水珠产生,请用化学方程式表示产生该现象的原因。加热一段时间后,小水珠消失了,请用微粒的观点解释该现象。(3)、为检验粥汤中含有的淀粉,可以取样后向其中滴入。(4)、关闭燃气灶阀门,火焰立即熄灭,此方法的灭火原理是。25. 某实验员用硫酸、氢氧化钠、氧化铜为原料,制备氢氧化铜。请回答相关问题。(1)、Ⅰ.配制稀硫酸
(1)、烧粥用的钢由不锈钢制成,不锈钢属于___________材料。A、合成 B、复合 C、无机非金属 D、金属(2)、小宁家使用的是天然气(主要成分为甲烷),属于(选填“可再生”或“不可再生”)能源,刚点火加热时,发现锅的底部有一些小水珠产生,请用化学方程式表示产生该现象的原因。加热一段时间后,小水珠消失了,请用微粒的观点解释该现象。(3)、为检验粥汤中含有的淀粉,可以取样后向其中滴入。(4)、关闭燃气灶阀门,火焰立即熄灭,此方法的灭火原理是。25. 某实验员用硫酸、氢氧化钠、氧化铜为原料,制备氢氧化铜。请回答相关问题。(1)、Ⅰ.配制稀硫酸H2SO4中,硫元素的化合价为。
(2)、欲配制溶质质量分数为10%的稀硫酸490g,需溶质质量分数为98%的浓硫酸g。(3)、以下操作,会导致配制的稀硫酸溶质质量分数偏高的是(填序号)。①用量筒量取浓硫酸时仰视刻度
②稀释后,用水冲洗搅拌的玻璃棒,并将洗涤液并入稀释后的硫酸
③将配置好的稀硫酸转移至细口瓶时,有少许液体洒出
(4)、Ⅱ.制备氢氧化铜向氧化铜粉末中加入一定量的稀硫酸,待固体完全消失后,再缓缓滴加氢氧化钠溶液,获得沉淀质量随氢氧化钠质量的变化关系如图所示。

a点所得溶液的pH7(选填>、<=)。
(5)、b点所得溶液中含有的溶质是(填化学式)。(6)、将最终所得混合物(填写一种操作)、洗涤、低温烘干,得到氢氧化铜固体。三、综合题
-
26. 图(A-E)是初中化学制备气体常用的实验装置。
 (1)、仪器a的名称是。(2)、写出加热硫酸铵和氢氧化钙固体混合物制取氨气的化学方程式 , 已知氨气极易溶于水,密度小于空气,则用此法制氨气的发生和收集装置的组合为(填字母)。(3)、某化学学习小组利用图装置,研究二氧化碳制备与性质实验,大号塑料瓶内壁两边,分别贴一张干燥的蓝色石蕊试纸和湿润的蓝色石蕊试纸。
(1)、仪器a的名称是。(2)、写出加热硫酸铵和氢氧化钙固体混合物制取氨气的化学方程式 , 已知氨气极易溶于水,密度小于空气,则用此法制氨气的发生和收集装置的组合为(填字母)。(3)、某化学学习小组利用图装置,研究二氧化碳制备与性质实验,大号塑料瓶内壁两边,分别贴一张干燥的蓝色石蕊试纸和湿润的蓝色石蕊试纸。
①装有石灰石的塑料瓶底部用剪刀戳了一些小孔,则此发生装置的优点是。
②打开K1、K2、K3 , 关闭K4 , 可以看到(选填“高”或“低”)的蜡烛先熄灭。
③打开K1、K4 , 关闭K2、K3 , 一段时间后,大号塑料瓶中出现的现象是 , 小号塑料瓶中发生反应的化学方程式为。
④该大号塑料瓶的容积为2.2L,若需将其充满二氧化碳(密度为2g/L),至少需要含碳酸钙80%的石灰石多少g?(根据化学方程式计算,写出计算过程)
27. 小华同学利用图装置,探究碳和氧化铁的反应,请回答下列问题。 (1)、请简述实验前检查该装置气密性的操作和现象。(2)、气球的作用是;与使用普通导管相比,球形导管上的球体部分所起作用是。(3)、小华采用对比实验的方式,研究不同形态的碳和氧化铁的反应,并用一氧化碳传感器测得试管内一氧化碳含量如图所示。
(1)、请简述实验前检查该装置气密性的操作和现象。(2)、气球的作用是;与使用普通导管相比,球形导管上的球体部分所起作用是。(3)、小华采用对比实验的方式,研究不同形态的碳和氧化铁的反应,并用一氧化碳传感器测得试管内一氧化碳含量如图所示。

①实验进行时试管内发生的化学反应是(写出化学方程式)。
②小华认为选择活性炭和氧化铁反应更适合,他的理由是。
③通过对图两幅图像的分析,90秒至300秒之间一氧化碳含量变化趋势明显不同的主要原因可能是。
28. 粉煤灰的主要成分是Al2O3和SiO2 , 还含有少量的Fe2O3、FeO,以粉煤灰为原料制备铝的流程如图所示。
资料卡:①SiO2既不溶于水,也不溶于常见的酸。
②“沉淀”时,通入CO2是为了调节提纯液的pH。
(1)、“酸浸”后,所得溶液中含有种阳离子,“滤渣”的主要成分是。(2)、写出“提纯”步骤中生成Fe(OH)3沉淀的化学方程式。(3)、下列关于流程的说法正确的是___________(填字母)。A、相比于块状矿石,粉煤灰和酸反应的速率更快 B、“氧化”时不宜温度太高,以防双氧水受热分解 C、“灼烧”过程中,固体中氧元素的质量分数在逐渐升高,到某一数值后保持恒定 D、“电解”时,能量的转化形式是由电能转化为化学能(4)、仅根据流程图推测,Al(OH)3可溶于溶液。29. 某种碱式碳酸锌是制备功能材料氧化锌的原料,其化学式可以表示为Znx(OH)y(CO3)z , 受热分解后会生成氧化锌固体和另外两种气体。某化学探究小组设计了图所示装置(虚线框中的装置未画出),对碱式碳酸锌进行探究。
资料卡:①碱石灰是氢氧化钠固体和生石灰的混合物。
②无水硫酸铜是白色固体,遇水变蓝。
(1)、Ⅰ定性探究:碱式碳酸锌受热分解后产生的气体成分(猜想假设)1.H2O; 2.CO2; 3.NH3
其中猜想3明显不合理,理由是。
(2)、(实验探究)检查完气密性后,装药品,在虚线框A、B中依次选择、(选填①、②、③,每个虚线框仅选一个),加热后观察现象。(实验结论)通过上述实验现象得知,碱式碳酸锌受热分解后有水和二氧化碳生成。
(3)、Ⅱ.定量探究:碱式碳酸锌的组成
重新组装仪器,虚线框A处是换装了浓硫酸的装置①,浓硫酸的作用是;在虚线框B处是连续的2个装置②。
(4)、加热前先通入N2排尽装置内的空气,防止空气中的影响实验的精确性;再关闭止水夹,停止通入氮气,对碱式碳酸锌加热实验过程中可根据的现象判断碱式碳酸锌样品已完全分解;待样品完全分解后,打开止水夹,需要继续通一会N2 , 目的是。(5)、取一定量碱式碳酸锌样品(不含杂质),置于热分解装置内,完全反应后测得A处增重3.6g,B处先通过的碱石灰增重4.4g。则x:y:z的最简整数比为。