安徽省合肥市肥东县2021年中考化学二模试卷
试卷更新日期:2021-07-05 类型:中考模拟
一、单选题
-
1. 下图所示活动体现了我国古代劳动人民的勤劳和智慧。其中涉及化学变化的是( )A、
 织布
B、
织布
B、 耕田
C、
耕田
C、 生火
D、
生火
D、 灌溉
2. 每年的6月5日是“世界环境日”。“山更绿,水更清,空气更清新”是我们共同的愿望。下列做法与这种愿望不符的是( )A、火力发电厂进行脱硫、控尘处理 B、工厂废气直接排放到空气中 C、出行尽量步行、骑自行车或乘坐公交车,减少使用私家车 D、开发使用太阳能等清洁能源3. 饺子是中国人餐桌上的传统美食,下列食材中富含糖类的是( )A、芹菜 B、面粉 C、麻油 D、瘦肉4. 冬季天气寒冷,流感多发,奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播。下列对奥司他韦的说法正确的是( )A、奥司他韦由碳、氢、氮、氧四种原子构成 B、一个奥司他韦分子中含有一个氮分子 C、奥司他韦中氢元素和氮元素的质量分数相等 D、奥司他韦中C,H,N,O元素的质量比为16:28:2:45. 下列物质的名称、俗名、化学式、分类均正确的一组是( )A、汞 水银 单质 B、碳酸氢钠 小苏打 ,盐 C、氧化钙 熟石灰 氧化物 D、氢氧化钠 纯碱 碱6. 化学离不开实验,下列实验操作正确的是( )A、
灌溉
2. 每年的6月5日是“世界环境日”。“山更绿,水更清,空气更清新”是我们共同的愿望。下列做法与这种愿望不符的是( )A、火力发电厂进行脱硫、控尘处理 B、工厂废气直接排放到空气中 C、出行尽量步行、骑自行车或乘坐公交车,减少使用私家车 D、开发使用太阳能等清洁能源3. 饺子是中国人餐桌上的传统美食,下列食材中富含糖类的是( )A、芹菜 B、面粉 C、麻油 D、瘦肉4. 冬季天气寒冷,流感多发,奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播。下列对奥司他韦的说法正确的是( )A、奥司他韦由碳、氢、氮、氧四种原子构成 B、一个奥司他韦分子中含有一个氮分子 C、奥司他韦中氢元素和氮元素的质量分数相等 D、奥司他韦中C,H,N,O元素的质量比为16:28:2:45. 下列物质的名称、俗名、化学式、分类均正确的一组是( )A、汞 水银 单质 B、碳酸氢钠 小苏打 ,盐 C、氧化钙 熟石灰 氧化物 D、氢氧化钠 纯碱 碱6. 化学离不开实验,下列实验操作正确的是( )A、 蒸发
B、
蒸发
B、 检查装置气密性
C、
检查装置气密性
C、 稀释浓硫酸
D、
稀释浓硫酸
D、 细铁丝在氧气中燃烧
7. 我国的稀土储量居世界第一位。稀土金属广泛应用在冶金、石油化工、材料工业等领域。钕(Nd)是一种制造导弹的稀土元素,钕元素在元素周期表中的信息如图所示。下列有关说法错误的是( )
细铁丝在氧气中燃烧
7. 我国的稀土储量居世界第一位。稀土金属广泛应用在冶金、石油化工、材料工业等领域。钕(Nd)是一种制造导弹的稀土元素,钕元素在元素周期表中的信息如图所示。下列有关说法错误的是( )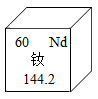 A、钕属于金属元素 B、钕原子中的质子数是60 C、钕原子的核外电子数是60 D、钕的相对原子质量是144.2 g8. 推理是化学学习中常用的思维方法,下列推理正确的是( )A、溶液是均一稳定的混合物,碘酒均一稳定且是混合物,碘酒属于溶液 B、氧化钙、氢氧化钠都具有吸水性,故它们都能用来干燥二氧化碳气体 C、氯化钠、硫酸铜等盐中都含有金属元素,所以盐中一定都含有金属元素 D、碱溶液能使无色酚酞溶液变红,所以使无色酚酞溶液变红的溶液一定是碱的溶液9. 如图是某化学反应前后的微观模型图,下列说法正确的是( )
A、钕属于金属元素 B、钕原子中的质子数是60 C、钕原子的核外电子数是60 D、钕的相对原子质量是144.2 g8. 推理是化学学习中常用的思维方法,下列推理正确的是( )A、溶液是均一稳定的混合物,碘酒均一稳定且是混合物,碘酒属于溶液 B、氧化钙、氢氧化钠都具有吸水性,故它们都能用来干燥二氧化碳气体 C、氯化钠、硫酸铜等盐中都含有金属元素,所以盐中一定都含有金属元素 D、碱溶液能使无色酚酞溶液变红,所以使无色酚酞溶液变红的溶液一定是碱的溶液9. 如图是某化学反应前后的微观模型图,下列说法正确的是( ) A、该反应是分解反应 B、该反应中生成物分子的个数比为1:1 C、该反应前后各元素的化合价都没有发生变化 D、该反应中反应物的质量比为17:2410. 下列实验方案不能达到相应实验目的是( )
A、该反应是分解反应 B、该反应中生成物分子的个数比为1:1 C、该反应前后各元素的化合价都没有发生变化 D、该反应中反应物的质量比为17:2410. 下列实验方案不能达到相应实验目的是( )选项
实验目的
实验方案
A
检验甲烷中是否含有氢元素
点燃,在火焰上方罩一干冷的烧杯,观察现象
B
鉴别O2和CO2
依次通入澄清石灰水
C
比较Fe、Cu、Ag的金属活动性
铁丝分别浸入CuSO4溶液和AgNO3溶液中
D
区分棉线和人造纤维
分别灼烧,用手揉捏燃烧后的产物
A、A B、B C、C D、D11. 小明同学用已配好的溶质质量分数为6%的氯化钠溶液,配制50g溶质质量分数为3%的氯化钠溶液,有关说法正确的是( )A、用100mL量筒量取所需水的体积 B、配制过程中不需要用托盘天平 C、用量筒量取水时俯视读数,所得溶液的落质质量分数小于3% D、将配好的溶液装入试剂瓶中时有少量溅出,所得溶液的溶质质量分数小于3%12. 用型玻璃管进行微型实验,如图所示,下列错误的是( ) A、a处的反应方程式为 B、a处红棕色粉末变为黑色 C、b处澄清石灰水变浑浊证明有CO2生成 D、可利用点燃的方法进行尾气处理
A、a处的反应方程式为 B、a处红棕色粉末变为黑色 C、b处澄清石灰水变浑浊证明有CO2生成 D、可利用点燃的方法进行尾气处理二、填空题
-
13. 在新冠肺炎疫情防控期间,人们广泛使用医用口罩和消毒液进行防护。
 (1)、口罩的防护原理与化学中的(填实验操作名称)相似。(2)、“84”消毒液的消毒原理是 ,生成的HClO具有杀菌作用。化学方程式中X的化学式为 , HClO中氯元素的化合价为。14. 实验室常用下列装置制取气体,请你根据所学知识回答有关问题。
(1)、口罩的防护原理与化学中的(填实验操作名称)相似。(2)、“84”消毒液的消毒原理是 ,生成的HClO具有杀菌作用。化学方程式中X的化学式为 , HClO中氯元素的化合价为。14. 实验室常用下列装置制取气体,请你根据所学知识回答有关问题。
 (1)、写出图中标有序号②的仪器名称:。(2)、实验室用装置A来制取氧气,但装置A有明显不正确,若按该装置操作的后果是。(3)、实验室常用装置B来制取较纯净的氧气,其反应的化学方程式为 , 收集装置选。实验室选用装置B或装置C还可以制取CO2 , 其反应药品是(填名称),与装置B相比,装置C的一个突出优点是。
(1)、写出图中标有序号②的仪器名称:。(2)、实验室用装置A来制取氧气,但装置A有明显不正确,若按该装置操作的后果是。(3)、实验室常用装置B来制取较纯净的氧气,其反应的化学方程式为 , 收集装置选。实验室选用装置B或装置C还可以制取CO2 , 其反应药品是(填名称),与装置B相比,装置C的一个突出优点是。三、综合题
-
15. 为了从某废旧电子产品中提炼贵重金属,得到硫酸铜溶液。小军所在的学习小组设计了如下流程:
 (1)、废旧电子产品属于(填“厨余垃圾”或“可回收物”或“有害垃圾”)。(2)、②中发生反应的基本类型为 , 滤液中存在的金属阳离子有、(填离子符号)。(3)、滤渣Ⅱ中的贵重金属为。(4)、写出④中发生反应的化学方程式。16. 化学兴趣小组用如下装置,进行有关碳及其氧化物的实验(图中夹持仪器已略去)在完成气密性检查后加入药品,并已设法在玻璃管及试管中充满二氧化碳。
(1)、废旧电子产品属于(填“厨余垃圾”或“可回收物”或“有害垃圾”)。(2)、②中发生反应的基本类型为 , 滤液中存在的金属阳离子有、(填离子符号)。(3)、滤渣Ⅱ中的贵重金属为。(4)、写出④中发生反应的化学方程式。16. 化学兴趣小组用如下装置,进行有关碳及其氧化物的实验(图中夹持仪器已略去)在完成气密性检查后加入药品,并已设法在玻璃管及试管中充满二氧化碳。 (1)、完成实验,填好表格
(1)、完成实验,填好表格实验步骤
实验现象
实验分析
缓缓通入CO2 , 点燃A处酒精喷灯加热一段时间。
木炭粉减少,D中有气泡、石灰水变浑浊且D中石灰水进入E中
A中发生反应的化学方程式
为
点燃B处酒精灯加热一段时间。
B处玻璃管内固体变红
说明一氧化碳具有
(2)、C装置的作用是。(3)、小明同学又将木炭与氧化铜混合加热得到红色固体,为弄清这种红色固体的成分,进行了如下的探究:(查阅资料)Cu和Cu2O均为红色固体,且
(提出猜想)红色固体是:Ⅰ.Cu Ⅱ.Cu2O Ⅲ.。
(4)、(进行实验)操作
现象
结论
取灼烧后的红色固体2.88g于试管中,加入足量稀硫酸充分反应
红色固体一定有Cu2O
(5)、(思考与分析)小林同学认为猜想Ⅱ正确,同学们分析后认为他的结论不准确,理由是 , 要得出正确结论,还需要测定的数据是 , 若用a表示该数据,则a的取值范围为 , 可以得出猜想Ⅲ正确。四、计算题
-
17. 我国著名的化学家侯德榜发明了联合制碱法,大大提高了原料的利用率,其反应原理之一为 ,某化工厂消耗117t氯化钠,理论上可生产碳酸氢钠的质量是多少?(注:在20℃时,将二氧化碳通入含NH3的饱和NaCl溶液中能生成 NaHCO3晶体和NH4Cl溶液)