安徽省池州市贵池区2021年中考化学二模试卷
试卷更新日期:2021-07-05 类型:中考模拟
一、单选题
-
1. 庆祝新中国70华诞,2019年10月1日,举行盛大阅兵仪式。阅兵过程中,下列一定发生化学变化的是( )A、
 三军将士昂首阔步
B、
三军将士昂首阔步
B、 放飞7万只气球
C、
放飞7万只气球
C、 56门礼炮齐鸣
D、
56门礼炮齐鸣
D、 飞机拉出的彩烟
2. “有山有水、依山伴水、显山露水”是重庆独特的魅力。下列关于水的说法错误的是( )A、水是一种化学资源 B、电解水是验证水的组成的方法之一 C、水分子保持水的化学性质 D、在固态时水分子是静止不动的3. 2020年3月,四川凉山木里县突发森林火灾,下列说法错误的是( )A、森林地表腐质层的可燃性气体在雷击作用下达到着火点而燃烧,引发森林火灾 B、出动直升机开展吊桶投水扑灭山火,主要目的是降低可燃物的着火点 C、森林大火不易扑灭是因为山势陡峭,树林茂密,难以通过砍伐树木形成隔离带 D、消防人员灭火时要防止被森林大火灼烧,并戴好防护面罩避免吸入有害物质4. 小明同学依据描述书写的化学符号:①两个氮分子:2N2;②由三个氧原子构成的臭氧分子:3O;③粒子结构示意图
飞机拉出的彩烟
2. “有山有水、依山伴水、显山露水”是重庆独特的魅力。下列关于水的说法错误的是( )A、水是一种化学资源 B、电解水是验证水的组成的方法之一 C、水分子保持水的化学性质 D、在固态时水分子是静止不动的3. 2020年3月,四川凉山木里县突发森林火灾,下列说法错误的是( )A、森林地表腐质层的可燃性气体在雷击作用下达到着火点而燃烧,引发森林火灾 B、出动直升机开展吊桶投水扑灭山火,主要目的是降低可燃物的着火点 C、森林大火不易扑灭是因为山势陡峭,树林茂密,难以通过砍伐树木形成隔离带 D、消防人员灭火时要防止被森林大火灼烧,并戴好防护面罩避免吸入有害物质4. 小明同学依据描述书写的化学符号:①两个氮分子:2N2;②由三个氧原子构成的臭氧分子:3O;③粒子结构示意图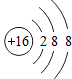 表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+。其中,正确的是( ) A、②④⑤ B、①④⑤ C、①③⑤ D、①④⑥5. 宏微结合是研究化学的重要思想。如图所示,提起压在水面上方的活塞,则相同微小空间内微粒的变化最可能是( )
表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+。其中,正确的是( ) A、②④⑤ B、①④⑤ C、①③⑤ D、①④⑥5. 宏微结合是研究化学的重要思想。如图所示,提起压在水面上方的活塞,则相同微小空间内微粒的变化最可能是( ) A、
A、 B、
B、 C、
C、 D、
D、 6. C919大飞机采用的复合材料中使用了高温陶瓷材料氮化硅(Si3N4),其中硅元素的化合价为+4价。下列说法正确的是( )A、Si3N4中Si、N元素的质量比是3:4 B、Si3N4中N元素的化合价为-3价 C、Si3N4含有2个氮分子 D、硅元素常温下化学性质比较活泼7. 下列实验操作正确的是( )A、
6. C919大飞机采用的复合材料中使用了高温陶瓷材料氮化硅(Si3N4),其中硅元素的化合价为+4价。下列说法正确的是( )A、Si3N4中Si、N元素的质量比是3:4 B、Si3N4中N元素的化合价为-3价 C、Si3N4含有2个氮分子 D、硅元素常温下化学性质比较活泼7. 下列实验操作正确的是( )A、 点燃酒精灯
B、
点燃酒精灯
B、 稀释浓硫酸
C、
稀释浓硫酸
C、 收集O2
D、
收集O2
D、 称量7.5g食盐
8. 推理是研究和学习化学的重要方法。以下说法正确的是( )A、甲烷和乙醇的燃烧产物都是二氧化碳和水,则甲烷和乙醇都是由碳、氢两种元素组成的碳氢化合物 B、洗涤剂除去衣服上的油污是利用了乳化作用,则汽油除去衣服上的油污也是利用了乳化作用 C、二氧化碳使饱和石灰水变浑浊是化学变化,则升温使饱和石灰水变浑浊也是化学变化 D、元素的种类是由质子数决定的,则质子数相同的原子属于同种元素9. 我国科研人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图所示,下列说法正确的是()
称量7.5g食盐
8. 推理是研究和学习化学的重要方法。以下说法正确的是( )A、甲烷和乙醇的燃烧产物都是二氧化碳和水,则甲烷和乙醇都是由碳、氢两种元素组成的碳氢化合物 B、洗涤剂除去衣服上的油污是利用了乳化作用,则汽油除去衣服上的油污也是利用了乳化作用 C、二氧化碳使饱和石灰水变浑浊是化学变化,则升温使饱和石灰水变浑浊也是化学变化 D、元素的种类是由质子数决定的,则质子数相同的原子属于同种元素9. 我国科研人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图所示,下列说法正确的是() A、甲是单质,乙、丙、丁均为氧化物 B、生成物丙由1个碳原子、4个氢原子和1个氧原子构成 C、参加反应的甲和乙的分子个数比为3:1 D、生成物丙中碳、氢和氧元素的质量比为1:4:110. 下列各组固体物质,只用水不能进行鉴别的是( )A、CaCO3、Na2CO3 B、Na2CO3、NaCl C、CaO、Ca(OH)2 D、CuSO4、FeCl311. 已知生活中厕所清洁剂的pH=1,厨房的清洁剂的pH=12。下列关于两者的说法错误的是( )A、厕所清洁剂加水稀释,溶液pH升高 B、厨房清洁剂可能含有NaOH C、混合使用能提高两者的清洁效果 D、厕所清洁剂可能使铁制下水道腐蚀12. NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是( )
A、甲是单质,乙、丙、丁均为氧化物 B、生成物丙由1个碳原子、4个氢原子和1个氧原子构成 C、参加反应的甲和乙的分子个数比为3:1 D、生成物丙中碳、氢和氧元素的质量比为1:4:110. 下列各组固体物质,只用水不能进行鉴别的是( )A、CaCO3、Na2CO3 B、Na2CO3、NaCl C、CaO、Ca(OH)2 D、CuSO4、FeCl311. 已知生活中厕所清洁剂的pH=1,厨房的清洁剂的pH=12。下列关于两者的说法错误的是( )A、厕所清洁剂加水稀释,溶液pH升高 B、厨房清洁剂可能含有NaOH C、混合使用能提高两者的清洁效果 D、厕所清洁剂可能使铁制下水道腐蚀12. NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是( )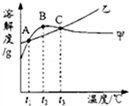
温度/℃ 10 20 30 40 50 60 溶解度S/g NH4Cl 33.3 37.2 41.4 45.8 50.4 60.2 Na2SO4 9.6 20.2 40.8 48.4 47.5 47.0 A、乙为NH4Cl B、t3应介于40℃﹣50℃ C、55℃时,分别将两饱和溶液蒸发等质量的水,得到固体质量甲>乙 D、等质量的甲、乙饱和溶液从t3降温到t1 , 析出的晶体质量相等二、填空题
-
13. 全球碳循环如图所示,为降低大气中CO2浓度,有以下途径。

海洋封存:利用庞大的水体使海洋成为封存CO2的容器,但会引起海水酸化等。
地质封存:将CO2注入特定的地层,该方法最大的风险是CO2泄漏,局部CO2浓度快速上升,直接威胁人类生命健康等。
综合利用:工业上可以将CO2转化成尿素[CO(NH2)2]、甲醇(CH3OH)等资源。科学家发现了一种镍与有机物组成的混合催化剂,利用太阳光能,将水中溶解的CO2转化成CO和O2。
依据文章内容,回答下列问题。
(1)、在全球碳循环中,能消耗二氧化碳的途径是(2)、化石燃料包括煤、石油和 , 化石燃料燃烧会产生二氧化碳,因为化石燃料中含有元素。(3)、上述综合利用CO2得到的产品中,属于氧化物的是(填化学式)。(4)、下列说法错误的是_______。A、碳循环中的“碳”是指碳单质 B、CO2是温室气体,对人类生活有害无利 C、海洋封存CO2会引起海水酸化14. 某课外活动中,学生利用下图所示的材料完成探究实验,杠杆已调至平衡。 (1)、实验1中,较长时间后,左边铁粉布包下降,是因为铁粉与发生了反应。将铁粉换成下列物质中的(填序号),杠杆也会出现相似现象。
(1)、实验1中,较长时间后,左边铁粉布包下降,是因为铁粉与发生了反应。将铁粉换成下列物质中的(填序号),杠杆也会出现相似现象。A.NaCl
B.NaOH
C.CaO
(2)、实验2中,通入CO2一段时间,右边乒乓球(填“上升”或“下降”)。再往集气瓶中滴入足量NaOH溶液,杠杆重新平衡,发生反应的化学方程式为。三、综合题
-
15. 某化学实验室从含少量硝酸锌的硝酸银废液中提取贵金属Ag,其主要操作流程如下:
 (1)、步骤Ⅰ中用到玻璃棒的作用: , 得到的固体A的成分:。(2)、步骤Ⅰ中发生反应的化学方程式是 , 这一反应说明两金属的活泼性ZnAg(填“>”或“<”)。(3)、向溶液D中加入适量某物质,可得到只含一种溶质的溶液,这种物质是。16. “富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗炼钢等。在2019年年末出现的“新型肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和"富氧空气"差不多,化学兴趣小组欲制取“富氧空气”并开展相关探究,进行以下实验。(1)、实验一:制取“富氧空气”
(1)、步骤Ⅰ中用到玻璃棒的作用: , 得到的固体A的成分:。(2)、步骤Ⅰ中发生反应的化学方程式是 , 这一反应说明两金属的活泼性ZnAg(填“>”或“<”)。(3)、向溶液D中加入适量某物质,可得到只含一种溶质的溶液,这种物质是。16. “富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗炼钢等。在2019年年末出现的“新型肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和"富氧空气"差不多,化学兴趣小组欲制取“富氧空气”并开展相关探究,进行以下实验。(1)、实验一:制取“富氧空气”
用高锰酸钾制取氧气
①写出反应的化学方程式:
②仪器C的名称为;
(2)、混制“富氧空气”
如图,用纯氮气及上述实验制取的氧气,混制一瓶氧气体积分数为40%的“富氧空气”,气体应从装置中的管(选“a”或“b”)通入,先通入氮气排出120mL水,再通入氧气排出mL水。
(3)、实验二:测定“富氧空气”中氧气的含量用下图装置测定“富氧空气”中氧气的含量(集气瓶中"富氧空气"体积为100mL,底部残留少量水,燃烧匙内有足量红磷)。操作如下:

i往量筒内加入适量水,读出量筒内水的体积为V1mL;
ii用电点火装置点燃红磷,充分反应;
iii打开止水夹,待右侧量筒内液面不再变化时,排出气球中的气体,调节两边液面在同一水平面上,读出量筒内水的体积为V2mL。回答问题:
实验前,检查装置气密性的方法:;
(4)、操作 ii中可观察到现象:(5)、本次实验测得“富氧空气”中氧气的含量为(用含V1、V2的式子表示)。(6)、若读取V1时仰视,读取V2时俯视,则测得实验结果(选填“偏大”“偏小”或“无影响”)。(7)、实验三:研究“富氧空气”的应用通过重油、褐煤在氧气含量不同的空气中燃烧的实验,得到有关数据如下图:

结合图1,说明空气中氧气含量与燃烧产生的温度的关系:。
(8)、结合图2,简述减少燃料燃烧尾气污染的措施:。17. 某实验小组探究了溶质的质量分数对H2O2分解速率的影响。实验装置如图所示,用注射器加入不同浓度的H2O2溶液(见下表),实验中使用传感器装置测算生成O2的质量(圆底烧瓶内气压变化在安全范围),绘制氧气质量随时间变化的曲线,如图所示。试验编号
的质量分数(%)
溶液的体积(mL)
对应曲线
Ⅰ
3.4
10.0
a
Ⅱ
2.4
10.0
b
Ⅲ
1.7
10.0
C(待绘制)
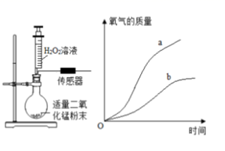 (1)、实验前需准备不同浓度的H2O2溶液,若要配制100g质量分数为2.4%的H2O2溶液,需质量分数为30%的H2O2溶液g。(2)、根据实验探究目的,从曲线a、b中,可得出的结论是(3)、在图中画出曲线c的大致位置及趋势。(4)、计算实验Ⅰ条件下H2O2完全分解所得氧气的质量,并写出具体计算过程(1.5-5.0%H2O2溶液的密度均取值1.0g/mL)。
(1)、实验前需准备不同浓度的H2O2溶液,若要配制100g质量分数为2.4%的H2O2溶液,需质量分数为30%的H2O2溶液g。(2)、根据实验探究目的,从曲线a、b中,可得出的结论是(3)、在图中画出曲线c的大致位置及趋势。(4)、计算实验Ⅰ条件下H2O2完全分解所得氧气的质量,并写出具体计算过程(1.5-5.0%H2O2溶液的密度均取值1.0g/mL)。