浙教版科学九上第一章第5节 酸和碱之间发生的反应同步练习(基础巩固)
试卷更新日期:2021-07-05 类型:同步测试
一、单选题
-
1. 蚂蚁等昆虫叮咬人时,会向人体注入一种物质R,使皮肤红肿。实验测定物质R呈酸性,由此推断,要消除红肿,可涂抹下列物质中的( )A、食醋 B、肥皂水 C、浓氢氧化钠溶液 D、稀盐酸2. 如图所示是硫酸和氢氧化钠溶液反应时pH的变化图象,下列说法正( )
 A、图中a点所示溶液中,含有的溶质是硫酸钠和硫酸 B、图中b点时,硫酸和氢氧化钠恰好完全反应 C、图中c点所示溶液呈碱性 D、该实验是将氢氧化钠溶液滴到硫酸溶液中3. 在做盐酸和氢氧化钠溶液反应的实验时,通常不需要用到( )。A、酚酞试液 B、试管 C、滴管 D、量筒4. 科学与生活密切相关,下列说法正确的是( )A、在煤炉上放一盆水可防止煤气中毒 B、用铅笔芯的粉末可使锁的开启变得灵活 C、胃酸过多的病人在空腹时最好多喝一些柠檬汁 D、打雷下雨时,可以站在大树下避雨5. SO2是形成酸雨的主要物质,能有效吸收SO2的溶液是( )A、NaOH B、Na2SO4 C、H2SO4 D、NaCl6. 芋艿(俗称毛芋)是一种常见的食品,新鲜芋艿在去皮时会出现一种白色的汁液,汁液内含有一种碱性物质——皂角甙,沾上它会奇痒难忍,下列厨房中的物质止痒效果最好的是( )A、食醋 B、料酒 C、纯碱 D、食盐水7. 关于中和反应的说法,错误的是( )A、一定是复分解反应 B、一定有氧化物生成 C、一定是放热反应 D、一定没有沉淀生成8. 下列关于酸和碱反应的说法中,错误的是( )A、酸碱的反应要放出热量 B、酸碱的反应一定有盐生成 C、酸碱的反应一定有水生成 D、酸碱恰好完全反应后溶液的pH=09.
A、图中a点所示溶液中,含有的溶质是硫酸钠和硫酸 B、图中b点时,硫酸和氢氧化钠恰好完全反应 C、图中c点所示溶液呈碱性 D、该实验是将氢氧化钠溶液滴到硫酸溶液中3. 在做盐酸和氢氧化钠溶液反应的实验时,通常不需要用到( )。A、酚酞试液 B、试管 C、滴管 D、量筒4. 科学与生活密切相关,下列说法正确的是( )A、在煤炉上放一盆水可防止煤气中毒 B、用铅笔芯的粉末可使锁的开启变得灵活 C、胃酸过多的病人在空腹时最好多喝一些柠檬汁 D、打雷下雨时,可以站在大树下避雨5. SO2是形成酸雨的主要物质,能有效吸收SO2的溶液是( )A、NaOH B、Na2SO4 C、H2SO4 D、NaCl6. 芋艿(俗称毛芋)是一种常见的食品,新鲜芋艿在去皮时会出现一种白色的汁液,汁液内含有一种碱性物质——皂角甙,沾上它会奇痒难忍,下列厨房中的物质止痒效果最好的是( )A、食醋 B、料酒 C、纯碱 D、食盐水7. 关于中和反应的说法,错误的是( )A、一定是复分解反应 B、一定有氧化物生成 C、一定是放热反应 D、一定没有沉淀生成8. 下列关于酸和碱反应的说法中,错误的是( )A、酸碱的反应要放出热量 B、酸碱的反应一定有盐生成 C、酸碱的反应一定有水生成 D、酸碱恰好完全反应后溶液的pH=09.根据图,判断以下说法错误的是( )
 A、取液后的滴管不能倒置 B、用玻璃棒搅拌使反应充分 C、用酚酞溶液判断该反应是否发生 D、生成盐和水的反应都是中和反应10. 下列没有运用中和反应原理的是( )A、服用含氢氧化镁的药物,可以治疗胃酸过多症 B、用熟石灰改良酸性土壤 C、蚊虫叮咬处涂上肥皂水,可减轻痛痒 D、用生石灰做干燥剂11. 下列物质中常用来改良土壤酸性的是 ( )A、石灰石 B、熟石灰 C、干冰 D、烧碱12. 稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( )
A、取液后的滴管不能倒置 B、用玻璃棒搅拌使反应充分 C、用酚酞溶液判断该反应是否发生 D、生成盐和水的反应都是中和反应10. 下列没有运用中和反应原理的是( )A、服用含氢氧化镁的药物,可以治疗胃酸过多症 B、用熟石灰改良酸性土壤 C、蚊虫叮咬处涂上肥皂水,可减轻痛痒 D、用生石灰做干燥剂11. 下列物质中常用来改良土壤酸性的是 ( )A、石灰石 B、熟石灰 C、干冰 D、烧碱12. 稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( ) A、在混合液中加金属Zn,无气泡产生 B、在混合液中加无色酚酞,溶液呈无色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH等于713. 下图是收集、吸收某气体的装置(A 装置收集气体,B装置吸收多余气体)。由实验装置推测该气体的有关性质如下表,其中可能正确的是( )
A、在混合液中加金属Zn,无气泡产生 B、在混合液中加无色酚酞,溶液呈无色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH等于713. 下图是收集、吸收某气体的装置(A 装置收集气体,B装置吸收多余气体)。由实验装置推测该气体的有关性质如下表,其中可能正确的是( )
A
B
C
D
密度比空气
小
小
大
大
溶于水中所得溶液的pH
>7
<7
>7
<7
A、A B、B C、C D、D14. 某实验小组用传感器探究稀氢氧化钠溶液与稀盐酸反应过程中温度和pH的变化,测定结果如图所示。下列说法正确的是( ) A、实验中溶液的温度一直升高、pH一直增大 B、氢氧化钠与盐酸的中和反应先放热后吸热 C、40s时溶液中的溶质为氢氧化钠和氯化钠 D、该实验是将稀氢氧化钠溶液滴入稀盐酸中15. 下列生活经验没有应用酸碱反应原理的是( )A、用熟石灰改良酸性土壤 B、用氢氧化钠溶液洗涤石油产品中的残留硫酸 C、用氢氧化铝治疗胃酸过多 D、用生石灰作干燥剂16. 酸碱反应在日常生产和生活中有广泛的用途。下列应用与酸碱反应原理无关的是( )A、用氢氧化钠溶液洗涤石油产品中残余硫酸 B、用Al(OH)3中和多余的胃酸 C、手上沾到浓硫酸用抹布擦去、清水冲洗后,涂抹小苏打溶液 D、施用熟石灰改良酸性土壤17. 小晨在完成如图氢氧化钠与稀硫酸反应试验后,想判断加入的稀硫酸是否过量,他取出部分反应后的液体,利用下列方法进行判断,可取的是( )
A、实验中溶液的温度一直升高、pH一直增大 B、氢氧化钠与盐酸的中和反应先放热后吸热 C、40s时溶液中的溶质为氢氧化钠和氯化钠 D、该实验是将稀氢氧化钠溶液滴入稀盐酸中15. 下列生活经验没有应用酸碱反应原理的是( )A、用熟石灰改良酸性土壤 B、用氢氧化钠溶液洗涤石油产品中的残留硫酸 C、用氢氧化铝治疗胃酸过多 D、用生石灰作干燥剂16. 酸碱反应在日常生产和生活中有广泛的用途。下列应用与酸碱反应原理无关的是( )A、用氢氧化钠溶液洗涤石油产品中残余硫酸 B、用Al(OH)3中和多余的胃酸 C、手上沾到浓硫酸用抹布擦去、清水冲洗后,涂抹小苏打溶液 D、施用熟石灰改良酸性土壤17. 小晨在完成如图氢氧化钠与稀硫酸反应试验后,想判断加入的稀硫酸是否过量,他取出部分反应后的液体,利用下列方法进行判断,可取的是( ) A、加入氯化钡溶液,是否有白色沉淀产生 B、加入少量氯化铜溶液,是否有蓝色沉淀生成 C、加入少量氢氧化铁,红色固体是否消失 D、滴加酚酞试液,观察是否不变色18. 下列化学反应属于酸碱反应的是( )A、Cu(OH)2 +2HNO3=Cu(NO3)2 +2H2O B、CO2+H2O=H2CO3 C、2KMnO4 K2MnO4 + MnO2 + O2↑ D、AgNO3+HCl=AgCl↓+HNO319. 某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
A、加入氯化钡溶液,是否有白色沉淀产生 B、加入少量氯化铜溶液,是否有蓝色沉淀生成 C、加入少量氢氧化铁,红色固体是否消失 D、滴加酚酞试液,观察是否不变色18. 下列化学反应属于酸碱反应的是( )A、Cu(OH)2 +2HNO3=Cu(NO3)2 +2H2O B、CO2+H2O=H2CO3 C、2KMnO4 K2MnO4 + MnO2 + O2↑ D、AgNO3+HCl=AgCl↓+HNO319. 某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( ) A、图中a点所示溶液中,含有的溶质是NaCl和NaOH B、由a点到b点的pH变化过程证明酸和碱发生了中和反应 C、向图中c点所示溶液中滴加无色酚酞,溶液不变色 D、该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中20. 中和反应在生活生产中有广泛的应用,下列做法不是利用中和反应原理的是( )A、用熟石灰改良酸性土壤 B、用含氢氧化镁的药物治疗胃酸过多 C、用盐酸除去铁锈 D、用氨水(NH3·H2O)处理工厂的硫酸
A、图中a点所示溶液中,含有的溶质是NaCl和NaOH B、由a点到b点的pH变化过程证明酸和碱发生了中和反应 C、向图中c点所示溶液中滴加无色酚酞,溶液不变色 D、该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中20. 中和反应在生活生产中有广泛的应用,下列做法不是利用中和反应原理的是( )A、用熟石灰改良酸性土壤 B、用含氢氧化镁的药物治疗胃酸过多 C、用盐酸除去铁锈 D、用氨水(NH3·H2O)处理工厂的硫酸二、填空题
-
21. 教材指出:酸与碱中和反应的结果是酸和碱各自的特性都消失.如图描述的是氢氧化钠与盐酸反应的微观实质,请从微观的角度分析,甲、乙处应填入的化学符号依次是 、 .
 22. 中和反应: 跟 作用生成盐和水的反应叫做中和反应。23. 处理工厂的废水。如硫酸厂废水中含有硫酸等杂质,可以用 、 等碱性物质中和。
22. 中和反应: 跟 作用生成盐和水的反应叫做中和反应。23. 处理工厂的废水。如硫酸厂废水中含有硫酸等杂质,可以用 、 等碱性物质中和。
24. 中和反应的实质是酸中的 和碱中 的反应生成 。25. 在酸性环境中可抑制 的繁殖,人们经常在食物中加入少量食用醋酸。26. 如图1表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化曲线.请从曲线图中获取信息,回答下列问题:
(1)实验操作是按照图2中 (甲或乙)图所示进行的,烧杯中溶液的颜色由 色逐渐变为 色.发生反应的化学方程式为 .
(2)实验结束时,老师滴加两滴反应后的溶液到玻璃片上,烘干后出现白色固体.小明说这是氢氧化钠,小刚认为不可能,证据是 .
(3)图3是反应的微观变化图,对比反应前后的微粒,此反应的实质是盐酸溶液中的 与氢氧化钠溶液中的氢氧根离子结合,生成了水.酸和碱往往都能发生类似反应,请尝试书写氯酸(HClO3)与氢氧化钾(KOH)反应的化学方程式 .
(4)用溶质的质量分数为36.5%的盐酸20g与足量氢氧化钠溶液恰好完全反应,需要溶质的质量分数为20%的氢氧化钠溶液 g.
27. 某同学取自家农田的土壤测得pH小于7,大部分农作物适合在接近中性的土壤中生长,你认为此农田应该加入一种碱 (写俗称)来改良,写出它的另一种用途 。28. 中和反应的实质是酸溶液中的 离子和碱中的 离子相结合生成 分子,例如:在稀盐酸溶液中滴加氢氧化钠溶液 。29. 构建安全体系,建设小康社会,关系国计民生.近期,媒体报道的某些环境问题、卫生问题和安全问题引发人们的关注:(1)据报道:“济南俩月查处了13家‘铝包子’铺”,所得‘铝包子’是指所用面粉中非法加入含有硫酸铝铵[NH4Al(SO4)2.12H2O]成分的泡打粉,食物中铝元素超标,危害身体健康,在硫酸铝铵中,所含非金属元素共有 种.
(2)露天烧烤不仅污染环境,导致周边空气中PM2.5指数严重超标.在烧烤的肉类食物中还含有强致癌物质﹣﹣苯并(a)芘(化学式C20H12),在苯并(a)芘中,氢元素与碳元素的原子个数之比为 (填最简整数比).
(3)据报道,2015年5月6日在104国道某段,一辆载有20多吨浓硫酸的罐车不慎侧翻,造成大量硫酸泄漏,有关部门调来大量熟石灰粉[主要成分Ca(OH)2]和沙土用于清除泄漏的硫酸.试写出硫酸和熟石灰反应的化学方程式 .
(4)世界卫生组织将5月31日定为“世界无烟日”,我国采用了公共场所禁止吸烟等控烟措施.吸烟有害健康,我国遭受二手烟危害的非吸烟人口就多达7.4亿.烟雾中主要含有一氧化碳、尼古丁(C10H14N2)和焦油,这三种物质被称为香烟的三大杀手.下列有关说法中,正确的是 (填写序号A、B、C、D之一)
①生活中应拒绝毒品 ②焦油能诱发细胞病变 ③吸烟对他人无害
④“煤气”中毒是由一氧化碳引起的 ⑤在尼古丁中氮元素的含量最高
A.①④⑤,B.①②③,C.①②④,D.②③⑤
30. 请完成以下实验报告的填写.实验名称:酸和碱的中和反应
实验目的:验证盐酸和氢氧化钠能否发生反应.
供选择的仪器和药品:试管、胶头滴管、烧杯、酚酞溶液、稀盐酸、氢氧化钠稀溶液.
实验步骤
实验现象
实验结论、解释
(1)在 中加入约1mL氢氧化钠稀溶液,用胶头滴管滴入几滴酚酞溶液.
溶液显 色
碱能使酚酞溶液变色
(2)然后, ,直至溶液恰好变无色为止.
溶液颜色最后褪去
两者能发生反应,反应的化学方程式是 .
三、解答题
-
31. 将m1g 7.3% HCl溶液和m2g未知浓度的NaOH溶液混合均匀,测量并记录溶液温度,实验结果如下图所示(实验中始终保持m1+m2=50g)。
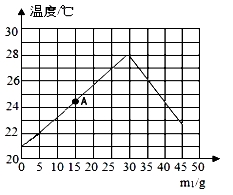 (1)、做该实验时环境温度为℃左右。(2)、实验过程中溶液温度升高的原因是。(3)、图中A点所得溶液中的两种溶质是。(4)、通过计算确定NaOH溶液的溶质质量分数为多少?32. 用质量分数为 5%的稀盐酸和 10%的氢氧化钠溶液进行酸碱反应实验时,反应过程中溶 液的酸碱度变化如图所示:
(1)、做该实验时环境温度为℃左右。(2)、实验过程中溶液温度升高的原因是。(3)、图中A点所得溶液中的两种溶质是。(4)、通过计算确定NaOH溶液的溶质质量分数为多少?32. 用质量分数为 5%的稀盐酸和 10%的氢氧化钠溶液进行酸碱反应实验时,反应过程中溶 液的酸碱度变化如图所示: (1)、该实验是将(选填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中;(2)、当加入溶液的质量为 b 时,溶液中的溶质有;(3)、当加入溶液的质量 a 为 20 g 时,求所得溶液中溶质的质量。
(1)、该实验是将(选填“稀盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中;(2)、当加入溶液的质量为 b 时,溶液中的溶质有;(3)、当加入溶液的质量 a 为 20 g 时,求所得溶液中溶质的质量。四、实验探究题
-
33. 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
(1)、【学生板演】该反应的化学方程式 .(2)、【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下,请你补上猜想四.
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH
猜想四:
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 ,
理由是 .
(3)、【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 .
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用了老师提供的pH试纸、Na2CO3溶液、BaCl2溶液,进行如下三个方案的探究.
实验方案
测溶液的pH
滴加Na2CO3溶液
滴加BaCl2溶液
实验操作



实验现象
试纸变色,对比比色卡,pH<7
产生白色沉淀
实验结论
溶液中有H2SO4
溶液中有H2SO4
溶液中有H2SO4
(4)、【得出结论】通过探究,全班同学一致确定猜想二是正确的.【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了如下两处错误:
①实验操作中的错误是 ;
②实验方案中也有一个是错误的,错误的原因是 .