湖南省湘潭市2021年中考化学试卷
试卷更新日期:2021-07-02 类型:中考真卷
一、单选题
-
1. 下列变化属于物理变化的是( )A、酒精挥发 B、蜡烛燃烧 C、钢铁冶炼 D、粮食酿酒2. 下列物质属于纯净物的是( )A、河水 B、空气 C、石油 D、氮气3. 下列食物主要为人体提供蛋白质的是( )A、米饭 B、鸡蛋 C、牛油 D、蔬菜4. 下列图标与燃烧和爆炸有关的是( )A、
 B、
B、 C、
C、 D、
D、 5. 湘潭又名“莲城”,初夏时节,荷花盛开,花香怡人,这主要是因为( )A、分子之间有间隔 B、分子质量很小 C、分子在不断运动 D、分子由原子构成6. 人体适量摄入下列哪种微量元素可以预防贫血( )A、铁 B、锌 C、硒 D、碘7. 正确的实验操作是科学探究成功的基础。下列操作错误的是( )A、稀释浓硫酸
5. 湘潭又名“莲城”,初夏时节,荷花盛开,花香怡人,这主要是因为( )A、分子之间有间隔 B、分子质量很小 C、分子在不断运动 D、分子由原子构成6. 人体适量摄入下列哪种微量元素可以预防贫血( )A、铁 B、锌 C、硒 D、碘7. 正确的实验操作是科学探究成功的基础。下列操作错误的是( )A、稀释浓硫酸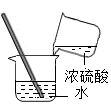 B、检查装置气密性
B、检查装置气密性  C、闻药品气味
C、闻药品气味  D、配制氯化钠溶液
D、配制氯化钠溶液 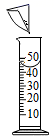 8. “庄稼一枝花,全靠肥当家”,下列化肥属于含钾复合肥的是( )A、CO(NH2)2 B、KNO3 C、KCl D、Ca3(PO4)29. 下列实验现象的描述,正确的是( )A、红磷在氧气中燃烧产生大量白雾 B、硫在氧气中燃烧产生微弱的淡蓝色火焰 C、铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 D、一氧化碳高温还原氧化铁,红棕色粉末逐渐变为黑色10. 2021年全球新冠肺炎疫情防控期间,各种消毒剂如酒精、二氧化氯、过氧乙酸等被广泛使用,其中二氧化氯(ClO2)中Cl元素的化合价是( )A、-1 B、+1 C、+4 D、+711. 生活中一些常见物质的近似pH如下表,其中酸性最强的物质是( )
8. “庄稼一枝花,全靠肥当家”,下列化肥属于含钾复合肥的是( )A、CO(NH2)2 B、KNO3 C、KCl D、Ca3(PO4)29. 下列实验现象的描述,正确的是( )A、红磷在氧气中燃烧产生大量白雾 B、硫在氧气中燃烧产生微弱的淡蓝色火焰 C、铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 D、一氧化碳高温还原氧化铁,红棕色粉末逐渐变为黑色10. 2021年全球新冠肺炎疫情防控期间,各种消毒剂如酒精、二氧化氯、过氧乙酸等被广泛使用,其中二氧化氯(ClO2)中Cl元素的化合价是( )A、-1 B、+1 C、+4 D、+711. 生活中一些常见物质的近似pH如下表,其中酸性最强的物质是( )物质
葡萄汁
苹果汁
牛奶
玉米粥
pH
3.5~4.5
2.9~3.3
6.3~6.6
6.8~8.0
A、葡萄汁 B、苹果汁 C、牛奶 D、玉米粥12. 下列说法错误的是( )A、炒菜时油锅着火,可用锅盖盖灭 B、煤炉上放一壶水可预防CO中毒 C、干冰升华吸热,可用于人工降雨 D、洗洁精有乳化作用,可用于去油污13. 根据如下微观示意图分析,下列结论正确的是( ) A、反应前后原子种类不变 B、丙物质的相对分子质量是18g C、参加反应的甲与乙分子个数比为1:1 D、反应前后各元素的化合价均不变14. 下列说法不合理的是( )A、鉴别羊毛和棉线可用灼烧的方法 B、稀硫酸可用于金属表面除锈 C、NH4NO3溶于水放出热量,水温升高 D、熟石灰可用于改良酸性土壤15. 石笋和钟乳石的形成蕴含许多化学原理,其反应之一为: 则X的化学式为( )A、CaCO3 B、Ca(OH)2 C、CaO D、CaH216. 能在pH=3的溶液中大量共存,且溶液无色透明的一组离子是( )A、Ag+、K+、 、Cl- B、Fe3+、Ca2+、Cl-、 C、Ba2+、Na+、 、 D、Mg2+、Na+、 、Cl-17. 将下列四种物质放入密闭容器中充分反应,测得反应前后各物质的质量如下表。下列说法正确的是( )
A、反应前后原子种类不变 B、丙物质的相对分子质量是18g C、参加反应的甲与乙分子个数比为1:1 D、反应前后各元素的化合价均不变14. 下列说法不合理的是( )A、鉴别羊毛和棉线可用灼烧的方法 B、稀硫酸可用于金属表面除锈 C、NH4NO3溶于水放出热量,水温升高 D、熟石灰可用于改良酸性土壤15. 石笋和钟乳石的形成蕴含许多化学原理,其反应之一为: 则X的化学式为( )A、CaCO3 B、Ca(OH)2 C、CaO D、CaH216. 能在pH=3的溶液中大量共存,且溶液无色透明的一组离子是( )A、Ag+、K+、 、Cl- B、Fe3+、Ca2+、Cl-、 C、Ba2+、Na+、 、 D、Mg2+、Na+、 、Cl-17. 将下列四种物质放入密闭容器中充分反应,测得反应前后各物质的质量如下表。下列说法正确的是( )物质
甲
乙
丙
丁
反应前质量/g
1
10
27
4
反应后质量/g
1
a
0
23
A、a的值是8 B、甲物质一定是该反应的催化剂 C、该反应属于分解反应 D、反应过程中乙、丁的质量比是5:218. 除去下列括号内的余质,所选用的试剂错误的是( )A、CaO(CaCO3):足量稀盐酸 B、Fe(Zn):足量硫酸亚铁溶液 C、MnO2(KCl):足量水 D、NaCl(MgCl2):适量氢氧化钠溶液19. 下列图像不能正确反映其对应关系的是( )A、加热一定质量的KMnO4固体制取氧气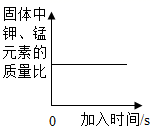 B、氯化铁和盐酸的混合溶液中加入氢氧化钠溶液至过量
B、氯化铁和盐酸的混合溶液中加入氢氧化钠溶液至过量 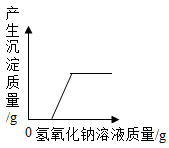 C、一定质量的AgNO3和 Cu(NO3)2的混合溶液中加入足量Fe粉
C、一定质量的AgNO3和 Cu(NO3)2的混合溶液中加入足量Fe粉 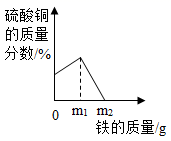 D、稀盐酸与氢氧化钠溶液反应过程中pH变化曲线,X表示氢氧化钠溶液
D、稀盐酸与氢氧化钠溶液反应过程中pH变化曲线,X表示氢氧化钠溶液 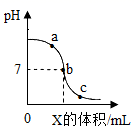 20. 取一定质量的Fe(OH)3固体加热至550℃完全分解为Fe2O3和H2O,温度提高到1400℃时,Fe2O3继续分解为复杂的铁的氧化物和O2;将产生的气体先通过浓硫酸,浓硫酸质量增加5.4克,再通过灼热的铜网,铜网质量增加0.8克(产生的气体均被完全吸收)。则所得复杂的铁的氧化物化学式为( )A、FeO B、Fe3O4 C、Fe4O5 D、Fe5O7
20. 取一定质量的Fe(OH)3固体加热至550℃完全分解为Fe2O3和H2O,温度提高到1400℃时,Fe2O3继续分解为复杂的铁的氧化物和O2;将产生的气体先通过浓硫酸,浓硫酸质量增加5.4克,再通过灼热的铜网,铜网质量增加0.8克(产生的气体均被完全吸收)。则所得复杂的铁的氧化物化学式为( )A、FeO B、Fe3O4 C、Fe4O5 D、Fe5O7二、填空题
-
21. 请用化学用语填空:(1)、氖元素。(2)、2个氢氧根离子。(3)、天然气的主要成分。(4)、氧化铝中铝元素的化合价。22. 化学就在我们身边。请从下列选项中选择适当的物质填空(填字母序号):
A.小苏打 B.二氧化硫 C.金刚石 D.生石灰
(1)、能形成酸雨的是。(2)、可用于做装饰品的是。(3)、可用作食品干燥剂的是。(4)、常用于治疗胃酸过多症的是。23. 2021年3月全国两会期间,“碳达峰”、“碳中和”成为热词,旨在推动社会各界和公众积极参与生态文明建设,携手行动,共建天蓝、地绿、水清的美丽中国。请回答:(1)、天气中CO2的含量不断上升,从而导致的环境问题是增强,全球气候变暖。(2)、大气中CO2的产生主要来自化石燃料的燃烧,化石燃料属于(填“可再生”或“不可再生”)能源。(3)、随着全球能源使用的增长,化石燃料日趋枯竭,科学家正在开发利用新能源,请列举一种新能源。(4)、“碳中和”主要是指抵消温室气体的排放量,实现正负抵消,达到相对“零排放”。下列说法错误的是______(填字母序号)。A、大力植树造林 B、捕集、利用和封存CO2 C、提倡使用一次性餐具24. 1869年,门捷列夫发现了元素周期律,使化学学习和研究变得有规律可循。左图是1至18号元素、右图是38号元素锶(元素符号为Sr)的原子结构示意图: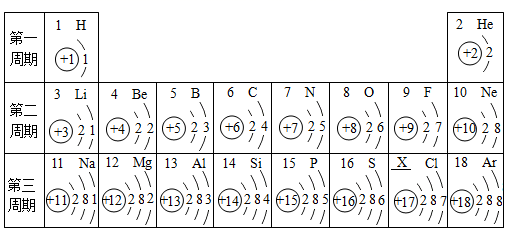
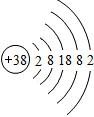 (1)、左图中,X=。(2)、锶原子在化学反应中容易(填“得到”或“失去”)电子,形成的离子符号为。(3)、你还能发现的规律是:同一周期(横行)从左往右依次递增(写一种即可)。25. 甲、乙、丙三种固体物质的溶解度曲线如下图所示,请回答下列问题:
(1)、左图中,X=。(2)、锶原子在化学反应中容易(填“得到”或“失去”)电子,形成的离子符号为。(3)、你还能发现的规律是:同一周期(横行)从左往右依次递增(写一种即可)。25. 甲、乙、丙三种固体物质的溶解度曲线如下图所示,请回答下列问题: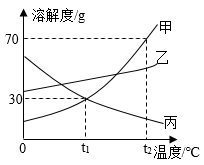 (1)、t1℃时,丙物质的溶解度为g。(2)、t2℃时,往盛有50g蒸馏水的烧杯中加入50g甲固体,充分溶解后所得溶液的质量为g。(3)、除去甲中含有的少量丙,可采用的方法是法(填“降温结晶”或“蒸发结晶”)。(4)、将t1℃时的甲、乙、丙三种物质的饱和溶液升温至t2℃,所得溶液溶质的质量分数由大到小的顺序为。26. 古代“丝绸之路”把中国的丝绸、茶叶传入西方,将西方的宝石传入中国。茶叶中含有维生素C(化学式为C6H8O6),请回答下列问题:(1)、维生素C属于(填“有机”或“无机”)化合物。(2)、维生素C是由种元素组成,其中碳、氢两种元素的质量比为(填最简整数比)。(3)、将维生素C在一定质量的氧气中充分燃烧,生成CO、CO2和H2O,测得生成物的总质量为30.4克,其中水的质量为7.2克,则参加反应的氧气质量为克。27. 2021年3月,三星堆遗址新出土重要文物500多件,有高2.62米的青铜大立人、高3.95米的青铜神树、象牙等,多属前所未见的稀世之珍。(1)、青铜古称“吉金”是金属冶铸史上最早出现的合金,青铜属于(填“金属”或“合成”)材料,青铜的硬度比纯铜(填“大”或“小”)。(2)、生活中铜制品长期露置在潮湿空气中会锈蚀,生成“铜绿”(化学式为Cu2(OH)2CO3)。
(1)、t1℃时,丙物质的溶解度为g。(2)、t2℃时,往盛有50g蒸馏水的烧杯中加入50g甲固体,充分溶解后所得溶液的质量为g。(3)、除去甲中含有的少量丙,可采用的方法是法(填“降温结晶”或“蒸发结晶”)。(4)、将t1℃时的甲、乙、丙三种物质的饱和溶液升温至t2℃,所得溶液溶质的质量分数由大到小的顺序为。26. 古代“丝绸之路”把中国的丝绸、茶叶传入西方,将西方的宝石传入中国。茶叶中含有维生素C(化学式为C6H8O6),请回答下列问题:(1)、维生素C属于(填“有机”或“无机”)化合物。(2)、维生素C是由种元素组成,其中碳、氢两种元素的质量比为(填最简整数比)。(3)、将维生素C在一定质量的氧气中充分燃烧,生成CO、CO2和H2O,测得生成物的总质量为30.4克,其中水的质量为7.2克,则参加反应的氧气质量为克。27. 2021年3月,三星堆遗址新出土重要文物500多件,有高2.62米的青铜大立人、高3.95米的青铜神树、象牙等,多属前所未见的稀世之珍。(1)、青铜古称“吉金”是金属冶铸史上最早出现的合金,青铜属于(填“金属”或“合成”)材料,青铜的硬度比纯铜(填“大”或“小”)。(2)、生活中铜制品长期露置在潮湿空气中会锈蚀,生成“铜绿”(化学式为Cu2(OH)2CO3)。(查阅资料)
(工艺流程)为从某锈蚀的铜样品中回收铜并制得硫酸锌,取该铜样品(除含有铜、锌和铜绿外,不含其它物质),进行如下操作:

请回答下列问题:
①气体a中含有H2和(填化学式),溶液A的颜色为色。
②操作Ⅰ的名称是 , 该操作中玻璃棒的作用是。
③写出②中发生反应的化学方程式(写一个即可),该反应属于基本反应类型中的反应。
28. 根据实验图示回答下列问题: (1)、写出图一中仪器a的名称。(2)、实验室用加热高锰酸钾固体的方法制取氧气,选择的发生装置是(填字母序字号),加热时,应使用酒精灯的焰集中加热;检验氧气可用。(3)、实验室制取CO2应选择的发生和收集装置是(填字母序号),其反应的化学方程式为。(4)、镁粉在火星上可以扮演地球上煤的角色,通过采用Mg/CO2金属粉末燃烧器可以为采矿车、电站等提供热能,其转化过程如图二:
(1)、写出图一中仪器a的名称。(2)、实验室用加热高锰酸钾固体的方法制取氧气,选择的发生装置是(填字母序字号),加热时,应使用酒精灯的焰集中加热;检验氧气可用。(3)、实验室制取CO2应选择的发生和收集装置是(填字母序号),其反应的化学方程式为。(4)、镁粉在火星上可以扮演地球上煤的角色,通过采用Mg/CO2金属粉末燃烧器可以为采矿车、电站等提供热能,其转化过程如图二:已知:燃烧器中发生的主要反应为
①热气中一定含有的物质有(写一种即可)。
②通过上述反应,你对燃烧条件的新认识是。
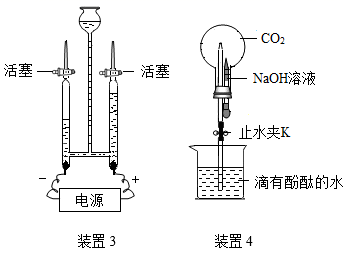
29. 实验是科学探究的重要方式,请结合图示回答下列问题: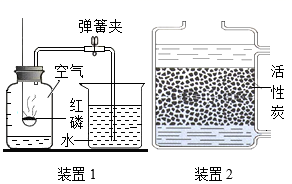
 (1)、装置1常用于实验室测定空气中氧气含量。请写出红磷燃烧的化学方程式。(2)、装置2中的活性炭有性,可用于净化水;常用区别硬水和软水,生活中常用的方法降低水的硬度。(3)、装置3常用于实验室电解水,与电源正极相连的玻璃管中收集的气体是;此实验可以证明水是由组成的。(4)、装置4可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开弹簧夹K。观察到的实验现象:形成美丽喷泉,写出该反应的化学方程式。30. 我国制碱工业先驱侯德榜发明了“侯氏制碱法”,为纯碱和氮肥工业技术的发展作出了杰出的贡献。纯碱的用途非常广泛,某化学兴趣小组的同学对它产生了浓厚的兴趣,设计了如下两个实验,并对反应后试管中残留废液进行探究。
(1)、装置1常用于实验室测定空气中氧气含量。请写出红磷燃烧的化学方程式。(2)、装置2中的活性炭有性,可用于净化水;常用区别硬水和软水,生活中常用的方法降低水的硬度。(3)、装置3常用于实验室电解水,与电源正极相连的玻璃管中收集的气体是;此实验可以证明水是由组成的。(4)、装置4可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开弹簧夹K。观察到的实验现象:形成美丽喷泉,写出该反应的化学方程式。30. 我国制碱工业先驱侯德榜发明了“侯氏制碱法”,为纯碱和氮肥工业技术的发展作出了杰出的贡献。纯碱的用途非常广泛,某化学兴趣小组的同学对它产生了浓厚的兴趣,设计了如下两个实验,并对反应后试管中残留废液进行探究。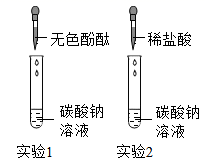 (1)、(实验1)往一支盛有碳酸钠溶液的试管中滴加无色酚酞溶液,观察到溶液变成色。
(1)、(实验1)往一支盛有碳酸钠溶液的试管中滴加无色酚酞溶液,观察到溶液变成色。(实验2)往另一支盛有碳酸钠溶液的试管中滴加稀盐酸,观察到的现象是。同学们对实验2反应后的废液中溶质成分进行探究。
(2)、(提出问题)废液中所含溶质是什么?(作出猜想)猜想一:废液中的溶质可能是NaCl、HCl
猜想二:废液中的溶质可能是NaCl、Na2CO3
猜想三:废液中的溶质可能是。
(3)、(设计实验)同学们为验证猜想,设计了如下实验:方案一:
实验操作与现象
反应方程式
实验结论
小芳取少量废液于试管中,滴加澄清石灰水,有白色沉淀产生
猜想二正确
(4)、方案二:小明取少量废液于试管中,滴加几滴无色酚酞溶液,发现溶液不变红色,小明认为猜想一正确。(进行讨论)同学们一致认为小明的实验结论不正确,理由是。
(5)、(进行总结)分析反应后溶液中溶质成分,除要考虑生成物外,还需考虑。(6)、(拓展与应用)现有14.9克纯碱样品(含Na2CO3和NaCl的混合物),将其放入干净的烧杯中,加入89.5克水使其完全溶解,向所得溶液中缓慢加入一定溶质质量分数的稀盐酸(反应方程式为: )。产生气体的质量与加入稀盐酸的质量关系如图所示,试回答下列问题:
①产生CO2的质量为克。
②所用稀盐酸中溶质的质量分数是多少?(写出具体的解题过程,下同)
③滴入稀盐酸至恰好完全反应时,所得溶液中溶质的质量分数是多少?