湖北省黄石市2021年中考化学试卷
试卷更新日期:2021-07-02 类型:中考真卷
一、单选题
-
1. 下列诗句中不涉及化学变化的是( )A、千锤万凿出深山 B、化作春泥更护花 C、蜡炬成灰泪始干 D、爆竹声中一岁除2. 化学与我们的生活息息相关下列说法错误的是( )A、缺钙会导致骨质疏松 B、贫血的人补充的铁越多越好 C、人体所需的热量主要来自糖类 D、吃水果蔬菜可以补充维生素3. 下列物质按照混合物、碱、氧化物顺序排列的是( )A、冰水混合物、苛性钠、二氧化锰 B、液化石油气、熟石灰、二氧化硫 C、食盐水、纯碱、干冰 D、天然气、氢氧化钾、大理石4. 下列有关化学用语的说法正确的是( )A、2N2表示4个氮原子 B、Cl-中的“-”表示氯元素的化合价为-1价 C、 表示一个碳酸根 D、H既可以表示氢元素,也可以表示一个氢原子5. 下列有关空气的说法错误的是( )A、氮气是制造氮肥的重要原料 B、氧气约占空气体积的21% C、空气中稀有气体所占比例虽小但用途广泛 D、空气污染不会造成臭氧层空洞6. 下列反应的化学方程式书写正确的是( )A、高炉炼铁: B、盐酸除铁锈: C、小苏打治疗胃酸过多: D、铝制品耐腐蚀:7. 下列对宏观事实的解释错误的是( )A、品红在热水中扩散的更快—温度升高,分子运动加快 B、铁在空气中只发生红热现象,在氧气中剧烈燃烧—氧气含量不同 C、一氧化碳和二氧化碳化学性质不同—原子种类不同,性质不同 D、明矾可以净水—生成的胶状物能吸附杂质8. 将足量X、Y、Z、M四种金属分别投入等质量、等质量分数的稀盐酸中(反应关系如图甲),把金属Y、Z分别投入硝酸银溶液中(反应关系如图乙),据此判断X、Y、Z、M的金属活动性顺序是( )
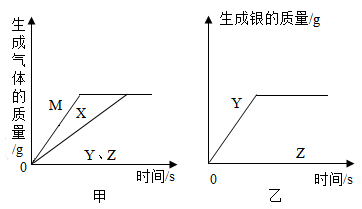 A、M>X>Y>Z B、M>X>Z>Y C、X>M>Z>Y D、X>M>Y>Z9. 思维导图是知识整理的重要工具,如图是某思维导图的一部分,可以填入括号中的是( )
A、M>X>Y>Z B、M>X>Z>Y C、X>M>Z>Y D、X>M>Y>Z9. 思维导图是知识整理的重要工具,如图是某思维导图的一部分,可以填入括号中的是( ) A、能与活泼非金属反应 B、能与某些酸反应 C、能与非金属氧化物反应 D、能与某些盐反应10. 下列实验操作正确的是( )A、
A、能与活泼非金属反应 B、能与某些酸反应 C、能与非金属氧化物反应 D、能与某些盐反应10. 下列实验操作正确的是( )A、 浓硫酸稀释
B、
浓硫酸稀释
B、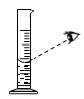 液体读数
C、
液体读数
C、 收集氢气
D、
收集氢气
D、 熄灭酒精灯
11. 下列常见物质的除杂方法错误的是( )
熄灭酒精灯
11. 下列常见物质的除杂方法错误的是( )选项
物质
杂质
所用方法
A
二氧化碳
一氧化碳
通过灼热的氧化铜
B
氯化钠
硝酸钾
加水溶解,蒸发结晶
C
氯酸钾
氯化钾
加水溶解,过滤
D
氧化钙
碳酸钙
高温煅烧
A、A B、B C、C D、D12. “归纳推理”是化学学习过程中常用的思维方法,以下类推结果正确的是( )A、单质是由同种元素组成,则由同种元素组成的物质都是单质 B、碳酸钙能与盐酸反应生成二氧化碳,则碳酸钠也能与盐酸反应生成二氧化碳 C、石墨能够导电,则由碳元素组成的金刚石也能导电 D、堆放杂物的纸箱着火可用水浇灭,则所有物质着火都可用水浇灭二、综合题
-
13. 阅读材料,回答下列问题。
绿色环保汽车
2021年两会期间,我国提出2030年前实现“碳达峰”,2060年前实现“碳中和”。目前汽车普遍使用的燃料是汽油和煤油,不仅产生大量二氧化碳,还因燃烧不充分释放了一氧化碳、颗粒物以及氮氧化物等有害物质,既造成资源浪费,污染环境。开发能够取代汽油的新能源,生产和使用环保型、零污染的绿色汽车是实现“碳中和”的有效措施。
发展绿色环保汽车,主要有以下途径:
一是改进现有车型:采用铝合金、钛合金、塑料等轻量化材料,为汽车“减肥”,从而降低然油消耗;改进发动机的燃烧方式,使汽油能充分燃烧;使用催化净化装置,将尾气中的有害物质转化为无害物质再排放等。二是开发汽车代用燃料,主要包括天然气、乙醇、生物柴油、氢气等,实现能源多元化。三是大力发展电动汽车。电动汽车具有效率高,在使用地点“零排放”的特点,尤其是氢燃料电池汽车,受到人们的广泛关注。开发利用电动汽车已成为发展绿色环保汽车的重要途径。
(1)、汽车尾气中的(A 一氧化碳 B 氮氧化物)会造成酸雨。(2)、铝合金的硬度一般比纯铝的硬度(A 大 B 小)。(3)、属于可再生能源的是(A 天然气 B 乙醇)。(4)、属于有机合成材料的是(A 生物柴油 B 塑料)。(5)、氢气被认为是最理想的清洁燃料的原因是。14. 溶液在生产、生活中起着十分重要的作用。请回答(1)-(2)题。(1)、如图,在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水进搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是。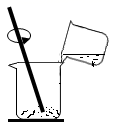
A 、氯化钠 B 、硝酸铵 C 、氢氧化钠 D、 蔗糖
(2)、用汽油或加了洗涤剂的水都能除去衣服上的油污,两者去油污的原理分别是。A 、乳化、乳化 B 、乳化、溶解 C、 溶解、乳化 D、 溶解、溶解
如图是甲、乙、丙三种固体物质的溶解度曲线。请回答(3)(4)题。
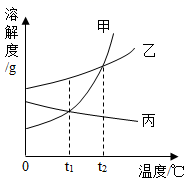 (3)、现有t1℃时甲乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是。
(3)、现有t1℃时甲乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是。A 、甲=乙>丙 B、 乙>甲=丙 C、 乙>甲>丙 D 、甲>乙>丙
(4)、为了将近饱和的丙溶液变为饱和溶液,可采用的方法有(有2-3个选项正确)。A、 加固体丙 B 、加水 C 、降低温度 D 、蒸发浓缩
15. 单质硫、硫化氢燃烧时会生成同种有毒的气体。请回答下列问题。(1)、如图是硫原子的结构示意图,其中x= , 在化学反应中该原子容易(“得到”或“失去”)电子。
硫化氢在空气中燃烧的微观示意图如下:
 (2)、硫化氢中硫元素的化合价是。(3)、生成的有毒气体中各元素的质量比为。(4)、写出上述反应的化学方程式。16. 下图是实验室常用的实验装置,请回答下列问题。
(2)、硫化氢中硫元素的化合价是。(3)、生成的有毒气体中各元素的质量比为。(4)、写出上述反应的化学方程式。16. 下图是实验室常用的实验装置,请回答下列问题。 (1)、图中仪器a的名称为。(2)、若用装置B制取氧气,相应反应的化学方程式为 , 若用此法制备并收集干燥的氧气,则装置的连接顺序为B→→。(3)、实验室用装置A、F进行碳还原氧化铜的实验,为了检验反应的产物,装置F中应盛放的试剂是 , 反应过程中该装置内的现象为。17. 某班同学在做“某些酸、碱、盐之间是否发生反应”的探究实验时发现,酸碱之间的反应,往往没有明显的现象。那么如何判断酸碱发生了化学反应呢?
(1)、图中仪器a的名称为。(2)、若用装置B制取氧气,相应反应的化学方程式为 , 若用此法制备并收集干燥的氧气,则装置的连接顺序为B→→。(3)、实验室用装置A、F进行碳还原氧化铜的实验,为了检验反应的产物,装置F中应盛放的试剂是 , 反应过程中该装置内的现象为。17. 某班同学在做“某些酸、碱、盐之间是否发生反应”的探究实验时发现,酸碱之间的反应,往往没有明显的现象。那么如何判断酸碱发生了化学反应呢?(提出问题)如何判断酸、碱溶液发生了化学反应?
(实验药品)一定质量分数的稀盐酸、一定质量分数的氢氧化钠溶液(稀)、酚酞溶液、蒸馏水
(1)、(实验探究)甲小组在烧杯中加入50mL氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入稀盐酸,发现(填现象),证明氢氧化钠溶液与稀盐酸发生了化学反应,该反应的化学方程式为。
(2)、乙小组进行了以下三个实验,并用温度传感器测定实验过程中的温度变化情况,得到了如下图所示的三条曲线。

实验1:50mL稀盐酸与50mL氢氧化钠溶液混合(曲线a);
实验2:50mL稀盐酸与50mL蒸馏水混合(曲线b);
实验3:50mL氢氧化钠溶液与50mL蒸馏水混合(曲线c)。
结合实验目的分析,增加实验2、实验3的目的是。
对比三条曲线,可以得到如下结论:①氢氧化钠溶液和稀盐酸一定发生了化学反应。②酸碱中和反应是反应(填“放热”或“吸热”)。
(3)、(交流与反思)甲小组认为,通过实验探究(2)得出“中和反应是放热反应”的结论不严谨,应该补充实验。
18. 以黄铜矿(主要成分为CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,同时还可以获得绿矾(FeSO4﹒7H2O),流程如下: (1)、步骤①中的化学方程式: 。(2)、步骤②中的反应有两个:反应一是 ,该反应属于(填基本反应类型),反应二的化学方程式为。(3)、加入的A是(填化学式)。(4)、获得绿矾的“一系列操作”为:蒸发浓缩、、过滤等。
(1)、步骤①中的化学方程式: 。(2)、步骤②中的反应有两个:反应一是 ,该反应属于(填基本反应类型),反应二的化学方程式为。(3)、加入的A是(填化学式)。(4)、获得绿矾的“一系列操作”为:蒸发浓缩、、过滤等。三、计算题
-
19. 取一氧化碳还原氧化铜实验的固体残留物20g,向其中加入稀硫酸,剩余固体质量与加入稀硫酸质量关系如图所示,请回答下列问题。
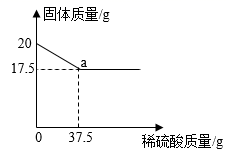 (1)、所取固体残留物中铜的质量为g。(2)、求a点处溶液中溶质的质量分数(写出计算过程)。
(1)、所取固体残留物中铜的质量为g。(2)、求a点处溶液中溶质的质量分数(写出计算过程)。