浙教版科学九年级上册第2章5.6节同步训练
试卷更新日期:2021-06-29 类型:同步测试
一、单选题
-
1. 某同学对Fe2O3做了如图探究活动,已知氯气在水溶液中能将Fe2+转变为Fe3+ , 且每一步都充分反应。下列分析正确的是( )
 A、无色气体可以使澄清石灰水变浑浊 B、黑色粉末是Fe3O4 C、①过程Fe2O3中的氧元素全部转人无色气体 D、②过程有置换反应发生2. 物质X、Y之间存在如下关系:X+2NaOH=2Y+Cu(OH)2↓,则( )A、X一定是Cu(NO3)2 B、X的式量比Y大 C、Y中阴离子的化合价为-2 D、该反应类型为置换反应3.
A、无色气体可以使澄清石灰水变浑浊 B、黑色粉末是Fe3O4 C、①过程Fe2O3中的氧元素全部转人无色气体 D、②过程有置换反应发生2. 物质X、Y之间存在如下关系:X+2NaOH=2Y+Cu(OH)2↓,则( )A、X一定是Cu(NO3)2 B、X的式量比Y大 C、Y中阴离子的化合价为-2 D、该反应类型为置换反应3.现有铁、氧化铁、稀硫酸、氢氧化钙溶液、碳酸钠溶液等五种物质,存在着如图所示的相互反应或转化关系(图中“—”表示物质间可以发生化学反应,“→”表示物质间存在相应的转化关系)。下列判断合理的是( )
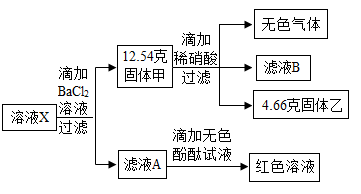
 A、丙可能是碳酸钠溶液 B、丁可能是氢氧化钙溶液 C、乙必须通过置换反应转化为铁 D、甲和丁的反应一定是中和反应4. 某固体混合物成分是由 Na+、Ba2+、Cu2+、Cl-、 、 、 中的几种离子构成,取一定质量的该固体混合物样品,进行如下实验:
A、丙可能是碳酸钠溶液 B、丁可能是氢氧化钙溶液 C、乙必须通过置换反应转化为铁 D、甲和丁的反应一定是中和反应4. 某固体混合物成分是由 Na+、Ba2+、Cu2+、Cl-、 、 、 中的几种离子构成,取一定质量的该固体混合物样品,进行如下实验:①将固体样品溶于水得无色透明溶液,加入足量 BaCl2 溶液过滤,得到白色沉淀和无色滤液。
②在①所得的白色沉淀中加入过量稀硝酸,白色沉淀部分溶解并产生气泡。
③在①所得的无色滤液中滴加 AgNO3溶液产生白色沉淀。
由此推断该固体中一定含有的离子是( )
A、Na+、 、 B、Na+、 、 、Cl- C、Ba2+、 、 、 Cl- D、Ba2+、Cu2+、 、5. 在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( )A、滤渣中一定有银、没有铜和锌 B、滤渣中一定有银和锌,可能有铜 C、滤液中一定有硝酸锌、硝酸铜、硝酸银 D、滤液中一定有硝酸锌、硝酸铜,可能有硝酸银6. 某废液中只含有Fe(NO3)2、Cu(NO3)2、Ba(NO3)2三种溶质。为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量)。下列判断不正确的是( ) A、向固体a中滴加过量的盐酸,实验现象为固体部分溶解,产生气泡,溶液呈浅绿色 B、溶液B中含有的盐是Ba(NO3)2和NaNO3 C、X可能是Na2SO4 D、若回收到6.4g固体a,则加入的铁屑质量为5.6g7. 某同学实验时,用氢气还原16g氧化铜,反应一段时间后,停止加热,冷却后称量剩余固体质量为14.4g,则下列结论正确的是( )A、有1.6g水生成 B、有1.4g铜生成 C、实际用去氢气的质量大于0.2g D、有80%的氧化铜参加反应8. 某混合气体可能含有CO、CO2、CH4和HCl中的一种或几种,为了确定其成分,将混合气体按如图所示装置进行实验(假设各步均充分反应或吸收),结果装置A中的石灰水不变浑浊,但混合气体的体积明显减小;装置D增重1.8g;装置E增重2.4g,下列分析正确的是( )
A、向固体a中滴加过量的盐酸,实验现象为固体部分溶解,产生气泡,溶液呈浅绿色 B、溶液B中含有的盐是Ba(NO3)2和NaNO3 C、X可能是Na2SO4 D、若回收到6.4g固体a,则加入的铁屑质量为5.6g7. 某同学实验时,用氢气还原16g氧化铜,反应一段时间后,停止加热,冷却后称量剩余固体质量为14.4g,则下列结论正确的是( )A、有1.6g水生成 B、有1.4g铜生成 C、实际用去氢气的质量大于0.2g D、有80%的氧化铜参加反应8. 某混合气体可能含有CO、CO2、CH4和HCl中的一种或几种,为了确定其成分,将混合气体按如图所示装置进行实验(假设各步均充分反应或吸收),结果装置A中的石灰水不变浑浊,但混合气体的体积明显减小;装置D增重1.8g;装置E增重2.4g,下列分析正确的是( ) A、装置A中石灰水不变浑浊,所以气体中一定不含二氧化碳 B、装置C对实验结果不产生影响,所以可以去掉装置C以简化实验方案 C、后续装置的目的是阻止空气中的二氧化碳进入装置E中,干扰CO的检验 D、该混合气体成分可能是CH4 和CO9. 向100g质量分数分别为14.6%HCl和12%MgSO4的混合溶液中,滴加Ba(OH)2溶液至过量.下列图象中,产生的沉淀量与滴入Ba(OH)2相符的是( )A、
A、装置A中石灰水不变浑浊,所以气体中一定不含二氧化碳 B、装置C对实验结果不产生影响,所以可以去掉装置C以简化实验方案 C、后续装置的目的是阻止空气中的二氧化碳进入装置E中,干扰CO的检验 D、该混合气体成分可能是CH4 和CO9. 向100g质量分数分别为14.6%HCl和12%MgSO4的混合溶液中,滴加Ba(OH)2溶液至过量.下列图象中,产生的沉淀量与滴入Ba(OH)2相符的是( )A、 B、
B、 C、
C、 D、
D、 10. 下列各组物质的溶液,不另加试剂就能鉴别出来的一组是( )A、Na2CO3、HCl、H2SO4 B、KCl、NaCl、Na2SO4 C、FeCl3、NaOH、KNO3 D、HCl、NaOH、Ca(OH)211. 如图所示,已知甲是含两种或两种以上初中科学常见盐的黄色溶液,乙为NaNO3溶液。为探究甲的组成,同学们按如图所示进行了探究(每步加的试剂都是过量的)。下列推断中不正确的是( )
10. 下列各组物质的溶液,不另加试剂就能鉴别出来的一组是( )A、Na2CO3、HCl、H2SO4 B、KCl、NaCl、Na2SO4 C、FeCl3、NaOH、KNO3 D、HCl、NaOH、Ca(OH)211. 如图所示,已知甲是含两种或两种以上初中科学常见盐的黄色溶液,乙为NaNO3溶液。为探究甲的组成,同学们按如图所示进行了探究(每步加的试剂都是过量的)。下列推断中不正确的是( )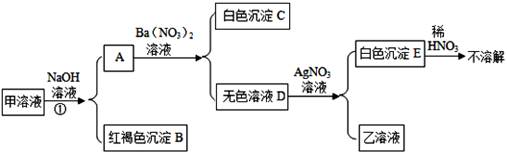 A、①一定不是氧化还原反应 B、甲中溶质不一定是FeCl3和Na2SO4 C、C可能是碳酸钡 D、E一定是氯化银12. 一包混有杂质的Na2CO3 , 其杂质可能是Ba(NO3)2、KCl、NaHCO3一种或几种,今取10.6g样品,溶于水得澄清溶液,另取5.3克样品,加入足量的盐酸,收集到2gCO2 , 则下列判断正确的是( )A、样品中只含有NaHCO3 B、样品中一定混有NaHCO3 , 可能有KCl C、样品中有NaHCO3 , 也有Ba(NO3)2 D、样品中混有KCl,也可能有NaHCO313. C,H2 , CO都具有可燃性和还原性.如果C,H2 , CO以一定的质量比分别跟等质量的O2恰好完全应生成CO2或H2O,则C,H2 , CO以同样的质量比分别跟足量的CuO完全反应时,所对应消耗的CuO的质量比为( )A、2:1:1 B、1:2:l C、1:l:2 D、1:1:114.
A、①一定不是氧化还原反应 B、甲中溶质不一定是FeCl3和Na2SO4 C、C可能是碳酸钡 D、E一定是氯化银12. 一包混有杂质的Na2CO3 , 其杂质可能是Ba(NO3)2、KCl、NaHCO3一种或几种,今取10.6g样品,溶于水得澄清溶液,另取5.3克样品,加入足量的盐酸,收集到2gCO2 , 则下列判断正确的是( )A、样品中只含有NaHCO3 B、样品中一定混有NaHCO3 , 可能有KCl C、样品中有NaHCO3 , 也有Ba(NO3)2 D、样品中混有KCl,也可能有NaHCO313. C,H2 , CO都具有可燃性和还原性.如果C,H2 , CO以一定的质量比分别跟等质量的O2恰好完全应生成CO2或H2O,则C,H2 , CO以同样的质量比分别跟足量的CuO完全反应时,所对应消耗的CuO的质量比为( )A、2:1:1 B、1:2:l C、1:l:2 D、1:1:114.实验室里,用如图装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法不正确的是( )
 A、实验开始时,应该先点燃酒精灯,一段时间后再通入一氧化碳 B、实验过程中,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 C、实验结束后,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁 D、为了减少空气污染,需要增加尾气处理装置15. 某同学为研究相同条件下一氧化碳和氢气哪个还原氧化铁的量更多,将一氧化碳和氢气等体积混合后先通过图甲装置,再通过图乙中的仪器组合。为达到实验目的,图乙中仪器选择和连接最好的是( )
A、实验开始时,应该先点燃酒精灯,一段时间后再通入一氧化碳 B、实验过程中,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成 C、实验结束后,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁 D、为了减少空气污染,需要增加尾气处理装置15. 某同学为研究相同条件下一氧化碳和氢气哪个还原氧化铁的量更多,将一氧化碳和氢气等体积混合后先通过图甲装置,再通过图乙中的仪器组合。为达到实验目的,图乙中仪器选择和连接最好的是( )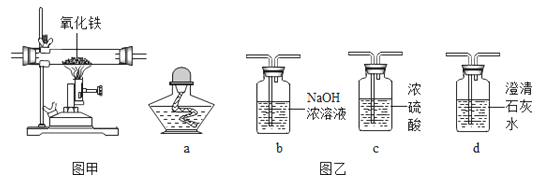 A、cba B、cda C、cbd D、bca16.
A、cba B、cda C、cbd D、bca16.小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
 A、HCl NaOH BaCl2 Na2SO4 B、HCl Ba(OH)2 Na2SO4 BaCl2 C、H2SO4 Ba(OH)2 Na2SO4 BaCl2 D、H2SO4 NaOH BaCl2 Na2SO417. 有一包粉末可能由CaCO3、Na2SO4、KNO3、CuSO4、BaCl2中的一种或几种组成,做实验得到以下结果:①将此固体粉末加入到水中,得到白色沉淀,且上层清液为无色;②该白色沉淀部分溶于稀硝酸,且有无色气体产生。据此实验,下列判断正确的是( )A、该粉末中一定含有CaCO3、Na2SO4、BaCl2 B、该粉末中一定不含有KNO3、CuSO4 C、该粉末中一定含有KNO3 D、该粉末中一定含有Na2SO4、KNO3、BaCl218.
A、HCl NaOH BaCl2 Na2SO4 B、HCl Ba(OH)2 Na2SO4 BaCl2 C、H2SO4 Ba(OH)2 Na2SO4 BaCl2 D、H2SO4 NaOH BaCl2 Na2SO417. 有一包粉末可能由CaCO3、Na2SO4、KNO3、CuSO4、BaCl2中的一种或几种组成,做实验得到以下结果:①将此固体粉末加入到水中,得到白色沉淀,且上层清液为无色;②该白色沉淀部分溶于稀硝酸,且有无色气体产生。据此实验,下列判断正确的是( )A、该粉末中一定含有CaCO3、Na2SO4、BaCl2 B、该粉末中一定不含有KNO3、CuSO4 C、该粉末中一定含有KNO3 D、该粉末中一定含有Na2SO4、KNO3、BaCl218.甲、乙、丙、丁是初中化学常见的物质,常温下,它们具有如图所示关系.“﹣”表示连接的两种物质能反应,“→”表示物质转化的方向,下列推断错误的是( )
 A、若甲是HCl,则丁可能是CaCl2 B、若甲是HCl,则乙和丙中可能有一个为碱 C、若甲是Ca(OH)2 , 则丁可能是NaOH D、若甲是Ca(OH)2 , 则乙和丙中至少有一个为酸19. 某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取mg该固体粉末按下列流程进行实验(本流程涉及到的反应均为初中化学常用的反应,且各步均恰好完全反应)。
A、若甲是HCl,则丁可能是CaCl2 B、若甲是HCl,则乙和丙中可能有一个为碱 C、若甲是Ca(OH)2 , 则丁可能是NaOH D、若甲是Ca(OH)2 , 则乙和丙中至少有一个为酸19. 某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取mg该固体粉末按下列流程进行实验(本流程涉及到的反应均为初中化学常用的反应,且各步均恰好完全反应)。
下列说法中正确的是( )
A、溶液N中只含一种溶质 B、原固体粉末中可能含有碳酸钙 C、白色沉淀Y一定是碳酸钙,气体W可能是氢气 D、原固体粉末中一定没有氧化铜,一定含有碳酸钙20. 通过海水晒得的粗盐,除NaCl外,还含有MgCl2、CaCl2等杂质,将粗盐按如图流程,可获得较纯净的氯化钠,以备工业生产所需。在此过程中,a、b物质分别为() A、NaOH、K2CO3 B、Ca(OH)2、Na2CO3 C、KOH、K2CO3 D、KOH、Na2CO3
A、NaOH、K2CO3 B、Ca(OH)2、Na2CO3 C、KOH、K2CO3 D、KOH、Na2CO3二、填空题
-
21. 学习了物质推断专题内容后,科学研究小组同学设计了如下实验方案进行探究。步骤如下:
①往镁粉和氧化铜的混合物中加入过量稀硫酸,充分反应并过滤,得到滤渣甲和滤液A;
②往滴有无色酚酞的氢氧化钠和硝酸钡的混合溶液中,加入一定量的稀硫酸,充分反应并过滤,得到沉淀乙和无色滤液B;
③将滤液A和B充分混合后,得到沉淀丙和滤液C; ④往滤液C中滴加氯化钡溶液,没有沉淀产生。
回答下列问题:
(1)、步骤②中沉淀乙的化学式为;(2)、滤液C中除酚酞外,一定含有的溶质是。22. 有一包白色固体,可能由BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种组成。为确定其成分,实验小组进行实验。实验过程中所加试剂均足量,实验过程及现象如图所示。 (1)、白色沉淀A稀盐酸反应的化学反应方程式为 。
(1)、白色沉淀A稀盐酸反应的化学反应方程式为 。
(2)、白色沉淀C的化学式为。(3)、这包白色固体是由(填化学式)组成的。23.现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成。为确定其组成,进行了如下图所示的实验。

请回答:
(1)、若X溶液只含一种溶质,根据实验可以确定X溶液的溶质是 ;(2)、原固体粉末的所有可能组成是 。24. 一包不纯的氯化钾粉末,杂质可能是硫酸钠、氢氧化钠、氯化钠、硝酸钡中的一种或几种。为确定其成分,某兴趣小组的同学进行如下实验:实验一:取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得到无色澄清溶液,往溶液中通入CO2 , 产生白色沉淀。
实验二:取14.0g该粉末于烧杯中,加入蒸馏水完全溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后,产生28.7g白色沉淀。
请回答下列问题:
(1)、实验一中产生白色沉淀的化学式为 。(2)、根据上述两个实验可判断杂质中一定没有 , 一定有 。25. 如图所示,A是金属氧化物,B是一种金属单质,C是黄色溶液,D是浅绿色溶液,反应③是物质E与氧气、水发生的一个化合反应,请回答下列问题: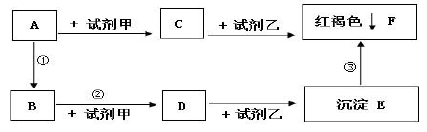 (1)、写出试剂甲可能的化学式:。(2)、试剂乙中一定含有的离子:。(3)、写出化学变化①和②的化学方程式:
(1)、写出试剂甲可能的化学式:。(2)、试剂乙中一定含有的离子:。(3)、写出化学变化①和②的化学方程式:① 。
② 。
26. 某溶液中可能含有氢氧化钠、碳酸钠、硫酸钠、氯化钠、硝酸钠中的一种或几种,小晨同学为测定其成分,进行如下实验。首先她取了一定样品,先后逐滴加入氯化钡溶液、稀硝酸。0~t1时刻表示加入的氯化钡过程;t1时刻之后表示加入的稀硝酸的过程,她将产生沉淀的质量与时间的关系绘制成了如图所示的图像。回答下列问题: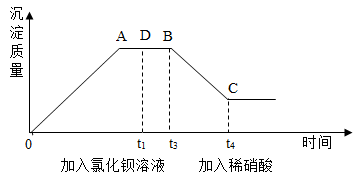 (1)、由上述实验可知,原溶液中一定含;(2)、BD之间(不包括B、D端点)对应的溶液中的一定存在的离子有;(用离子符号表示)
(1)、由上述实验可知,原溶液中一定含;(2)、BD之间(不包括B、D端点)对应的溶液中的一定存在的离子有;(用离子符号表示)三、实验探究题
-
27. 实验室有瓶标签残缺(如图)的试剂,实孩员告诉小明,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种.为确定试剂成分,小明进行如下实验:

步骤
实验操作
实验现象
①
取5毫升试剂于A试管中,滴入几滴无色酚酞试液
无色酚酞试液
②
另取5毫升试剂于B 试管中,滴入几滴氯化钡溶液
溶液中出现白色沉淀
(1)、根据步骤① 现象,小明得出了该试剂可能为氯化钠溶液或硫酸钠溶液。小明作出该判断的依据是步骤① 的实验现象是“无色酚酞试液 ”。
(2)、由步骤②可确定该试剂为 溶液。
28.硫燃烧产生的二氧化硫气体会造成空气污染。为避免二氧化硫污染空气,某教师对教材中“硫在空气和氧气中燃烧”的实验进行了改进与创新,设计了如图甲所示的实验装置:

【实验原理】
① B装置是燃烧匙固定在带有A导管的单塞上,硬质玻璃管透光性好,不影响实验现象的观察;
② C装置的广口瓶中盛放氢氧化钠溶液可吸收二氧化硫气体,避免污染;
③ 打开D装置中的阀门,气体就会从左向右依次进入装置。
【实验过程】
步骤一:将硫粉放在燃烧匙上,在空气中点燃后,迅速伸入硬质玻璃管内(如图B装置),打开阀门,观察硫在空气中燃烧的现象;
步骤二:将导管a伸入盛有氧气的集气瓶中(如图A装置),观察硫在氧气中燃烧的现象。
【交流讨论】
(1)、硫在空气中燃烧并发出 火焰,生成的SO2气体被氢氧化钠溶液吸收的反应原理是 (用化学方程式表示);(2)、气流能从左向右作定向流动的原因是 ;(3)、【拓展应用】
小丽同学认为,运用该装置设计原理,还能进行其它有毒气体的实验,同样能达到避免污染的目的。于是设计了图乙实验装置,用以完成“CO
还原氧化铜”实验。

图乙D装置在实验中除了形成气体定向流动外,还有的用途是 ;
(4)、实验时,小芳同学先打开止水夹K1和阀门,过一会儿再点燃酒精灯,她这样操作的目的是 。29.有一包固体粉末,可能含有氧化钙、氯化钠、碳酸钠、硫酸钠中的一种或几种。为确定其组成,小杨设计出实验方案,实验步骤及现象如下。请回答:
 (1)、写出步骤④中产生白色沉淀的化学方程式。(2)、根据实验中的现象,能否确定原固体粉末的组成?若能,请写出各成分的化学式;若不能,在原实验步骤的基础上,对上述方案中的试剂作一改进,并描述相应的实验现象及结论,以确定固体粉末的组成。 。30.
(1)、写出步骤④中产生白色沉淀的化学方程式。(2)、根据实验中的现象,能否确定原固体粉末的组成?若能,请写出各成分的化学式;若不能,在原实验步骤的基础上,对上述方案中的试剂作一改进,并描述相应的实验现象及结论,以确定固体粉末的组成。 。30.现有一包固体粉末,可能由碳酸钠、硫酸钠、碳酸钙和氯化钠中的一种或几种组成,某同学想确定其组成成分,按如图所示步骤进行了如下实验(各步骤中加入的试剂均为足量):

请回答:
(1)、固体粉末中肯定存在的物质是 , 用化学方程式表示白色沉淀部分溶解的原因;(2)、如何判断固体粉末中是否有“可能存在的物质”,简述实验操作步骤、现象和结论。31. 天然气作为燃料已进入千家万户。小聪在帮助父母烧菜时想到:天然气燃烧的产物是什么呢?带着这一问题,小聪和同学一起进行了如下的探究。 (1)、设计与实验:同学们设计了甲图装置(固定装置未画出),将天然气在氧气中点燃后得到的混合气体通过该装置进行实验。开始时应(填“先通气体”或“先加热”);加热过程中发现黑色CuO固体变红,澄清石灰水变浑浊。写出CuO固体变红的化学方程式。仅根据甲图装置出现的现象,写出混合气体所有的可能组成。(2)、评价与改进:小聪认为上述实验方案有缺陷,通过讨论,增加了乙图中的3个装置(固定装置未画出),对方案作了改进并进行实验:将混合气体先通过乙图中连接的装置后,再通入甲图装置。实验中部分现象如下:A装置质量增加,B装置中溶液不变浑浊,甲图装置中实验现象与(1)相同。
(1)、设计与实验:同学们设计了甲图装置(固定装置未画出),将天然气在氧气中点燃后得到的混合气体通过该装置进行实验。开始时应(填“先通气体”或“先加热”);加热过程中发现黑色CuO固体变红,澄清石灰水变浑浊。写出CuO固体变红的化学方程式。仅根据甲图装置出现的现象,写出混合气体所有的可能组成。(2)、评价与改进:小聪认为上述实验方案有缺陷,通过讨论,增加了乙图中的3个装置(固定装置未画出),对方案作了改进并进行实验:将混合气体先通过乙图中连接的装置后,再通入甲图装置。实验中部分现象如下:A装置质量增加,B装置中溶液不变浑浊,甲图装置中实验现象与(1)相同。
请你写出改进方案的装置连接顺序(装置不重复使用):混合气体→→甲图装置(填装置编号)
交流与讨论:通过对改进实验的现象分析,同学们得出了正确的结论。
32. 如图所示为气体X(纯净物)与氧化铜反应制取铜的实验装置。回答问题: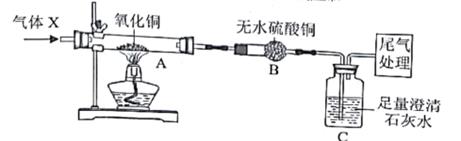 (1)、在对A中氧化铜进行加热前,需要先通一段时间的气体X,其目的是。(2)、若实验中,观察到A中黑色氧化铜粉末变红,B中无水硫酸铜无明显现象,C中澄清石灰水变浑浊,则通入的气体X为。(3)、查阅资料得知:①气体X与氧化铜反应除生成铜外还可能生成氧化亚铜(Cu2O) ;
(1)、在对A中氧化铜进行加热前,需要先通一段时间的气体X,其目的是。(2)、若实验中,观察到A中黑色氧化铜粉末变红,B中无水硫酸铜无明显现象,C中澄清石灰水变浑浊,则通入的气体X为。(3)、查阅资料得知:①气体X与氧化铜反应除生成铜外还可能生成氧化亚铜(Cu2O) ;②铜和氧化亚铜均为不溶于水的红色固体;③Cu2O+H2SO4=CuSO4+Cu+H2O
小乐为了探究反应所得红色固体的成分,进行了如下实验: .
实验操作
步骤一
取20g红色固体于烧杯中,加入足量稀硫酸
红色固体可能是氧化亚铜,也可能是铜和氧化亚铜
步骤二
将步骤一反应所得的混合物经过滤、洗涤、干燥并称量剩余红色固体质量
剩余红色固体质量为12g
20g红色固体中,铜和氧化亚铜的质量比为
四、解答题
-
33. 取敞口放置的氢氧化钠溶液于烧杯中,倒入一定量的稀硫酸充分反应。为探究反应后所得溶液X的成分,兴趣小组进行了如下实验(所加试剂均足量):
 (1)、过滤中玻璃棒的作用是 。(2)、产生的无色气体是 。(3)、溶液X的溶质是。(4)、计算滤液A中氯化钠的质量。34. 有一包白色粉末,可能含氯化钠、氢氧化钠、碳酸钠中的一种或几种。为了确定其组成,小明称取了9.3克粉末,向其中加入100克7.3%的稀盐酸充分反应,生成的二氧化碳气体完全逸出(忽略其他物质逸出),所得溶液的质量为107.1克。用pH试纸检测溶液呈中性。(1)、产生二氧化碳气体的化学反应方程式为。(2)、这包白色粉末的成分为。(3)、求所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)35. 小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验:
(1)、过滤中玻璃棒的作用是 。(2)、产生的无色气体是 。(3)、溶液X的溶质是。(4)、计算滤液A中氯化钠的质量。34. 有一包白色粉末,可能含氯化钠、氢氧化钠、碳酸钠中的一种或几种。为了确定其组成,小明称取了9.3克粉末,向其中加入100克7.3%的稀盐酸充分反应,生成的二氧化碳气体完全逸出(忽略其他物质逸出),所得溶液的质量为107.1克。用pH试纸检测溶液呈中性。(1)、产生二氧化碳气体的化学反应方程式为。(2)、这包白色粉末的成分为。(3)、求所得溶液中溶质的质量分数。(写出计算过程,结果保留一位小数)35. 小明取一包某食品包装袋内的“脱氧剂”,查阅资料发现其成分除铁粉外,可能含有碳粉、Na2CO3、NaCl、Fe2O3等。为确定其成分,进行了如下实验: (1)、过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有 。(2)、写出用pH试纸测定滤液pH的方法:。(3)、试剂X的名称是。36. 为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数进行如下实验:
(1)、过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有 。(2)、写出用pH试纸测定滤液pH的方法:。(3)、试剂X的名称是。36. 为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数进行如下实验:①取200g混合溶液加入足量的AgNO3溶液,经过滤洗涤、干燥、称量得到143.5gAgCl固体;
②另取原混合溶液各200与含有杂质的废铁用反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
实验组别
一
二
三
四
五
混合溶液质量/g
200
200
200
200
200
铁屑质量/g
6
9
12
15
18
析出铜的质量/g
6.4
9.6
m
16
16
请分析计算:
(1)、表中第三组实验的m值为。(2)、第组实验恰好完全反应。(3)、铁屑中铁的质量分数为多少?(计算结果精确到0.1%)(4)、原混合溶液中FeCl2的质量分数为多少?(计算结果精确到0.1%)37.小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系。已知A中氧元素的质量分数为60%,C、D、E、F均含有铜元素.请回答:
(1)“A+H2O=B”的反应属于基本反应类型中的 ;
(2)写出B和D反应得到C和水的化学方程式为 ;
(3)列举3种能与E反应得到F的物质 。
