江苏省连云港市2021年中考化学试卷
试卷更新日期:2021-06-25 类型:中考真卷
一、选择题(本题包括12小题,每小题2分,共24分。每小题只有一个选项符合题意)
-
1. 2021年5月15日“祝融号”火星车成功着陆。该车使用了新型镁锂合金,下列说法正确的是( )
 A、镁锂合金属于金属材料 B、锂属于非金属元素 C、镁是地壳中含量最高的金属元素 D、镁锂合金的硬度比镁的小2. 变化无处不在。生活中的下列现象是由化学变化引起的是( )A、湿衣晾干 B、铁锅生锈 C、小麦磨粉 D、滴水成冰3. 下氟在元素周期表中相关信息如图1所示,其原子在化学反应中容易得到1个电子达到相对稳定结构,两个氟原子构成一个氟气分子。在牙膏中添加氟化钠可降低患蛀牙的概率。钠原子的结构示意图如图2所示。
A、镁锂合金属于金属材料 B、锂属于非金属元素 C、镁是地壳中含量最高的金属元素 D、镁锂合金的硬度比镁的小2. 变化无处不在。生活中的下列现象是由化学变化引起的是( )A、湿衣晾干 B、铁锅生锈 C、小麦磨粉 D、滴水成冰3. 下氟在元素周期表中相关信息如图1所示,其原子在化学反应中容易得到1个电子达到相对稳定结构,两个氟原子构成一个氟气分子。在牙膏中添加氟化钠可降低患蛀牙的概率。钠原子的结构示意图如图2所示。列化学用语表示错误的是( )
 A、2个钠离子:2Na+ B、2个氟原子:F2 C、F-的结构示意图:
A、2个钠离子:2Na+ B、2个氟原子:F2 C、F-的结构示意图: D、氟化钠的化学式:NaF
4. 氟在元素周期表中相关信息如图1所示,其原子在化学反应中容易得到1个电子达到相对稳定结构,两个氟原子构成一个氟气分子。在牙膏中添加氟化钠可降低患蛀牙的概率。钠原子的结构示意图如图2所示。
D、氟化钠的化学式:NaF
4. 氟在元素周期表中相关信息如图1所示,其原子在化学反应中容易得到1个电子达到相对稳定结构,两个氟原子构成一个氟气分子。在牙膏中添加氟化钠可降低患蛀牙的概率。钠原子的结构示意图如图2所示。
下列说法正确的是( )
A、氟元素的相对原子质量为19.00g B、1个氟气分子中含有9个质子 C、钠原子在化学反应中易失去1个电子 D、F-和Na+的最外层电子数不相等5. 下列有关粗盐提纯实验中的相关装置和操作,正确的是( )A、溶解粗盐 
B、过滤食盐水
B、过滤食盐水 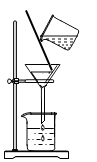
C、蒸发食盐水
C、蒸发食盐水 
D、冷却蒸发皿
D、冷却蒸发皿 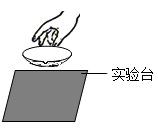
6. 空气是人类生产活动的重要资源。下列空气中各组分的性质与用途具有对应关系的是( )A、氧气无色无味可用于医疗急救吸氧 B、氮气化学性质不活泼,可用于制造硝酸 C、二氧化碳能与水反应,可用于制干冰 D、稀有气体在通电时能发出不同颜色的光,可用于制航标灯7. 化学就在我们身边。下列说法正确的是( )A、生活中常用煮沸的方法来降低水的硬度 B、霉变的大米、花生经蒸煮后可继续食用 C、铵态氮肥与熟石灰混合使用可以提高肥效 D、炒菜时油锅起火可放入菜叶灭火,原理是降低了油的着火点8. 化学是实验科学。下列实验方法能达到实验目的的是( )
6. 空气是人类生产活动的重要资源。下列空气中各组分的性质与用途具有对应关系的是( )A、氧气无色无味可用于医疗急救吸氧 B、氮气化学性质不活泼,可用于制造硝酸 C、二氧化碳能与水反应,可用于制干冰 D、稀有气体在通电时能发出不同颜色的光,可用于制航标灯7. 化学就在我们身边。下列说法正确的是( )A、生活中常用煮沸的方法来降低水的硬度 B、霉变的大米、花生经蒸煮后可继续食用 C、铵态氮肥与熟石灰混合使用可以提高肥效 D、炒菜时油锅起火可放入菜叶灭火,原理是降低了油的着火点8. 化学是实验科学。下列实验方法能达到实验目的的是( )选项
实验目的
实验方法
A
配制质量分数为5%的KNO3溶液
向盛有5.0gKNO3固体的烧杯中,加入100g水,搅拌
B
验证Al、Cu、Ag的金属活动性顺序
向CuSO4溶液和AgNO3溶液中各放入大小、形状相同的Al丝
c
检验氢气的纯度
用拇指堵住集满氢气的试管口,管口向下靠近火焰,移开拇指点火
D
鉴别CuSO4、BaSO4和CaCO3三种白色固体
分别取少量固体样品,加适量水,搅拌
A、A B、B C、C D、D9. NH3的合成开启了工业催化新纪元,为世界粮食增产做出了巨大贡献。以N2和H2为反应物合成NH3的微观过程如下:
下列说法正确的是( )
A、 表示氢气分子
B、过程中有“NH”“NH2”原子团生成
C、参加反应的H2与生成的NH3个数比为2:3
D、反应结束后催化剂的质量增加
10. 回收含铜废料(主要成分为Cu)中的铜,部分实验流程如下:
表示氢气分子
B、过程中有“NH”“NH2”原子团生成
C、参加反应的H2与生成的NH3个数比为2:3
D、反应结束后催化剂的质量增加
10. 回收含铜废料(主要成分为Cu)中的铜,部分实验流程如下:
注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。
下列关于该流程的说法,错误的是( )
A、“灼烧”的主要目的是将Cu转变为CuO B、滤液X中的溶质为FeSO4 C、“酸溶”和“还原”过程中发生的反应均为置换反应 D、将Cu、Fe混合物加入足量稀硫酸中,充分反应后过滤得Cu11. 向盛有等质量水的甲、乙、丙三个烧杯中分别加入15g、30g、30g蔗糖固体,充分搅拌后静置,现象如图所示。下列说法正确的是( ) A、可采用升温的方法使乙烧杯中剩余的固体溶解 B、甲、丙烧杯中的溶液一定属于不饱和溶液 C、乙、丙烧杯中溶质的质量分数相等 D、蔗糖的溶解度随温度的升高而减小12. 常温下,通过下列实验探究Ca(OH)2的性质:
A、可采用升温的方法使乙烧杯中剩余的固体溶解 B、甲、丙烧杯中的溶液一定属于不饱和溶液 C、乙、丙烧杯中溶质的质量分数相等 D、蔗糖的溶解度随温度的升高而减小12. 常温下,通过下列实验探究Ca(OH)2的性质:步骤一:向两支试管中分别加入0.2gCa(OH)2粉末,然后各加入2mL水,振荡后静置,试管底部有粉末,溶液呈无色。
步骤二:向两支试管中再各滴入2滴酚酞溶液,振荡后静置,溶液由无色变为红色,试管底部粉末无明显变化。
步骤三:继续向其中一支试管中加入2mL水,振荡后静置,无明显变化;向另一只试管中加入2mL稀盐酸,振荡后静置,溶液由红色变为无色,试管底部的粉末消失。
下列说法正确的是( )
A、步骤一说明常温下Ca(OH)2不溶于水 B、步骤二中溶液变红是因为Ca(OH)2在水溶液中解离出Ca2+ C、步骤三中消失的Ca(OH)2固体溶解在稀盐酸所含的水中 D、步骤三中溶液由红色变为无色的原因是二、非选择题(本题包括4小题,共36分)
-
13. “十四五”期间,我国将独立完成“天宫二号”空间实验室建造。(1)、运载火箭使用的燃料有液氢、煤油等。
①氢气目前还不能在生活和生产中大规模使用的原因之一是(填字母)。
a.制取成本高 b.产物无污染 c.燃烧热值高
②为使煤油充分燃烧,一是要有足够的氧气,二是。
(2)、长期驻留空间实验室会导致航天员肌肉萎缩、骨钙丢失。通过航天食品摄取优质蛋白质、补充钙元素有利于维持航天员的身体健康。①下列航天食品中富含蛋白质的是(填字母)。
a.脱水米饭 b.鱼香肉丝 c.冻干水果
②可在航天食品中添加(填字母)来补钙。
a.C12H22O14Ca b. FeC6H6O7 c.KIO3
(3)、舱段建造使用的新型铝基碳化硅复合材料是由颗粒状的铝和碳化硅(SiC)复合而成。①铝在空气中具有很好的抗腐蚀性能,原因是。
②制取SiC的反应为 。关于该反应说法正确的是(填字母)。
a.SiO2是由Si原子和O2分子构成 b.反应前后元素的化合价均未发生变化
c.反应后固体减少的质量等于生成的CO质量
14. 过氧乙酸(CH3 COOOH)作为一种消毒剂,在新冠防疫中发挥了重要作用。(1)、组成。下列关于过氧乙酸的说法,正确的是(填字母)。a.属于有机物 b.H、O原子个数比为2:1 c.碳元素的质量分数最大
(2)、变化。过氧乙酸不稳定,能分解为乙酸(CH3COOH)和氧气。写出该反应的化学方程式:。(3)、制备。实验室中用题37图-1所示装置制备过氧乙酸,反应原理为:①浓硫酸的作用是。
②该反应须控制在40℃左右进行,可用对三颈烧瓶进行加热。
 (4)、拓展。除过氧乙酸外, NaClO等含氯消毒剂也可有效灭活新冠病毒。利用题37图-2所示装置电解饱和NaCl溶液可制取少量NaClO消毒液。电解过程中,a极区生成Cl2 , b极区生成气体单质M和NaOH。
(4)、拓展。除过氧乙酸外, NaClO等含氯消毒剂也可有效灭活新冠病毒。利用题37图-2所示装置电解饱和NaCl溶液可制取少量NaClO消毒液。电解过程中,a极区生成Cl2 , b极区生成气体单质M和NaOH。①气体M具有可燃性,其化学式为。
②Cl2与NaOH反应生成NaClO、NaCl和H2O,该反应的化学方程式为。
15. 在钢铁工业推进碳减排、碳捕集的过程中,化学发挥了重要作用。(1)、“焦炭炼钢”是先将铁精矿(Fe2O3)和焦炭同时加入高炉,鼓入热空气,充分反应后得生铁,再将生铁转移至炼钢炉中炼制得钢。①高炉炼铁的主要反应原理是在高温下,夺取了Fe2O3里的氧,将铁还原出来。
②某钢铁厂每年需要向高炉中加入120万吨的焦炭,若加入的焦炭全部转化为CO2 , 则该钢铁厂每年排放CO2的质量为万吨。
(2)、为了实现CO2的捕集利用,我国研制出一种多功能复合催化剂(含NaFe3O4),能将CO2转化为汽油,转化步骤如下:① 步骤Ⅰ除生成CO外,还生成另一种氧化物。该氧化物的化学式是。
②下列说法错误的是(填字母)。
a.所得汽油中含有C、H两种元素 b.NaFe3O4中O为-2价,Fe为+3价
c.上述转化不仅有利于CO2减排,还可以减轻人类对化石能源的需求
(3)、一种以“氢能炼钢”替代“焦炭炼钢”的工艺流程如右图所示。
①高温下,用H2炼铁时反应的化学方程式为。
② 跟“焦炭炼钢”工艺相比,“氢能炼钢”的主要优点有。
③从物质组成的角度,说明向炼钢炉中加入废钢的目的:。
16. 碳酸氢钠是一种应用广泛的盐,化学小组对其进行了探究。(1)、NaHCO3可称为钠盐或碳酸氢盐,它是由Na+和(填离子符号)构成,医疗上能用于治疗胃酸(含有盐酸)过多症,反应的化学方程式为。(2)、【提出问题】实验室中如何制取少量 NaHCO3?【查阅资料】
材料一:侯氏制碱的原理: ;
。
材料二:研究发现, NaHCO3溶于水时吸收热量,Na2CO3溶于水时放出热量.
【实验制备】根据侯氏制碱原理设计如图-1所示装置制取 NaHCO3。

反应结束后,将试管中的混合物过滤,洗涤,低温烘干得白色固体。
烧杯中冰水的作用是。
(3)、能进一步确认该白色固体是NaHCO3的实验方案是(须用到的仪器和药品:试管、温度计、水)。(4)、图-2中碳酸氢钠的溶解度在60℃后无数据的原因可能是。(5)、【性质探究】常温下,取一定量的 NaHCO3溶液于烧杯中,插入pH传感器,向烧杯中持续滴加CaCl2溶液,有白色沉淀生成,当溶液的pH变为6.68时开始有无色气体产生。反应过程中溶液的pH随时间变化如图-3所示。

【查阅资料】
材料三: NaHCO3溶于水后,少量的HCO3-能同时发生如下变化:
变化①: ;
变化②: 。
材料四:溶液的酸碱性与溶液中H+和OH-数目的相对大小有关。
常温下,当单位体积溶液中OH-的数目大于H+的数目时,溶液的pH>7,反之pH<7;
单位体积溶液中所含的H数目越大溶液的pH越小。
【交流反思】
NaHCO3溶液显(填“酸”“碱”或“中”)性结合材料三、四从微观角度说明原因:。
(6)、根据本实验,下列说法错误的是(填字母)。a.pH<6.68时生成的无色气体为CO2
b.从0-30s,单位体积溶液中H+数目不断增大
c.不能用CaCl2溶液鉴别Na2CO3和 NaHCO3溶液