广东省深圳市龙岗区2021年中考化学二模试卷
试卷更新日期:2021-06-25 类型:中考模拟
一、单选题
-
1. 实验仪器们展开了热烈的讨论,其中发生了化学变化的是( )A、玻璃棒:“我被摔成了两段。 ” B、蒸发皿:“看!食盐水冷却析出了晶体。 C、铁架台:“好难受啊! 我在潮湿的空气中生锈了。” D、酒精灯:“帽子哪里去了? 我的燃料跑掉了。”2. 下列化学实验操作正确的是( )A、塞紧橡皮塞
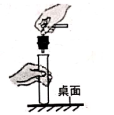 B、过滤
B、过滤  C、测定溶液的pH
C、测定溶液的pH  D、氧气验满
D、氧气验满  3. 搞怪化学衫、创意元素钟表等也有化学用语,以下分析正确的是( )A、
3. 搞怪化学衫、创意元素钟表等也有化学用语,以下分析正确的是( )A、 衬衫1的“2Fe"表示:两个铁离子
B、
衬衫1的“2Fe"表示:两个铁离子
B、 创意钟表里全是非金属元素
C、
创意钟表里全是非金属元素
C、 衬衫2表示的化学方程式:Mg+ZnSO4= MgSO4+Zn
D、
衬衫2表示的化学方程式:Mg+ZnSO4= MgSO4+Zn
D、 图4对应的微粒符号:Na+
4. 下列有关化学现象的描述,其中正确的是( )A、向FeCl3溶液中滴加NaOH溶液,生成红褐色沉淀 B、打开盛放浓H2SO4的试剂瓶瓶塞,瓶口出现大量白雾 C、硫磺在空气中燃烧,发出淡蓝色火焰,生成SO2气体 D、电解水时,电极上产生气泡,正、负极气体体积比约为2:15. 下列对化学基本观念的认识错误的是( )A、分类观:冰水混合物和于冰都属于纯净物 B、转化观:CO和CO2一定条件下可以相互转化 C、能量观:燃烧属于剧烈氧化,放热;食物腐败属于缓慢氧化,吸热 D、结构观:金刚石、石墨、C60物理性质差异大是因为碳原子的排列方式不同6. 甲酸(CH2O2)具有清洁制氢的巨大潜力,其反应微观示意图如图。说法正确的是( )
图4对应的微粒符号:Na+
4. 下列有关化学现象的描述,其中正确的是( )A、向FeCl3溶液中滴加NaOH溶液,生成红褐色沉淀 B、打开盛放浓H2SO4的试剂瓶瓶塞,瓶口出现大量白雾 C、硫磺在空气中燃烧,发出淡蓝色火焰,生成SO2气体 D、电解水时,电极上产生气泡,正、负极气体体积比约为2:15. 下列对化学基本观念的认识错误的是( )A、分类观:冰水混合物和于冰都属于纯净物 B、转化观:CO和CO2一定条件下可以相互转化 C、能量观:燃烧属于剧烈氧化,放热;食物腐败属于缓慢氧化,吸热 D、结构观:金刚石、石墨、C60物理性质差异大是因为碳原子的排列方式不同6. 甲酸(CH2O2)具有清洁制氢的巨大潜力,其反应微观示意图如图。说法正确的是( ) A、甲酸属于氧化物、有机物 B、甲酸由5个原子构成 C、甲酸中含有1个H2分子 D、生成甲、乙的质量比为1:227. 甲、乙两种固体物质(不含结晶水)在水中的溶解度曲线如图,下列说法正确的是( )
A、甲酸属于氧化物、有机物 B、甲酸由5个原子构成 C、甲酸中含有1个H2分子 D、生成甲、乙的质量比为1:227. 甲、乙两种固体物质(不含结晶水)在水中的溶解度曲线如图,下列说法正确的是( ) A、甲物质的溶解度大于乙物质 B、在t1℃时,甲、乙饱和溶液的溶质质量分数相等 C、t2℃时,100g甲饱和溶液中含有25g甲物质 D、降温或恒温蒸发溶剂均可使乙饱和溶液析出晶体8. 下列归纳总结完全正确的一组是( )
A、甲物质的溶解度大于乙物质 B、在t1℃时,甲、乙饱和溶液的溶质质量分数相等 C、t2℃时,100g甲饱和溶液中含有25g甲物质 D、降温或恒温蒸发溶剂均可使乙饱和溶液析出晶体8. 下列归纳总结完全正确的一组是( )A.化学与生活
B.化学与农业
①焙制糕点可加适量NaHCO3
②用洗涤剂清洗油污属于乳化作用
①在铁桶中配制农药波尔多液
②熟石灰与NH4Cl混合施用,增强肥效
C.化学与安全
D.化学与环境
①聚氯乙烯塑料不能用于包装食品
②夜间天然气泄漏立即开灯寻找泄漏源
①CO2是导致温室效应的一种空气污染物
③pH<7的雨水是酸雨
A、A B、B C、C D、D9. 下面是一些化学实验的改进装置图,下列相关评价或说明错误的是( )A、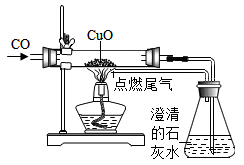 实验可说明CO具有还原性、可燃性
B、
实验可说明CO具有还原性、可燃性
B、 反应结束后,气球膨胀体积大则对应的金属更活泼
C、
反应结束后,气球膨胀体积大则对应的金属更活泼
C、 避免污染空气,操作更简单,测定结果更准确
D、
避免污染空气,操作更简单,测定结果更准确
D、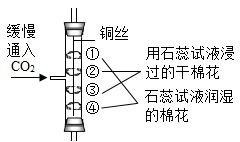 可证明CO2密度比空气大,且能与水反应生成酸性物质
10. 已知①中盛有一定量的Na2CO3溶液,根据图示的实验过程,下列说法错误的是( )
可证明CO2密度比空气大,且能与水反应生成酸性物质
10. 已知①中盛有一定量的Na2CO3溶液,根据图示的实验过程,下列说法错误的是( ) A、烧杯②中溶液呈红色 B、若步骤b中恰好完全反应,则静置后③中上层清液仍为红色 C、取上述静置后③中上层清液加入过量稀盐酸,无气泡生成 D、烧杯④中大量存在的离子有:Na+、Ca2+、H+、Cl-、 -11. 下列图像能正确表示其对应关系的是( )A、
A、烧杯②中溶液呈红色 B、若步骤b中恰好完全反应,则静置后③中上层清液仍为红色 C、取上述静置后③中上层清液加入过量稀盐酸,无气泡生成 D、烧杯④中大量存在的离子有:Na+、Ca2+、H+、Cl-、 -11. 下列图像能正确表示其对应关系的是( )A、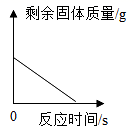 高温煅烧一定质量的石灰石,剩余固体质量随时间的变化
B、
高温煅烧一定质量的石灰石,剩余固体质量随时间的变化
B、 某物质的着火点为t℃,则图中P点时,该物质燃烧得最旺
C、
某物质的着火点为t℃,则图中P点时,该物质燃烧得最旺
C、 20℃时,向一定量接近饱和的KNO3溶液中加入KNO3固体
D、
20℃时,向一定量接近饱和的KNO3溶液中加入KNO3固体
D、 向一定量 溶液中逐滴加入稀盐酸至过量,溶液pH的变化
12. 对于如图的反应:A+B→C+D,下列说法正确的是( )
向一定量 溶液中逐滴加入稀盐酸至过量,溶液pH的变化
12. 对于如图的反应:A+B→C+D,下列说法正确的是( )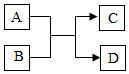 A、若C为金属单质,D为CO2 , 则该反应一定是置换反应 B、若C为一种盐,D为H2O,A为酸,则B一定是一种碱 C、若C为 ,A为AgNO3 , 则B一定是Cu,D一定是Ag D、若C为CO2 , D为H2O,B为O2 , 则A中一定含有C、H元素
A、若C为金属单质,D为CO2 , 则该反应一定是置换反应 B、若C为一种盐,D为H2O,A为酸,则B一定是一种碱 C、若C为 ,A为AgNO3 , 则B一定是Cu,D一定是Ag D、若C为CO2 , D为H2O,B为O2 , 则A中一定含有C、H元素二、综合题
-
13. 如图是一些气体的发生装置和收集装置。
 (1)、写出图中仪器①的名称:。(2)、选择发生装置A,加热暗紫色固体来制取O2 , 反应化学方程式为:。(3)、使用E装置制取CO2 , 铜丝可上下抽动,该装置的优点与装置(选填“B”“C”或“D”)相似。铜丝和铜丝网不能换成铁制品原因是(用化学方程式回答):。14. 某同学使用白醋和鸡蛋壳进行了“再探质量守恒定律”的家庭小实验,操作如图所示。
(1)、写出图中仪器①的名称:。(2)、选择发生装置A,加热暗紫色固体来制取O2 , 反应化学方程式为:。(3)、使用E装置制取CO2 , 铜丝可上下抽动,该装置的优点与装置(选填“B”“C”或“D”)相似。铜丝和铜丝网不能换成铁制品原因是(用化学方程式回答):。14. 某同学使用白醋和鸡蛋壳进行了“再探质量守恒定律”的家庭小实验,操作如图所示。
(査阅资料)鸡蛋壳主要含碳酸钙,与白醋(主要成分为乙酸 CH3COOH)的反应原理为:
(1)、(实验分析)有同学认为m1>m2 , 该反应不遵守质量守恒定律,你(选填“赞成”或“不赞成”)该同学的观点,你的理由是:。
(2)、用质量分数为4%的白醋配制80g质量分数为2%的白醋,需要加水g。如在实验室中,此处量取水最适合的仪器是(选择字母)。A、100mL烧杯、玻璃棒 B、50mL量筒、胶头滴管
C、100mL量筒、胶头滴管 D、10mL量筒、胶头滴管
(3)、假设鸡蛋壳中除CaCO3外,其它成分均不溶于水且不与酸反应,请计算鸡蛋壳中CaCO3的质量分数 , 写出具体的计算过程。(结果精确到0.1%)。15. 2021年3月20日,三星堆遗址发布最新考古成果,青铜神树、青铜面具等破土而出!“拉瓦锡”小组从生活中的铜制品上提取绿色的铜锈,开启“课外考古”探究。(査阅资料)①铜锈俗称铜绿,化学式 ,受热易分解;②无水CuSO4为白色粉末,遇水变蓝;③碱石灰是CaO和NaOH的固体混合物;④碳粉不与稀盐酸反应,不溶于稀盐酸。
(发现问题)小组同学将少量铜锈放入试管中加热,发现固体由绿色变成黑色,试管壁上有无色液滴生成。
(1)、探究一:生成的黑色固体成分。(猜想与假设)该黑色固体可能是:①C粉;②;③C粉和CuO的混合物。
(2)、(设计方案)实验操作
实验现象
实验结论
取少量样品于试管中,加入足量稀盐酸
猜想②正确
(3)、探究二:铜锈受热分解还会生成哪些物质。(进行实验)选择如图所示装置进行验证。

步骤一:连接A和B,打开弹簧夹,通入一段时间的空气;
步骤二:关闭弹簧夹,依次连接装置A→B→(选填“C→D”或“D→C”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
观察到装置D石灰水变浑浊,说明铜锈受热分解生成了CO2;当观察到无水CuSO4从白色变成蓝色,说明铜锈受热分解生成了。
(4)、(反思与评价)装置中A的作用是。写出铜锈受热分解的化学方程式:。16. 工业上以黄铁矿(主要成分为二硫化亚铁,FeS2)为原料生产硫酸,工艺流程如图:
(查阅资料)三个阶段所发生反应的化学方程式为:
①(沸腾炉)
②(接触室)
③(吸收塔)用98.3%硫酸吸收 (焦硫酸)加水
(回答问题)
(1)、将黄铁矿粉碎的目的是 , 反应方程式①中x的值为。(2)、在一密闭容器中进行反应②,某同学测得反应前后各物质的质量如表:物质
甲
乙
丙
丁
反应前质量/g
2.0
6.0
2.0
0
反应后质量/g
1.2
2.8
2.0
a
则乙物质为(选填“SO2、O2、SO3或V2O5”);
(3)、依据生产硫酸的工艺流程图,下列说法正确的是(填字母,多选);A将SO2和O2导回接触室,体现了绿色化学理念
B催化剂能够提高SO2的反应速率和产量
C沸腾炉排出的矿渣可供炼铁
D反应①②③中S元素的化合价都发生了变化
(4)、通常用NaOH溶液吸收尾气中的SO2 , 该反应的化学方程式为;(5)、还有另一制法,将沸腾炉生成的SO2首先溶于H2O变成H2SO3(亚硫酸);然后将H2SO3氧化得H2SO4。请写出两步反应中的任意一步化学方程式。