天津市红桥区2021年中考化学二模试卷
试卷更新日期:2021-06-23 类型:中考模拟
一、单选题
-
1. “绿色发展”、“低碳生活”等理念逐渐深入人心。下列做法值得提倡的是( )A、燃放烟花爆竹 B、生活垃圾进行分类回收处理 C、露天焚烧秸秆 D、实验室含酸废水倒入铁质下水道2. 下列生活中的有关做法不涉及化学变化的是( )A、服用碱性药物治疗胃酸过多 B、“新冠”疫情期间出门佩戴口罩 C、用食醋清洗水壶中的水垢 D、燃烧天然气和柴火煮饭、烧菜3. 空气是人类生产活动的重要资源。下列关于空气的说法正确的是( )A、洁净的空气是纯净物 B、空气中可分离出氧气用于医疗急救 C、空气中含量最多的气体是二氧化碳 D、空气中氮气的化学性质比氧气活泼4. 下列实验操作正确的是( )A、加热液体
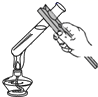 B、倾倒液体
B、倾倒液体  C、检查气密性
C、检查气密性 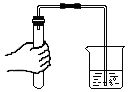 D、过滤
D、过滤 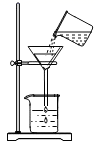 5. 下列物质分类正确的是( )A、单质:氢气、空气 B、氧化物:氧化铜、干冰 C、酸:硝酸、硫酸铜 D、碱:火碱、纯碱6. 下列能使紫色石蕊试液和无色酚酞试液均变色的是( )A、pH=1的盐酸 B、pH=3的硫酸 C、pH=7的氯化钠溶液 D、pH=14的氢氧化钾溶液7. 下列事实的微观解释中,错误的是( )A、墙内开花墙外可闻到花香——分子在不断地运动 B、蔗糖放入水中溶解一一蔗糖分子分解了 C、氧气和液氧都能支持燃烧——物质的分子相同,其化学性质相同 D、水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大8. 元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是( )
5. 下列物质分类正确的是( )A、单质:氢气、空气 B、氧化物:氧化铜、干冰 C、酸:硝酸、硫酸铜 D、碱:火碱、纯碱6. 下列能使紫色石蕊试液和无色酚酞试液均变色的是( )A、pH=1的盐酸 B、pH=3的硫酸 C、pH=7的氯化钠溶液 D、pH=14的氢氧化钾溶液7. 下列事实的微观解释中,错误的是( )A、墙内开花墙外可闻到花香——分子在不断地运动 B、蔗糖放入水中溶解一一蔗糖分子分解了 C、氧气和液氧都能支持燃烧——物质的分子相同,其化学性质相同 D、水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大8. 元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分,下列有关说法正确的是( ) A、铁的相对原子质量为55.85g B、锰元素为非金属元素 C、铬原子的原子核内有52个质子 D、等质量的铬、锰、铁中,含原子个数最多的是铬9. 在化学反应 中,已知 与 恰好完全反应,生成C和D的质量比为 ,又知B的相对分子质量为32,则D的相对分子质量为( )A、9 B、12 C、18 D、3610. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是由3种元素组成的有机物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成11. 类推是化学学习中常用的思维方法。现有以下类推结果,其中正确的是( )A、有机物中都含有碳元素,所以含碳元素的化合物都是有机物 B、把燃着的木条插入某无色气体中,木条火焰熄灭,证明瓶中的气体一定是CO2 C、酸碱盐之间的复分解反应一定有盐生成,则有盐生成的反应一定是复分解反应 D、水在通电条件下,可分解为氧气和氢气,说明在化学反应中分子是可分的12. 利用海带提取碘单质(I2)的工艺流程如图所示,下列说法错误的是( )
A、铁的相对原子质量为55.85g B、锰元素为非金属元素 C、铬原子的原子核内有52个质子 D、等质量的铬、锰、铁中,含原子个数最多的是铬9. 在化学反应 中,已知 与 恰好完全反应,生成C和D的质量比为 ,又知B的相对分子质量为32,则D的相对分子质量为( )A、9 B、12 C、18 D、3610. 连花清瘟胶囊具有清瘟解毒,宣肺泄热的功效。其成分中含有一种名为绿原酸的物质,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是由3种元素组成的有机物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸由16个碳原子、18个氢原子和9个氧原子构成11. 类推是化学学习中常用的思维方法。现有以下类推结果,其中正确的是( )A、有机物中都含有碳元素,所以含碳元素的化合物都是有机物 B、把燃着的木条插入某无色气体中,木条火焰熄灭,证明瓶中的气体一定是CO2 C、酸碱盐之间的复分解反应一定有盐生成,则有盐生成的反应一定是复分解反应 D、水在通电条件下,可分解为氧气和氢气,说明在化学反应中分子是可分的12. 利用海带提取碘单质(I2)的工艺流程如图所示,下列说法错误的是( )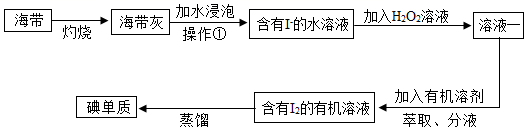 A、操作①中,所需要的玻璃仪器有3种 B、由于淀粉有遇碘(I2)变蓝的特性,因此可以利用淀粉检验加入H2O2溶液后所得的“溶液一”中是否有单质碘生成 C、在上述过程中碘元素的化合价没有发生变化 D、在蒸馏操作中,蒸馏烧瓶内加入沸石的目的是为了防止液体的暴沸
A、操作①中,所需要的玻璃仪器有3种 B、由于淀粉有遇碘(I2)变蓝的特性,因此可以利用淀粉检验加入H2O2溶液后所得的“溶液一”中是否有单质碘生成 C、在上述过程中碘元素的化合价没有发生变化 D、在蒸馏操作中,蒸馏烧瓶内加入沸石的目的是为了防止液体的暴沸二、多选题
-
13. 下列方法能达到除杂目的的是( )
选项
物质(括号内为杂质)
方法
A
CH4 (CO)
点燃混合气体
B
铜粉(碳粉)
在空气中灼烧固体混合物
C
O2(水蒸气)
将混合气体通过浓硫酸
D
NaCl(CaCO3)固体混合物
加水溶解,过滤,蒸发
A、A B、B C、C D、D14. 下列实验中,根据实验现象可得到相应结论的是( )实验操作
现象
结论
A
高温条件下,CO通入Fe2O3粉末
红色粉末变为黑色
利用CO的还原性炼铁
B
用拇指堵住收集了CH4的试管口,靠近火焰,移开拇指点火
发出尖锐爆鸣声
试管中CH4不纯
C
稀盐酸与氢氧化钠溶液反应后所得的溶液中滴加酚酞溶液
酚酞溶液仍为无色
稀盐酸与氢氧化钠溶液恰好完全反应
D
点燃某无色气体,在火焰上方罩一个冷而干燥的小烧杯
烧杯内壁有水珠
该无色气体一定为氢气
A、A B、B C、C D、D15. 下列说法正确的是( )A、质量和质量分数均相等的氢氧化钠溶液与稀硫酸充分反应,所得溶液呈酸性 B、等质量的镁与氧化镁混合,其混合物中镁、氧两种元素的质量比为4:1 C、硝酸镁样品(含一种杂质)14.8g,溶于水,与足量的氢氧化钠溶液充分反应生成沉淀5.5g,则样品中可能含有的杂质是硫酸镁 D、向一定量的氧化铁与氧化铜的混合物中加入100g质量分数为9.8%稀硫酸,恰好完全反应,则原混合物中氧元素的质量是1.6g三、填空题
-
16. 化学与我们的生活有着密切的联系。现有①火碱②酒精③小苏打④石墨⑤氯化钠⑥氧化钙,选择适当物质的序号填空。(1)、可用制铅笔芯的是。(2)、可配制消毒剂的是。(3)、发酵粉中含有的是。(4)、常见食品干燥剂中含有的是。(5)、生理盐水中含有的是。(6)、炉具清洁剂中含有。17. 复学防疫,化学助力。(1)、起床后,测体温。测体温时水银体温计中汞柱会上升的微观原因是汞原子。(2)、上学时,戴口罩。制作口罩用的无纺布面料主要是聚丙烯((C3H6)n),聚丙烯中碳、氢元素的质量比为。(3)、到校后,勤消毒:过氧乙酸用于教室消毒,其化学性质不稳定,分解的化学方程式为: ,则X的化学式为。用于手部消毒的酒精溶液属于易燃物,使用时要注意安全,酒精燃烧的化学方程式为。(4)、用餐时,讲营养。如午餐仅食用米饭、红烧肉、鸡蛋汤、牛奶,从均衡营养角度出发还应补充的一种食物是。18. 根据下列图示实验,回答有关问题:
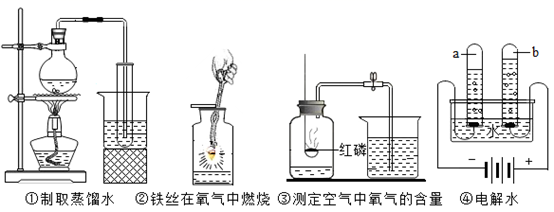 (1)、实验中烧杯内水的作用是。(2)、实验②中水的作用是。(3)、实验③中燃烧匙中放足量的红磷目的是。(4)、实验④中在水中加入硫酸钠目的是 , 电解水的化学方程式是。(5)、用肥皂清洗衣物时,若水中只产生少量的泡沫并出现大量浮渣,则可判断所用的水是(填“硬水”或“软水),生活中常采用的方法降低水的硬度。19. 写出下列反应的化学方程式:(1)、氧化铁和稀盐酸反应:。(2)、铁在氧气中燃烧:。(3)、甲烷燃烧:。20. 在宏观、微观和符号之间建立联系是化学学科的特点。元素周期表是学习和研究化学的重要工具。结合下图回答问题:
(1)、实验中烧杯内水的作用是。(2)、实验②中水的作用是。(3)、实验③中燃烧匙中放足量的红磷目的是。(4)、实验④中在水中加入硫酸钠目的是 , 电解水的化学方程式是。(5)、用肥皂清洗衣物时,若水中只产生少量的泡沫并出现大量浮渣,则可判断所用的水是(填“硬水”或“软水),生活中常采用的方法降低水的硬度。19. 写出下列反应的化学方程式:(1)、氧化铁和稀盐酸反应:。(2)、铁在氧气中燃烧:。(3)、甲烷燃烧:。20. 在宏观、微观和符号之间建立联系是化学学科的特点。元素周期表是学习和研究化学的重要工具。结合下图回答问题: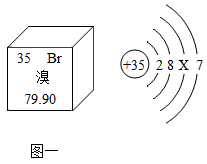
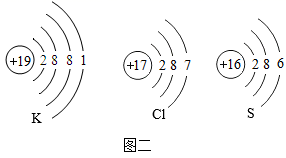 (1)、分析图一,分析溴的原子结构示意图,溴原子的质子数为 , 数值x=。(2)、溴和氯两种元素的化学性质具有相似性的原因是它们原子的相同。(3)、分析图二,在元素周期表中排在第三周期的是S和;写出K和S形成的化合物的化学式。(4)、如图是甲烷与二氧化碳反应的微观示意图。
(1)、分析图一,分析溴的原子结构示意图,溴原子的质子数为 , 数值x=。(2)、溴和氯两种元素的化学性质具有相似性的原因是它们原子的相同。(3)、分析图二,在元素周期表中排在第三周期的是S和;写出K和S形成的化合物的化学式。(4)、如图是甲烷与二氧化碳反应的微观示意图。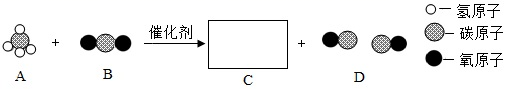
①该反应利用两种温室气体,兼具环保和经济价值;反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,破裂为(填微粒名称)并重新组合。
②C为一种单质,写出该反应的化学方程式。
21. 金属材料在生活生产中有着非常广泛的应用。(1)、金属大规模开发利用的先后顺序与下列因素有关。①金属在自然界中的含量 ②金属冶炼的难易程度 ③金属的导电性 ④金属的活泼性
(2)、按下图装置连接好仪器(铁架台夹持固定等仪器己略去)检查装置的气密性,往装置中添加药品,打开止水夹K通入含有少量二氧化碳的一氧化碳,一段时间后再点燃酒精喷灯。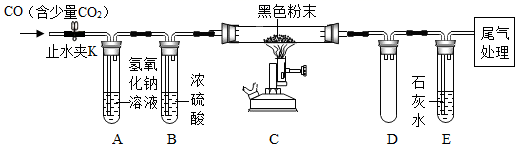
实验中观察到装置C中固体由红色变为黑色,而装置E中石灰水变浑浊,则硬质玻璃管中发生反应的化学方程式为。
(3)、将6.5g含有一种杂质的锌粉与足量稀硫酸反应,生成0.18g氢气。则该锌粉中混有的杂质是(填“铜”或“镁”)。在这种锌粉中加入过量的硝酸银溶液,充分反应后过滤,向溶液加入稀盐酸,有白色沉淀产生。则滤液中含有的溶质是(写化学式)。反应后溶液质量(填“增大”或“减少”)。(4)、某同学将铁粉和铜粉的混合物50g,放入足量的氯化铜溶液中,充分反应后过滤,干燥称得固体质量为54g,求原混合物中铁的质量分数。22. 溶液在日常生活、工农业生产和科学研究中具有广泛的用途。(1)、在盛有水的烧杯中加入以下某种物质,形成溶液的过程中温度下降。这种物质是______(填字母)。A、氯化钠 B、硝酸铵 C、氢氧化钠 D、浓硫酸(2)、在实验室里配制55g10%的氯化钠溶液,操作如图所示,回答下列问题: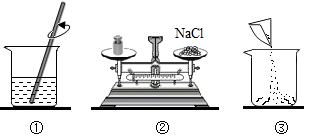
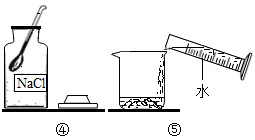
①请用图中的序号表示配制溶液的正确操作顺序。
②认真观察,改正图中的不正确操作。若不进行改正,其他操作步骤正确,则所配制溶液的溶质的质量分数(“大于“小于”或“等于”)10%。
③用15%的氯化钠溶液浸泡瓜果片刻可以起到消毒作用。要使上述氯化钠溶液的溶质质量分数变为15%,向其中加入g氯化钠。
23. 传统中药“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,其分子式为C16HxO9。已知绿原酸的相对分子质量为 354,请你计算:(1)、C16HxO9中 x=。(2)、“绿原酸”中碳元素和氧元素的质量比为。(3)、“绿原酸”中氧元素的质量分数是(结果精确到 0.1%)。四、综合题
-
24. 如下图所示,A-J是初中化学常见的物质。图中“→”表示转化关系,“一”表示相互能反应(部分反应物、生成物及反应条件已略去)。A、B、H常温下为气体,C、E为组成元素相同的氧化物。D、F、G为不同类别的化合物,其中F可以用于改良酸性土壤,G是常见的建筑材料,I广泛应用于玻璃、造纸、印染、纺织等工业、请回答下列问题:
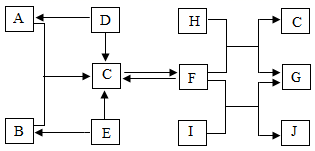 (1)、写出符合物质G的一个化学式。(2)、化学反应D→A基本反应类型为。(3)、写出E→C反应的化学方程式。(4)、写出F和I的反应的化学方程式。25. 化学是一门以实验为基础的科学。根据如图所示的装置,回答下列问题。
(1)、写出符合物质G的一个化学式。(2)、化学反应D→A基本反应类型为。(3)、写出E→C反应的化学方程式。(4)、写出F和I的反应的化学方程式。25. 化学是一门以实验为基础的科学。根据如图所示的装置,回答下列问题。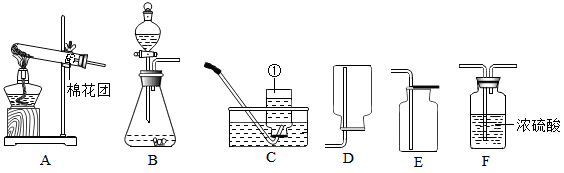 (1)、图中标有序号①的仪器名称是。(2)、实验室用A装置制取氧气,发生反应的化学方程式是 , 在试管口放棉花团的作用是。(3)、实验室制取CO2 , 选择的发生和收集装置是(填装置序号)。在装入药品前,必须要进行的实验操作是。收集过程中,检验二氧化碳收集满的方法是。(4)、实验室取用药品要注意节约,如果没有说明用量,一般应该取用最少量,固体药品只需 , 液体药品取用1-2mL。
(1)、图中标有序号①的仪器名称是。(2)、实验室用A装置制取氧气,发生反应的化学方程式是 , 在试管口放棉花团的作用是。(3)、实验室制取CO2 , 选择的发生和收集装置是(填装置序号)。在装入药品前,必须要进行的实验操作是。收集过程中,检验二氧化碳收集满的方法是。(4)、实验室取用药品要注意节约,如果没有说明用量,一般应该取用最少量,固体药品只需 , 液体药品取用1-2mL。五、计算题
-
26. 现有硫酸钠和硫酸镁固体混合物8g,向其中加入一定量的氢氧化钠溶液恰好完全反应,过滤,得到2.9g沉淀和溶质质量分数为10%的滤液,求:(1)、混合物中硫酸镁的质量;(2)、加入氢氧化钠溶液的溶质质量分数(计算结精确到0.1%)。