天津市和平区2021年中考化学一模试卷
试卷更新日期:2021-06-23 类型:中考模拟
一、单选题
-
1. 下列历史典故中发生了化学变化的是( )A、火烧赤壁 B、司马光砸缸 C、刻舟求剑 D、铁杵磨成针2. 2020年6月,某高速路上一辆液化着油气槽罐车发生爆炸。爆炸产生的以下物质不属于空气污染物的是( )A、NO2 B、CO C、粉尘 D、H2O3. 在太空舱里常用NiFe2O4作催化剂将宇航员呼出的CO2转化为O2。已知NiFe2O4中铁元素为+3价,则Ni元素的化合价为( )A、+1价 B、+2价 C、+3价 D、+4价4. 分离氯化钾和二氧化锰的混合物,下列操作正确的是( )A、取样
 B、溶解
B、溶解  C、过滤
C、过滤  D、蒸发
D、蒸发  5. 下列气体能供给动植物呼吸的是( )A、CO2 B、H2 C、O2 D、N26. 运用分类法学习和研究化学物质,能够收到事半功倍的效果,下列分类正确的是( )
5. 下列气体能供给动植物呼吸的是( )A、CO2 B、H2 C、O2 D、N26. 运用分类法学习和研究化学物质,能够收到事半功倍的效果,下列分类正确的是( )类别选项
混合物
单质
氧化物
碱
盐
A
黄铜
C60
Na2O
Cu2(OH)2CO3
明矾
B
过磷酸钙
Hg
干冰
KOH
纯碱
C
空气
煤
Fe3O4
Ca(OH)2
碳铵
D
福尔马林
Ne
SiO2
NH3·H2O
HBr
A、A B、B C、C D、D7. 磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关磷元素的说法正确的是( ) A、属于金属元素 B、原子核外有16个电子 C、相对原子质量为30.97g D、是农作物必需的营养元素8. 下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量白雾 B、铁丝在空气中燃烧,火星四射,生成黑色固体 C、向氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 D、氯化铵和熟石灰混合研磨生成氯化钙、氨气和水9. 学化学、用化学。生活中,下列做法错误的是( )A、洗发时,先用洗发剂后用护发剂 B、夜晚发现家中燃气泄露,立即开灯检查 C、室内着火时,要用湿毛巾捂住口鼻,贴近地面逃离现场 D、炒菜时发现燃气灶火焰呈黄色,锅底出现黑色物质,可调大燃气灶的进风口10. 在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法错误的是( )
A、属于金属元素 B、原子核外有16个电子 C、相对原子质量为30.97g D、是农作物必需的营养元素8. 下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量白雾 B、铁丝在空气中燃烧,火星四射,生成黑色固体 C、向氢氧化钠溶液中加入硫酸铜溶液,产生蓝色沉淀 D、氯化铵和熟石灰混合研磨生成氯化钙、氨气和水9. 学化学、用化学。生活中,下列做法错误的是( )A、洗发时,先用洗发剂后用护发剂 B、夜晚发现家中燃气泄露,立即开灯检查 C、室内着火时,要用湿毛巾捂住口鼻,贴近地面逃离现场 D、炒菜时发现燃气灶火焰呈黄色,锅底出现黑色物质,可调大燃气灶的进风口10. 在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法错误的是( )物质
a
b
c
d
反应前的质量/g
30
5
10
15
反应后的质量/g
x
y
20
20
A、a一定是反应物 B、x+y=20 C、x的取值范围一定是0<x<30 D、反应生成c与d的质量比为2:111. 归纳和推理是化学学习常用的思维方法。下列说法正确的是( )A、氯化钠、碳酸钙等盐中都含金属元素,所以盐中一定都含金属元素 B、二氧化锰在氯酸钾分解反应中作催化剂,所以二氧化锰可作一切化学反应的催化剂 C、化学变化过程中常伴随着发光、放热现象,所以有发光、放热现象产生的一定是化学变化 D、合金是由一种金属跟其他金属(或非金属)熔合而成的具有金属特性的物质,所以合金一定是混合物12. 下列图像不能正确反映对应变化关系的是( )A、 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量
B、
向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量
B、 向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量
C、
向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量
C、 向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D、
向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D、 向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
13. 碘元素被称为“智力元素”,是人体必需的微量元素之一,人体缺碘会引起甲状腺肿大,幼儿缺碘会造成思维迟钝,影响生长发育。因此,人们常通过摄入海产品或食用加碘盐来补充碘元素,以保证人体健康。利用海带提取碘单质(I2)的工艺流程如图所示,下列说法错误的是( )
向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
13. 碘元素被称为“智力元素”,是人体必需的微量元素之一,人体缺碘会引起甲状腺肿大,幼儿缺碘会造成思维迟钝,影响生长发育。因此,人们常通过摄入海产品或食用加碘盐来补充碘元素,以保证人体健康。利用海带提取碘单质(I2)的工艺流程如图所示,下列说法错误的是( ) A、操作①中,所需要的玻璃仪器有3种 B、由于淀粉有遇碘(I2)变蓝的特性,因此可以利用淀粉检验加入H2O2溶液后所得的“溶液一”中是否有单质碘生成 C、在上述过程中碘元素的化合价没有发生变化 D、在蒸馏操作中,蒸馏烧瓶内加入沸石的目的是为了防止液体的暴沸
A、操作①中,所需要的玻璃仪器有3种 B、由于淀粉有遇碘(I2)变蓝的特性,因此可以利用淀粉检验加入H2O2溶液后所得的“溶液一”中是否有单质碘生成 C、在上述过程中碘元素的化合价没有发生变化 D、在蒸馏操作中,蒸馏烧瓶内加入沸石的目的是为了防止液体的暴沸二、多选题
-
14. 下列实验方案不能达到相应实验目的的是( )
选项
实验目的
实验方案
A
除去CO2中的CO
通入氧气后点燃
B
鉴别CH4和H2
点燃,在火焰上方罩一个冷而干燥的烧杯
C
鉴别羊毛和涤纶
点燃,闻燃烧产物的气味
D
分离铁粉、铜粉
用磁铁吸引固体粉末
A、A B、B C、C D、D15. 下列说法正确的是( )
A、镁铝合金mg和足量的盐酸反应生成0.1g H2 , 则m可能是1 B、要使SO2、SO3中含有相同质量的氧元素,则SO2与SO3的分子个数比2:3 C、将质量分数为20%的KNO3溶液90g配制成40%的溶液,需加入45gKNO3固体 D、氧化钙和碳酸钙的固体混合物质量为120g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为84g。则原固体混合物中钙元素的质量分数为50%三、填空题
-
16. 化学与我们的生活、生产密切相关。选择下列物质的序号填空:。
a 食醋 b 棉花 c 稀有气体 d 干冰 e KNO3 f 加铁酱油
(1)、能有效预防贫血的是。(2)、能使石蕊溶液变红的是。(3)、属于天然高分子化合物的是。(4)、用于人工降雨的物质是。(5)、化肥对提高农作物的产量具有重要作用,属于复合肥料的是。(6)、用于填充霓虹灯灯管的是。17. 从微观角度研究物质的变化才能揭示变化的本质。 (1)、图一所示过程属于变化(填“物理”或“化学”);从微观角度可获得的信息是。(2)、请在图二空白方框内画出相应的微粒模型图。(3)、你对图三所示化学变化的微观解释是。(4)、如图是氪元素在元素周期表中的信息和B~F五种粒子结构示意图。请回答下列问题:
(1)、图一所示过程属于变化(填“物理”或“化学”);从微观角度可获得的信息是。(2)、请在图二空白方框内画出相应的微粒模型图。(3)、你对图三所示化学变化的微观解释是。(4)、如图是氪元素在元素周期表中的信息和B~F五种粒子结构示意图。请回答下列问题:
a.由图A信息可推测氪原子中的质子数为。
b.在B~F五种粒子中,共有(填数字)种元素,具有相对稳定结构的是(填字母序号),E与F的化学性质相似的主要原因是。
18. 水是生命之源,“珍惜水、节约水、保护水“是每个公民的义务和责任。(1)、下列“水”属于纯净物的是。(填序号)A 蒸馏水 B 河水 C 自来水
(2)、用如图甲装置进行电解水的实验,b中收集到的气体是。该实验说明水是由组成的。(3)、人们常用检验地下水是硬水还是软水;生活中可用的方法降低水的硬度:某同学自制如图乙所示简易净水器,图中活性炭的主要作用是。 (4)、高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。高铁酸钾受热时发生的反应为 ,则R是(填化学式)。(5)、电解水时,常在水中加入氢氧化钠使反应容易进行,氢氧化钠本身并不被分解,现用118g溶质质量分数为10%的氢氧化钠溶液进行电解水的实验,一段时间后,溶液中溶质质量分数变为11.8%,下列数据计算正确的是。
(4)、高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。高铁酸钾受热时发生的反应为 ,则R是(填化学式)。(5)、电解水时,常在水中加入氢氧化钠使反应容易进行,氢氧化钠本身并不被分解,现用118g溶质质量分数为10%的氢氧化钠溶液进行电解水的实验,一段时间后,溶液中溶质质量分数变为11.8%,下列数据计算正确的是。A 产生氧气质量为8g
B 溶液中氢氧化钠质量为18g
C 被电解的水的质量为18g
D 反应后溶液质量为90g
19. 按要求写出下列反应的化学方程式。(1)、一氧化碳燃烧的反应。(2)、暗紫色固体制氧气的反应。(3)、氢氧化镁治疗胃酸过多的反应。20. 下图为甲、乙、丙三种固体物质的溶解度曲线,请回答。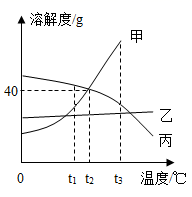 (1)、t1℃时,甲、乙、丙三种物质的溶解度大小关系是。(2)、甲中混有少量乙,若要提纯甲,可采取的结晶方法是。(3)、t2℃时,将50g丙物质放入100g水中充分溶解,所得溶液中溶质和溶液的质量比为(填最简整数比)。(4)、t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液的质量由大到小的顺序是。21. 金属材料对于促进生产发展、改善人类生活发挥了重大作用。(1)、铝具有很好的抗腐蚀性能,原因是。(2)、一氧化碳的还原性可用于冶金工业,写出一氧化碳和氧化铜反应的化学方程式。(3)、向硝酸银溶液中加入一定质量的锌粉和铜粉的混合物,充分反应后过滤,得到滤渣和滤液。以下推断正确的是。
(1)、t1℃时,甲、乙、丙三种物质的溶解度大小关系是。(2)、甲中混有少量乙,若要提纯甲,可采取的结晶方法是。(3)、t2℃时,将50g丙物质放入100g水中充分溶解,所得溶液中溶质和溶液的质量比为(填最简整数比)。(4)、t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液的质量由大到小的顺序是。21. 金属材料对于促进生产发展、改善人类生活发挥了重大作用。(1)、铝具有很好的抗腐蚀性能,原因是。(2)、一氧化碳的还原性可用于冶金工业,写出一氧化碳和氧化铜反应的化学方程式。(3)、向硝酸银溶液中加入一定质量的锌粉和铜粉的混合物,充分反应后过滤,得到滤渣和滤液。以下推断正确的是。A 若向滤渣中加入稀盐酸有气泡产生,则滤渣中一定有银、铜、锌
B 若滤液为无色,则滤渣中一定有锌
C 若滤液为蓝色,则滤液中一定有硝酸银、硝酸铜和硝酸锌
D 滤渣的质量一定比反应前锌粉和铜粉混合物质量大
(4)、下列保护金属资源的做法错误的是。A 任意开采矿物
B 回收利用废旧金属
C 铁制品存放在潮湿的环境中
D 用塑料代替金属材料制造管道
(5)、某废弃物中可能含有Cu、CuO、Mg、Zn中的一种或几种,为确定其成分并回收金属,取样品进行如图实验。
①步骤Ⅱ的操作是。
②步骤Ⅱ中产生的现象是。步骤Ⅰ中锌和稀硫酸反应的化学方程式为。
③若溶液C中只含一种溶质,则样品的成分是。
④通过测氢气的质量,也可确定样品的成分,则w的值为(用m和n的代数式表示)。
22. 如图所示是实验室制取气体的常用装置。请回答下列问题。 (1)、A装置中仪器①的名称是试管口略向下倾斜的原因是 。(2)、仪器②的名称是该仪器的主要作用是 。(3)、实验室用加热氧酸钾制取氧气,应选择的发生装置为(填字母序号);若要收集较纯净的氧气,应选择的收集装置是(填字每序号)。写出过氧化氢溶液和二氧化锰的混合物制取氧气的化学方程式。(4)、制取氧气和二氧化碳均可选择的发生装置和收集装置为(填字母序号)。23. A、B、C、D、E、F、X、Y都是初中化学只的常见物质,已知X 是一种混合物,A、B、Y是单质;通常情况下,C是一种具有刺激性气味且相对分子质量为17的气体,D、E是含有相同元素的氧化物。它们之间有如下转化关系:
(1)、A装置中仪器①的名称是试管口略向下倾斜的原因是 。(2)、仪器②的名称是该仪器的主要作用是 。(3)、实验室用加热氧酸钾制取氧气,应选择的发生装置为(填字母序号);若要收集较纯净的氧气,应选择的收集装置是(填字每序号)。写出过氧化氢溶液和二氧化锰的混合物制取氧气的化学方程式。(4)、制取氧气和二氧化碳均可选择的发生装置和收集装置为(填字母序号)。23. A、B、C、D、E、F、X、Y都是初中化学只的常见物质,已知X 是一种混合物,A、B、Y是单质;通常情况下,C是一种具有刺激性气味且相对分子质量为17的气体,D、E是含有相同元素的氧化物。它们之间有如下转化关系:
请你回答下列问题:
(1)、X的名称 是。(2)、B与Y反应的条件是。(3)、E+氧化铁→D的化学方程式是。(4)、C+D+饱和食盐水→F的化学方程式是。24. 如图1所示,小瑾将反应后试管中的物质全部倒入烧杯时,发现烧杯内白色沉淀明显增多。为了探究烧杯内物质的成分,她立即向其中逐滴加入稀硝酸,并不断搅拌,烧杯内沉淀的质量随加入稀硝酸的质量变化如图2所示。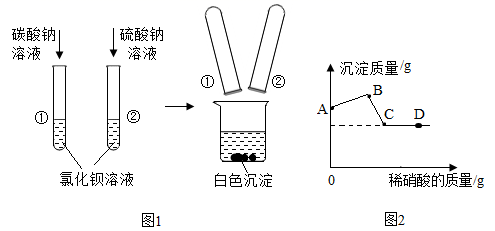
回答下列问题:
(1)、图1所示,烧杯内的白色沉淀是(写化学式)。(2)、BC段发生反应的化学方程式为。(3)、A点,烧杯内的溶液中一定大量含有的离子为(写离子符号)。B点,烧杯内的沉淀由种物质组成。(4)、检验D点溶液中是否含有氯离子的方法。四、计算题