山东省临沂市临沭县2021年中考化学一模试卷
试卷更新日期:2021-06-23 类型:中考模拟
一、单选题
-
1. 下列过程中不发生化学变化的是( )A、铁钉生锈
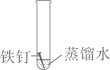 B、白磷放入冷水中
B、白磷放入冷水中  C、电解水实验
C、电解水实验  D、拉瓦锡研究空气成分
D、拉瓦锡研究空气成分 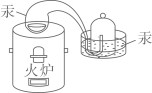 2. Na2CO3俗称纯碱,侯德榜为纯碱工业的发展做出了杰出贡献。Na2CO3属于( )A、氧化物 B、碱 C、盐 D、混合物3. 下列图示的实验操作中正确的是:( )A、浓硫酸稀释
2. Na2CO3俗称纯碱,侯德榜为纯碱工业的发展做出了杰出贡献。Na2CO3属于( )A、氧化物 B、碱 C、盐 D、混合物3. 下列图示的实验操作中正确的是:( )A、浓硫酸稀释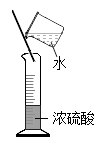 B、闻气体气味
B、闻气体气味  C、液体的倾倒
C、液体的倾倒  D、检查气密性
D、检查气密性 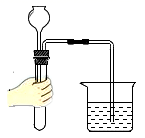 4. 实验时发意外需及时处理。下列处理方法错误的是( )A、过滤液体滤纸被戳破——把玻璃棒靠在三层滤纸处 B、蒸发时食盐四处飞溅——撤去酒精灯并不断搅拌 C、触碰热试管手被烫伤——冷水冲洗后涂抹烫伤膏 D、氢氧化钠沾到皮肤上——大量水冲洗后涂硼酸溶液5. 我国第一艘国产航母“山东舰”在制造的过程中使用了大量的金属材料。下列有关金属材料的说法错误的是( )A、合金的硬度一般比组成它们的纯金属更高 B、钢铁是使用最多的金属材料 C、金属在常温下都是固体 D、大多数金属为电和热的优良导体6. 下列说法错误的是( )A、为减少“白色污染”,提倡自带购物布袋 B、煤、石油、天然气属于化石燃料,取之不尽,用之不竭 C、对铁制品进行防锈处理,可以有效减少金属资源的浪费 D、开发新能源汽车可减少汽油、柴油的使用,从而减少环境污染7. 磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关磷元素的说法正确的是( )
4. 实验时发意外需及时处理。下列处理方法错误的是( )A、过滤液体滤纸被戳破——把玻璃棒靠在三层滤纸处 B、蒸发时食盐四处飞溅——撤去酒精灯并不断搅拌 C、触碰热试管手被烫伤——冷水冲洗后涂抹烫伤膏 D、氢氧化钠沾到皮肤上——大量水冲洗后涂硼酸溶液5. 我国第一艘国产航母“山东舰”在制造的过程中使用了大量的金属材料。下列有关金属材料的说法错误的是( )A、合金的硬度一般比组成它们的纯金属更高 B、钢铁是使用最多的金属材料 C、金属在常温下都是固体 D、大多数金属为电和热的优良导体6. 下列说法错误的是( )A、为减少“白色污染”,提倡自带购物布袋 B、煤、石油、天然气属于化石燃料,取之不尽,用之不竭 C、对铁制品进行防锈处理,可以有效减少金属资源的浪费 D、开发新能源汽车可减少汽油、柴油的使用,从而减少环境污染7. 磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关磷元素的说法正确的是( ) A、属于金属元素 B、原子核外有16个电子 C、相对原子质量为30.97g D、是农作物必需的营养元素8. 课本中用加入少Na2SO4的水进行电解水实验,从该实验中不能获取的信息是( )A、纯水的导电能力弱 B、负极产生气体的速率比正极快 C、常温下,水的pH=7 D、水由氢元素和氧元素组成9. 食品安全问题日益引起人们的重视,下列做法会损害人体健康的是 ( )A、用小苏打烘焙糕点 B、加工火腿肠时放入过量亚硝酸钠防腐 C、用干冰冷藏食物 D、在酱油中加入铁强化剂补充铁元素10. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
A、属于金属元素 B、原子核外有16个电子 C、相对原子质量为30.97g D、是农作物必需的营养元素8. 课本中用加入少Na2SO4的水进行电解水实验,从该实验中不能获取的信息是( )A、纯水的导电能力弱 B、负极产生气体的速率比正极快 C、常温下,水的pH=7 D、水由氢元素和氧元素组成9. 食品安全问题日益引起人们的重视,下列做法会损害人体健康的是 ( )A、用小苏打烘焙糕点 B、加工火腿肠时放入过量亚硝酸钠防腐 C、用干冰冷藏食物 D、在酱油中加入铁强化剂补充铁元素10. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下: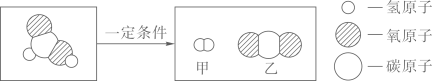
下列说法正确的是( )
A、甲酸分子中氢、氧原子个数比为1:2 B、乙中碳、氧元素质量比为1:2 C、46g甲酸中氢元素质量为2g D、生成甲与乙的分子个数比为2:111. 已知金属R和Fe、H活动性强弱关系为:Fe>R>H,下列说法正确的是( )A、金属R放入Zn(NO3)2溶液中,有锌析出 B、金属R放入CuSO4溶液中,金属表面有红色固体析出 C、金属铁(足量)放入R(NO3)2溶液中,溶液变黄色 D、金属铁放入AgNO3溶液中,一段时间后溶液质量变大12. 化学与生产、生活密切相关,下列说法错误的是( )A、炒菜时油锅着火,用锅盖盖灭 B、碳酸氢铵(NH4HCO3)是一种氮肥 C、人体缺碘会引起贫血 D、铁制品表面刷漆可防止生锈13. 2020年5月5日,配置有氢氧发动机的长征五号B火箭,搭载我国新一代载人试验飞船顺利升空,飞船成功返回。从变化观念和平衡思想认识反应: 。下列说法正确的是( )A、氢气和氧气混合生成水 B、反应前后元素种类不变、化合价改变 C、2g氢气和1g氧气反应生成3g水 D、氢气和氧气反应吸收热量14. X、Y、Z三种物质的溶解度曲线如图所示,下列说法正确的是( )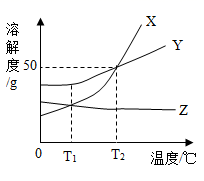 A、Y的溶解度为50g B、T2℃时,X、Y两种物质的溶解度相等 C、T1℃时,三种物质的溶解度由大到小的顺序是Y>X>Z D、T2℃时,50gH2O与50gX混合,可得到100gX的饱和溶液15. 20gKOH加入100g水中,配制成溶液。下列说法错误的是( )A、KOH在水中解离出K+和OH- B、一个K+带一个单位正电荷 C、该溶液的溶质质量分数为20% D、向该溶液中滴入酚酞指示剂,溶液变红16. 下列有关叙述对应的化学方程式、所属基本反应类型都正确的是( )A、细铁丝在氧气中燃烧 化合反应 B、铝与硫酸铜溶液反应 置换反应 C、氢氧化铝药物治疗胃酸过多 3HCl+Al(OH)3=AlCl3+H2O 中和反应 D、氯化钠溶液和硝酸银溶液反应 NaCl+AgNO3=AgCl↓+NaNO3 复分解反应17. 下列除杂的试剂和方法不可行的是( )
A、Y的溶解度为50g B、T2℃时,X、Y两种物质的溶解度相等 C、T1℃时,三种物质的溶解度由大到小的顺序是Y>X>Z D、T2℃时,50gH2O与50gX混合,可得到100gX的饱和溶液15. 20gKOH加入100g水中,配制成溶液。下列说法错误的是( )A、KOH在水中解离出K+和OH- B、一个K+带一个单位正电荷 C、该溶液的溶质质量分数为20% D、向该溶液中滴入酚酞指示剂,溶液变红16. 下列有关叙述对应的化学方程式、所属基本反应类型都正确的是( )A、细铁丝在氧气中燃烧 化合反应 B、铝与硫酸铜溶液反应 置换反应 C、氢氧化铝药物治疗胃酸过多 3HCl+Al(OH)3=AlCl3+H2O 中和反应 D、氯化钠溶液和硝酸银溶液反应 NaCl+AgNO3=AgCl↓+NaNO3 复分解反应17. 下列除杂的试剂和方法不可行的是( )选项
物质(括号内为杂质)
除杂试剂和方法
A
CO2(CO)
通过足量灼热的氧化铜
B
FeSO4溶液(CuSO4)
加入过量铁粉,过滤
C
NaCl(AgCl)
加足量水溶解、过滤、蒸发结晶
D
CuO(C)
加足量稀盐酸,过滤,干燥
A、A B、B C、C D、D18. 将一定质量的Zn放入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,得到滤渣和滤液,下列说法错误的是( )A、滤渣中只含有Ag时,滤液一定呈蓝色 B、滤渣中含有Cu和Ag时,滤液一定呈无色 C、滤渣中含有Zn时,滤液中的溶质只有Zn(NO3)2 D、滤渣中含有Cu时,滤液中的溶质一定没有AgNO3二、填空题
-
19. 化学与我们的生活息息相关。(1)、某食堂的午餐食谱为:米饭、馒头、红烧牛肉、油炸刀鱼和炒青椒。为了补充维生素,应选择的菜品是。(2)、洗手、消毒能有效防止新型冠状病毒感染。“84”消毒液能迅速杀菌消毒,其有效成分NaClO中氯元素的化合价为。(3)、在治疗胃酸过多症的药物成分中,含有的物质不可以是(填字母)。
A 碳酸氢钠 B 氢氧化铝 C 氢氧化钠
(4)、生活中,用于腌渍蔬菜、鱼、蛋等,起到延长保存时间作用的物质是(填化学式)。20. 文房四宝“笔、墨、纸、砚”承载着优秀的中华传统文化。(1)、制作毛笔常用羊毛、兔毛等,检验笔毛是动物毛发的简易方法是。(2)、用墨汁写绘的字画能从古代保存至今而不褪色,是因为常温下碳的化学性质很(填“稳定”或“不稳定”)。(3)、宣纸制作过程中有道工序是从纸浆中用竹帘捞纸,该操作相当于(填字母)。A 蒸发 B 过滤 C 结晶
(4)、砚台产地不同,成分也有差别,但其中的主要成分都(填“易溶”或“难溶”)于水。21. 2019年碳家族再添新成员,某研究小组合成出第一个由18个碳原子构成的环状纯碳分子,其结构如图所示。回答: (1)、碳原子的结构示意图为
(1)、碳原子的结构示意图为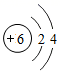 ,其最外层电子数是 , 若碳元素在化合物中的化合价为+4价,符合要求的化合物的化学式为。 (2)、尝试写出环状纯碳分子的化学式。22. 从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。
,其最外层电子数是 , 若碳元素在化合物中的化合价为+4价,符合要求的化合物的化学式为。 (2)、尝试写出环状纯碳分子的化学式。22. 从下图选择仪器,配置60g溶质质量分数为10%的NaCl溶液。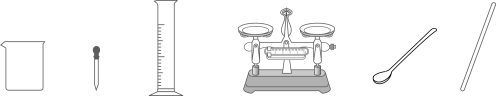 (1)、需要称量NaCl的质量为g。(2)、量取水用到的仪器有(写名称)。(3)、从配好的溶液中倒出10g,其中溶质和溶剂的质量比为。23. 酸、碱、盐的溶解性表是学习化学的重要工具之一。下表是部分酸、碱、盐在水中的溶解性(20℃),请回答下列问题。
(1)、需要称量NaCl的质量为g。(2)、量取水用到的仪器有(写名称)。(3)、从配好的溶液中倒出10g,其中溶质和溶剂的质量比为。23. 酸、碱、盐的溶解性表是学习化学的重要工具之一。下表是部分酸、碱、盐在水中的溶解性(20℃),请回答下列问题。阴离子
阳离子
OH-
NO3-
CO32-
Cl-
K+
溶
溶
溶
溶
Ba2+
溶
溶
不
溶
Cu2+
不
溶
不
溶
(1)、上述阴、阳离子形成不溶性碱的化学式为 , 形成复合肥料的化学式为。(2)、KOH溶液和Ba(NO3)2溶液(填“能“或“不能“)反应,理由是。(3)、下列各组离子在水溶液中能大量共存的是_______________ 。A、OH-、H+、Ba2+、NO B、OH-、Ba2+、K+、Cl- C、CO 、K+、Ba2+、Cl- D、CO 、Cu2+、NO 、K+24. 金属的用途很广,我们应该节约和保护金属资源,铁制品长期裸露在室外易生锈,铁生锈实际上是铁与空气中的氧气和水蒸气等发生化学反应的过程。为了预防铁制品生锈,我们常在其表面镀一层抗腐蚀的金属,但在镀金属之前,先要除去铁制品表面的铁锈。用稀盐酸除去铁锈的化学反应方程式是。25. 正确选择实验仪器是实验成功的关键,下列仪器常用于实验室制气体,请根据装置回答下列问题。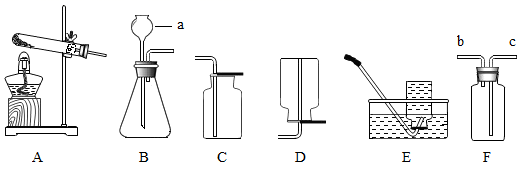 (1)、实验室需纯净的氧气用于铁丝燃烧实验,从A-E中选择合适的制取和收集氧气的装置是(填字母序号)。(2)、为探究二氧化碳的性质,小军制取并收集了一瓶二氧化碳气体,反应的化学方程式是。(3)、若要用F装置检测CO2 , 在F装置中盛放的试剂名称是 , CO2应从(填“b”或“c”)端通入。26. 莽草酸(C7H10O5)是从八角中提取的一种化合物,是合成治疗新冠肺炎的药物“奥司他韦”的原料。计算:(1)、莽草酸的相对分子质量是。(2)、莽草酸中氧元素的质量分数为。(结果精确到0.1%)27. X、Y、Z是中学化学常见的物质,三种物质均含有同一种元素,它们之间有下图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。
(1)、实验室需纯净的氧气用于铁丝燃烧实验,从A-E中选择合适的制取和收集氧气的装置是(填字母序号)。(2)、为探究二氧化碳的性质,小军制取并收集了一瓶二氧化碳气体,反应的化学方程式是。(3)、若要用F装置检测CO2 , 在F装置中盛放的试剂名称是 , CO2应从(填“b”或“c”)端通入。26. 莽草酸(C7H10O5)是从八角中提取的一种化合物,是合成治疗新冠肺炎的药物“奥司他韦”的原料。计算:(1)、莽草酸的相对分子质量是。(2)、莽草酸中氧元素的质量分数为。(结果精确到0.1%)27. X、Y、Z是中学化学常见的物质,三种物质均含有同一种元素,它们之间有下图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。 (1)、若X、Y的组成元素完全相同;Z为气体单质,能供给呼吸,也能使带火星的木条复燃,X转化为Y的化学方程式为;从微观角度解释X、Y性质有差异的原因是。(2)、若X为固体单质;Y可以用于灭火;Z是易与血液中血红蛋白结合的有毒气体,Y转化为Z的化学方程式为。(3)、若三种物质均含有钙元素; X可以用来改良酸性土壤;Z为难溶于水的白色固体,其中金属元素的质量分数为40%,Y的化学式为。
(1)、若X、Y的组成元素完全相同;Z为气体单质,能供给呼吸,也能使带火星的木条复燃,X转化为Y的化学方程式为;从微观角度解释X、Y性质有差异的原因是。(2)、若X为固体单质;Y可以用于灭火;Z是易与血液中血红蛋白结合的有毒气体,Y转化为Z的化学方程式为。(3)、若三种物质均含有钙元素; X可以用来改良酸性土壤;Z为难溶于水的白色固体,其中金属元素的质量分数为40%,Y的化学式为。三、综合题
-
28. 火是文明的起源,取火的方法,经历了漫长的演变过程。(1)、古代人使用的“火折子”吹气即可燃,“火折子”的制作材料中有硫磺。硫燃烧的化学反应方程式为。(2)、1830年,法国人发明了摩擦火柴,将白磷、硫、KClO3、MnO2混合做火柴,摩擦生热使白磷燃烧,利用白磷燃烧的热量使KClO3分解,然后是硫燃烧。该过程中KClO3分解的化学反应方程式为。推测摩擦过程中白磷比硫先燃烧的原因是。(3)、19世纪中期,瑞典人创造出安全火柴,将红磷涂在火柴盒的摩擦面上,硫、KClO3、MnO2则藏于火柴头中。火柴划燃的瞬间,火苗异常旺,对产生此现象的原因推测不合理的是______________(填序号)。A、火柴头里的硫比火柴梗燃烧更剧烈 B、MnO2分解产生氧气助燃 C、KClO3分解产生氧气助燃29. 高锰酸钾是一种重要的化工产品,在化学、生产、生活等场境中都有重要的用途。某工厂生产高锰酸钾的流程如下图所示。
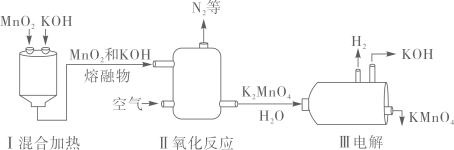
请回答下列问题:
(1)、写出高锰酸钾的一种用途。(2)、“I混合加热”发生的主要是(填“物理”或“化学”)变化。(3)、请将“Ⅱ氧化反应”发生反应的化学方程式补充完整(在横线上填化学式)。+2MnO2+4KOH 2K2MnO4+2
(4)、“Ⅲ电解”反应中,反应前后化合价发生变化的元素有(写元素符号)。(5)、生产流程中可循环利用的物质是(写化学式)。30. 某化学兴趣小组在学完金属活动性顺序相关知识后,他们做了钠与硫酸铜溶液反应的实验,发现并没有铜生成,而是产生蓝色沉淀和少量黑色物质。于是他们进行了如下探究:(实验探究1)取一块绿豆大小的金属钠,擦干,放入盛有20mL蒸馏水的烧杯中,发现金属钠浮在水面上,熔化成一个闪亮的小球并四处游动,发出嘶嘶的响声,收集反应产生的气体,发现该气体能燃烧。
(实验探究2)在上述反应所得溶液中滴加硫酸铜溶液,产生蓝色絮状沉淀。
(实验探究3)将蓝色絮状沉淀加热得到黑色固体。
(查阅资料)①钠在常温下能与水剧烈反应,生成一种碱和一种气体。②氢氧化铜受热易分解。③氧化铜为黑色固体。
(1)、(问题分析)①写出钠与水反应的化学方程式 , 点燃反应产生的气体前应先。
②写出产生蓝色絮状沉淀的化学方程式。
(2)、(实验结论)在金属活动性顺序中,活动性较强的金属(填“一定”或“不一定”)能将位于其后面的金属从它们的盐溶液中置换出来。(3)、(反思与交流)钠与硫酸铜溶液反应产生少量黑色物质的可能原因。四、计算题
-
31. 向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
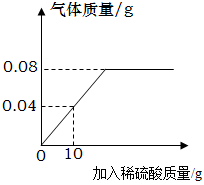 (1)、铁粉反应完时,产生氢气的质量为g。(2)、原稀硫酸中溶质的质量分数(写出计算过程)。
(1)、铁粉反应完时,产生氢气的质量为g。(2)、原稀硫酸中溶质的质量分数(写出计算过程)。