山东省德州市乐陵市2021年中考化学二模试卷
试卷更新日期:2021-06-23 类型:中考模拟
一、单选题
-
1. “垃圾是放错位置的资源”、我市以创建文明城市为契机,全域推进垃圾分类工作。把生活垃圾按图示分四类进行科学处置,实行“定时、定点”投放,金属易拉罐属于( )A、
 B、
B、 C、
C、 D、
D、
-
2. 正确的操作是实验成功的关键,下列图示实验操作正确的是( )A、稀释浓硫酸
 B、加热液体
B、加热液体  C、读取液体体积
C、读取液体体积  D、移开蒸发皿
D、移开蒸发皿 
-
3. 氧气是空气的主要成分之一。下列说法错误的是( )A、通常状况下,O2是无色气体 B、相同条件下,O2的密度大于CO2的 C、分离液态空气可获得O2 D、O2能够支持可燃物的燃烧
-
4. 2019年12月,发射成功的“胖五”(长征五号运载火箭)使用了液氢做燃料。氢气在液化过程中,下列说法正确的是( )A、分子质量增大 B、分子间的间隔减小 C、分子的体积减小 D、分子停止运动
-
5. 下列关于水的说法正确的是( )A、用肥皂水能区别硬水和软水 B、过滤后得到的河水是纯净物 C、生活污水可以随意排放 D、在河水样品中加入明矾可以除去水中所有杂质
-
6. 如图表示两种气体发生的化学反应,其中相同的球代表同种原子,下列说法正确的是( )
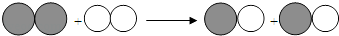 A、生成物一定是混合物 B、分子在化学变化中不可分 C、化学反应前后原子的种类不变 D、该反应既不是化合反应也不是分解反应
A、生成物一定是混合物 B、分子在化学变化中不可分 C、化学反应前后原子的种类不变 D、该反应既不是化合反应也不是分解反应 -
7. 对比是学习化学的重要方法,下列关于二氧化碳和一氧化碳的比较,完全正确的是( )A、组成:CO2、CO均由碳元素和氧元素组成 B、性质:CO2、CO都有可燃性 C、用途:CO2可用于灭火;CO可用于人工降雨 D、危害:CO2会导致酸雨;CO会引起中毒
-
8. 下列实验中,能证明燃烧需要氧气的是( )A、
 B、
B、 C、
C、 D、
D、
-
9. 铁在海水中容易被锈蚀、通常在轮船的吃水线以下焊接比铁更活泼的金属块,用于保护铁质船壳。该金属块的材料可以是( )A、金 B、银 C、铜 D、锌
-
10. 若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实验( )
 A、甲和乙 B、乙和丙 C、甲和丙 D、丙和丁
A、甲和乙 B、乙和丙 C、甲和丙 D、丙和丁 -
11. 小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是( )
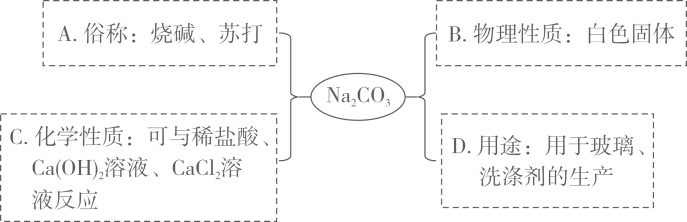 A、A B、B C、C D、D
A、A B、B C、C D、D -
12. 建立模型是学习化学的重要方法,下列化学模型表示中错误的是( )A、

B、
B、
C、
C、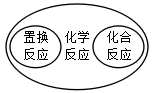
D、
D、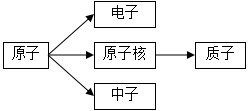
-
13. 下图是某实验小组做粗盐提纯实验的部分操作示意图。下列有关实验叙述错误的是( )
 A、④中缺少玻璃棒引流溶液 B、①中玻璃棒的作用是搅拌,加速粗盐溶解 C、上述操作顺序为③①②④ D、当②蒸发皿中出现较多固体时,停止加热
A、④中缺少玻璃棒引流溶液 B、①中玻璃棒的作用是搅拌,加速粗盐溶解 C、上述操作顺序为③①②④ D、当②蒸发皿中出现较多固体时,停止加热 -
14. 下列图像能正确反映其对应关系的是()A、
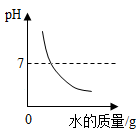 表示向NaOH溶液中不断加水稀释
B、
表示向NaOH溶液中不断加水稀释
B、 表示水电解生成氢气与氧气的质量关系
C、
表示水电解生成氢气与氧气的质量关系
C、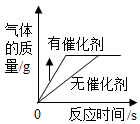 表示用等质量、等质量分数的过氧化氢溶液制取氧气
D、
表示用等质量、等质量分数的过氧化氢溶液制取氧气
D、 表示分别向等质量、等质量分数的稀硫酸中加入足量的镁、铝
表示分别向等质量、等质量分数的稀硫酸中加入足量的镁、铝
-
15. 下列各组固体物质,不能用水鉴别的是( )A、KNO3、KCl B、CaCO3、CaCl2 C、CuSO4、Na2SO4 D、NH4NO3、CaO
-
16. 下列各组实验方案错误的是( )
序号
实验目的
实验方案
A
除去NaCl固体中的Na2CO3
加入适量的稀盐酸,充分反应
B
鉴别NH4Cl和KCl两种白色固体肥料
加入熟石灰研磨后闻气味
C
除去Cu中的CuO
加足量稀盐酸,充分反应后过滤、洗涤、烘干
D
氯酸钾制取氧气后回收MnO2固体
加足量水溶解,过滤,洗涤,干燥
A、A B、B C、C D、D
二、填空题
-
17. 化学就在我们身边,人类的衣、食、住、行都离不开化学。
 (1)、图1是某服装标签的部分内容。面料和里料中属于合成材料的是。(2)、某学校的早餐饼配料表见图2,其中富含蛋白质的物质是;当衣服上沾有花生油时,可用洗涤剂除去,是由于洗涤剂对花生油有作用。(3)、饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,可服用碳酸氢钠片或胃舒平(主要成分为Al(OH)3)治疗,其反应的基本类型均为反应。(4)、2019年5月,华为宣布做好了启动备用芯片的准备,硅是计算机芯片的基体材料。高温下氢气与四氯化硅反应制硅的反应为: ,其中X的化学式为。
(1)、图1是某服装标签的部分内容。面料和里料中属于合成材料的是。(2)、某学校的早餐饼配料表见图2,其中富含蛋白质的物质是;当衣服上沾有花生油时,可用洗涤剂除去,是由于洗涤剂对花生油有作用。(3)、饮食过量,胃酸会大量分泌,以致消化不良。为缓减该症状,可服用碳酸氢钠片或胃舒平(主要成分为Al(OH)3)治疗,其反应的基本类型均为反应。(4)、2019年5月,华为宣布做好了启动备用芯片的准备,硅是计算机芯片的基体材料。高温下氢气与四氯化硅反应制硅的反应为: ,其中X的化学式为。 -
18. 运用分类法学习和研究化学物质,能够收到事半功倍的效果,根据如下纯净物的分类图,回答列问题:
 (1)、如图中的空白方框内应填。(2)、用下列物质的化学式填空:氢氧化钙、金刚石、汞、乙醇、三氧化硫、小苏打。
(1)、如图中的空白方框内应填。(2)、用下列物质的化学式填空:氢氧化钙、金刚石、汞、乙醇、三氧化硫、小苏打。①属于有机物的是。
②属于氧化物的是。
③属于非金属单质的是。
④属于盐的是。
-
19. 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。(1)、(一)分析物质结构,全面了解物质的性质
构成氢气的粒子是(填“氢分子”或“氢原子”)。
(2)、根据如图1所示图示信息判断,下列说法正确的是______(填序号)。A、硫属于金属元素 B、硫原子中的质子数为16 C、硫的相对原子质量为32.06g(3)、根据如图2粒子的结构示意图,回答问题。
①图2中粒子共表示种元素(填数字)。
②A为氯原子的结构示意图,与氯原子的化学性质最相似的是(填序号)。
(4)、(二)研究物质的变化,揭示变化的本质。
图一所示过程属于变化(填“物理”或“化学”):从微观角度可获得的信息是。
(5)、请在图二空白方框内画出相应的微粒模型图。(6)、你对图三所示化学变化的微观解释是。 -
20. 金属是大自然赐予人类的宝物,是现代文明不可缺少的物质基础。(1)、人类冶炼和使用金属铝的时间较晚。可能是因为(填字母)。
a.地壳中铝元素含量少 b.冶炼铝的技术要求高
(2)、银器在使用过程中,因为发生化学反应: ,产生的Ag2S使银器渐失去光泽。已知银的化合价为+1价,则Ag2S中S的化合价为。(3)、A是目前世界年产量最高的金属,根据下图回答下列问题:
B的名称是。
溶液C中溶质的化学式为。
③可证明铁的金属活动性比铜(填“强”或“弱”)。
②的基本反应类型是。
④的化学方程式为。
-
21. 甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答下列问题:
 (1)、t1℃时,甲、乙、丙三种物质中溶解度最大的是。(2)、t2℃时,甲物质的溶解度为g。(3)、少量甲物质混在乙物质中,若提纯乙物质,可采取的结晶方法是。(4)、将t2℃时的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液溶质质量分数由大到小的顺序为。(5)、如图2,t1℃时,若向烧杯中加入足量的______(填字母序号)并使之充分溶解,在试管中可观察到有晶体析出。A、氯化钠 B、氢氧化钠 C、硝酸铵
(1)、t1℃时,甲、乙、丙三种物质中溶解度最大的是。(2)、t2℃时,甲物质的溶解度为g。(3)、少量甲物质混在乙物质中,若提纯乙物质,可采取的结晶方法是。(4)、将t2℃时的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液溶质质量分数由大到小的顺序为。(5)、如图2,t1℃时,若向烧杯中加入足量的______(填字母序号)并使之充分溶解,在试管中可观察到有晶体析出。A、氯化钠 B、氢氧化钠 C、硝酸铵
三、综合题
-
22. 实验室制取某种气体X,X为氢气、氧气或二氧化碳。根据下图回答下列问题:
 (1)、若将A和C连接制取气体X,则X为:。(2)、若将A和B或A和D连接都可制取气体X,则分液漏斗中盛装的药品为。(3)、若向锥形瓶中盛装大理石或石灰石,来制取气体X,反应的方程式为。(4)、若用加热氯酸钾和二氧化锰的混合物来制取氧气,除选取上图部分装置外,还需补充大试管、单孔塞、玻璃导管、胶皮管、铁架台(带铁夹)和(填一种仪器)。(5)、某小组将制取的O2和CO2(各一瓶)混淆了,设计如下方案进行区分。
(1)、若将A和C连接制取气体X,则X为:。(2)、若将A和B或A和D连接都可制取气体X,则分液漏斗中盛装的药品为。(3)、若向锥形瓶中盛装大理石或石灰石,来制取气体X,反应的方程式为。(4)、若用加热氯酸钾和二氧化锰的混合物来制取氧气,除选取上图部分装置外,还需补充大试管、单孔塞、玻璃导管、胶皮管、铁架台(带铁夹)和(填一种仪器)。(5)、某小组将制取的O2和CO2(各一瓶)混淆了,设计如下方案进行区分。方案
现象
结论
方案1:将带火星的木条分别伸入两个集气瓶中
若带火星的木条
则该瓶气体是O2
方案2:向两个集气瓶中分别滴入少量的溶液,振荡
若溶液变浑浊
则该瓶气体是CO2
方案3:向两个集气瓶中分别倒入少量的水,振荡后再滴加几滴紫色石蕊溶液
若紫色石蕊溶液变为色
则该瓶气体是CO2
-
23. 以“NaOH的性质”为中心,某化学兴趣小组进行以下探究实验(实验装置中夹持仪器已略去)。(1)、(实验1)配制溶液
用NaOH固体配制20g20%NaOH溶液,无需用到的玻璃仪器有(填标号)。
A胶头滴管 B酒精灯 C量筒 D烧杯 E玻璃棒
(2)、(实验2)开启氢氧化钠性质系列探究活动如下图所示。

回答下列问题:
实验①观察到紫色石蕊溶液变成色,实验②观察到无色酚酞溶液变成红色。由此得出:碱溶液能使指示剂变色。
(3)、实验③:Ⅰ、当滴加稀盐酸至溶液呈无色时,此时溶液中的溶质(除酚酞外)为或(填化学式)。Ⅱ、如图是氢氧化钠与盐酸反应的微观模拟示意图:从微观的角度分析,甲、乙两处应填入的离子符号分别为、。
 (4)、实验④观察到的现象是 , 说明碱溶液能与某些盐反应。该反应的化学方程式为。(5)、实验⑤⑥为用软矿泉水瓶所做的对比实验,装的软塑料瓶变瘪更明显,原因是(用化学方程式表示)。
(4)、实验④观察到的现象是 , 说明碱溶液能与某些盐反应。该反应的化学方程式为。(5)、实验⑤⑥为用软矿泉水瓶所做的对比实验,装的软塑料瓶变瘪更明显,原因是(用化学方程式表示)。