宁夏石嘴山市平罗县2021年中考化学一模试卷
试卷更新日期:2021-06-23 类型:中考模拟
一、单选题
-
1. “一带一路”是跨越时空的宏伟构想,赋予了古丝绸之路崭新的时代内涵。下列通过古丝绸之路传到国外的发明和技术中不涉及化学变化的是()A、使用火药 B、指南针指引航海 C、用泥土烧制陶瓷 D、冶炼金属2. 2021年3月接连不断的沙尘天气对人们生活造成影响,下列做法与低碳环保理念一致的是( )A、农田里的秸杆就地焚烧 B、生活垃圾分类处理 C、为提高经济效益工业废气直接排放 D、用煤炭燃烧火力发电3. 化学符号是学习化学的重要工具。下列对①~④所示化学符号的意义叙述正确的是( )
①He ②Zn ③Zn2+ ④H2O2
A、①②④都表示一个分子 B、③表示一个锌离子带2个单位的正电荷 C、④表示H2O2分子中含有氢分子和氧分子 D、②和③属于同种元素,所以它们的化学性质相同4. 规范的实验操作是确保实验成功的前提。下列实验操作中正确的是( )A、稀释浓硫酸时,将水沿玻璃棒慢慢注入浓硫酸中,并不断搅拌 B、测定pH时,用玻璃棒蘸取待测液,滴在湿润的pH试纸上,颜色变化后与标准比色卡比较 C、实验完毕,先用嘴吹灭酒精灯,后盖上灯帽 D、蒸发操作时,当有大量晶体析出时停止加热,用余热使水蒸发5. 分类是学习化学的一种重要方法。下列归类正确的是( )A、塑料、涤纶、不锈钢都是合成材料 B、C60、He、水银都属于单质 C、纯碱、烧碱、Ba(OH)2都属于碱 D、KNO3、NH4NO3、(NH4)2HPO4都是复合肥料6. “共享单车”方便了市民的绿色出行;随着夏季气温的升高,“共享单车”的充气轮胎容易发生爆炸的主要原因是( )A、分子在不断运动 B、分子变成原子 C、分子体积变大 D、分子间隔变大,分子运动速率加快7. 在对抗新型冠状病毒的战役中,科学家发现瑞德西韦这种药物对抵抗病毒有一定的作用,其化学式为 C27H35N6O8P。下列有关瑞德西韦的叙述错误的是( )A、属于有机物 B、由五种元素组成 C、碳、氢元素的质量比为27:35 D、碳元素的质量分数最大8. 分析推理是学习化学常用的方法。下列推理正确的是( )A、复分解反应的条件是有气体生成,则有气体生成的反应是复分解反应 B、金属元素的最外层电子数小于 4,所以最外层电子数小于 4 的一定是金属元素 C、化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物 D、碱溶液能使无色酚酞溶液变红,所以能使无色酚酞溶液变红的溶液一定是碱溶液9. 学好化学的有效方法之一是善于梳理归纳知识,下列归纳不完全正确的是( )A 性质决定用途
B 日常生活经验
1.铜有优良的导电性——用于制导线
2.氮气的化学性质不活泼——可作保护气
3.氧气助燃——气焊切割金属
1.洗餐具上的油污——用洗洁精乳化
2.除去热水瓶上的水垢 ——用食醋反应
3.区别棉和羊毛织物——点燃闻气味
C 爱护水资源
D 安全常识
1.用淘米水浇花——节约用水
2.活性炭——除自来水异味
3.污水处理——防止污染
1.室内天然气泄漏——立即打开排气扇
2.炒菜时油锅着火——用锅盖盖灭
3.火场自救的必要措施——用湿毛巾捂住口鼻,蹲下靠近地面沿墙壁跑离着火区
A、A B、B C、C D、D10. 除去下列物质中少量杂质(括号内物质为杂质),所选用的试剂和操作方法错误的是( )选项
物质(杂质)
试剂、操作方法
A
MnO2固体(KCl)
加水溶解、过滤、洗涤、干燥
B
CO2(CO)
点燃
C
Fe(NO3)2溶液[Cu(NO3)2]
加入过量的铁粉、过滤
D
KCl(KOH)
加适量稀HCl蒸发结晶
A、A B、B C、C D、D11. 科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为CH2O),该反应过程的微观示意图如下。下列说法正确的是( )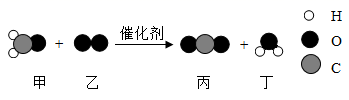 A、该反应属于化合反应 B、物质乙中氧元素的化合价为﹣2价 C、该反应前后原子种类和数目均发生改变 D、图中只有两种氧化物12. 下列物质的转化不能一步实现的是( )A、HCl—H2—H2O B、Zn—Fe—FeCl2 C、NaOH—H2O—O2 D、CaO—CaCO3—Na2CO3
A、该反应属于化合反应 B、物质乙中氧元素的化合价为﹣2价 C、该反应前后原子种类和数目均发生改变 D、图中只有两种氧化物12. 下列物质的转化不能一步实现的是( )A、HCl—H2—H2O B、Zn—Fe—FeCl2 C、NaOH—H2O—O2 D、CaO—CaCO3—Na2CO3二、填空题
-
13. 从K、C、Na、H、O、N六种元素中选择,写出一个符合要求的化学式:(1)、最常用的溶剂。(2)、蒸馒头常用的小苏打是。(3)、显+3价氮的氧化物。14. a、b、c三种物质的溶解度曲线如图1所示,请结合图示回答下列问题:
 (1)、P点的含义是。(2)、若图2试管中为b物质的饱和溶液,则固体X放入水中会(填“吸热”或“放热”)。(3)、t3℃时,将50克的a物质放入50克水中形成的溶液中溶质和溶液的质量比为。(4)、t3℃时,a、b、c的饱和溶液降温至t2℃时,所得溶液中溶质质量分数由大到小的顺序为。15. 通过近一年的学习,同学们一定深刻感受到化学就在身边,化学与生活、生产密切相关。(1)、中卫硒砂瓜中含“硒”元素,它属于元素(选填“常量”或“微量”)。(2)、厨房中长期未使用的铝制高压锅光亮如新、而铁锅上却有许多红色铁锈。铝制高压锅光亮如新的原因是(用文字描述)。某同学用稀盐酸洗去铁锅上的铁锈,请你帮他写出稀盐酸与铁锈反应的化学方程式是。(3)、宁夏开采出的天然气属于能源。(选填“可再生”或“不可再生”)(4)、大武口凉皮,麻辣鲜香,凉皮用淀粉制作,则凉皮主要富含的营养素是;彭阳杏子远销省内外,杏子中含有的主要营养素是。
(1)、P点的含义是。(2)、若图2试管中为b物质的饱和溶液,则固体X放入水中会(填“吸热”或“放热”)。(3)、t3℃时,将50克的a物质放入50克水中形成的溶液中溶质和溶液的质量比为。(4)、t3℃时,a、b、c的饱和溶液降温至t2℃时,所得溶液中溶质质量分数由大到小的顺序为。15. 通过近一年的学习,同学们一定深刻感受到化学就在身边,化学与生活、生产密切相关。(1)、中卫硒砂瓜中含“硒”元素,它属于元素(选填“常量”或“微量”)。(2)、厨房中长期未使用的铝制高压锅光亮如新、而铁锅上却有许多红色铁锈。铝制高压锅光亮如新的原因是(用文字描述)。某同学用稀盐酸洗去铁锅上的铁锈,请你帮他写出稀盐酸与铁锈反应的化学方程式是。(3)、宁夏开采出的天然气属于能源。(选填“可再生”或“不可再生”)(4)、大武口凉皮,麻辣鲜香,凉皮用淀粉制作,则凉皮主要富含的营养素是;彭阳杏子远销省内外,杏子中含有的主要营养素是。三、综合题
-
16. 根据下图回答问题。
 (1)、仪器a的名称是。(2)、用高锰酸钾制取氧气的化学方程式是 , 选用的发生装置(填字母序号,下同)。(3)、实验室制取二氧化碳时,选用的收集装置是 , 原因是。将燃着的木条放在瓶口,若观察到 , 说明瓶中已充满二氧化碳。17. 小明在帮助老师清理化学实验室时,发现一瓶名为草酸的白色固体。仔细查看药品标签,确认其化学式为H2C2O4。草酸具有哪些化学性质呢?为此他展开了探究。(1)、探究一:草酸是否具有和稀盐酸、稀硫酸相似的化学性质?
(1)、仪器a的名称是。(2)、用高锰酸钾制取氧气的化学方程式是 , 选用的发生装置(填字母序号,下同)。(3)、实验室制取二氧化碳时,选用的收集装置是 , 原因是。将燃着的木条放在瓶口,若观察到 , 说明瓶中已充满二氧化碳。17. 小明在帮助老师清理化学实验室时,发现一瓶名为草酸的白色固体。仔细查看药品标签,确认其化学式为H2C2O4。草酸具有哪些化学性质呢?为此他展开了探究。(1)、探究一:草酸是否具有和稀盐酸、稀硫酸相似的化学性质?(设计实验)先将少量草酸固体溶于水中得到草酸溶液,并进行以下实验:
向草酸溶液中滴加 , 发现溶液变红,说明草酸溶液显酸性。
(2)、向草酸溶液中加入少量铝粉,有气泡产生。(得出结论)草酸与稀盐酸、稀硫酸化学性质相似:能使指示剂变色,能与反应。
写出稀硫酸与金属铝反应的化学方程式。
(3)、探究二:草酸加热能否分解?取少量草酸固体于试管中,加热,得到水和气体氧化物,产生的气体可能是。
(4)、(设计实验)为验证草酸分解生成的气体,小明设计如图所示实验:
当观察到 , 说明草酸分解生成的气体中含有CO2。
(5)、氧化铁粉末由红色变为黑色,且F中澄清石灰水变浑浊,说明草酸分解生成的气体中含有 , 由上述实验可得草酸受热能分解,其反应的化学方程式为。(6)、(拓展反思)在进行金属冶炼实验时,需进行尾气处理,其原因是。18. 小红同学进行酸碱中和反应的实验(如下图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂。为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中液体颜色没有变化。于是她对烧杯中的溶液进行了以下探究: (1)、小红认为此时烧杯中的溶液可能有以下三种情况:①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸有剩余。小明同学却判定不可能“氢氧化钠有剩余”,他的理由是。(2)、他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写下表:
(1)、小红认为此时烧杯中的溶液可能有以下三种情况:①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸有剩余。小明同学却判定不可能“氢氧化钠有剩余”,他的理由是。(2)、他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写下表:实验方法
可能观察到的现象
结论
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中
盐酸过量
无明显现象
盐酸与氢氧化钠恰好完全反应
(3)、经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的,你认为其中错误的是(填序号)。A生锈的铁钉 B碳酸钠粉末 C硫酸钠粉末 D氢氧化铜
(4)、下列曲线能够表示小红所做实验中溶液pH变化趋势的是(填序号)。 (5)、小红在完成实验的过程中看到有气泡冒出,你猜测的原因是。为证实自己的猜想是正确的,小红在向试管中取样后,还需要滴加 , (填两种种类不同的物质名称)。
(5)、小红在完成实验的过程中看到有气泡冒出,你猜测的原因是。为证实自己的猜想是正确的,小红在向试管中取样后,还需要滴加 , (填两种种类不同的物质名称)。四、计算题
-
19. 实验小组同学利用实验室制取二氧化碳的反应原理来测定一瓶标签残缺的稀盐酸的溶质质量分数。取大理石15.0g,向其中加入100.0g该稀盐酸,恰好完全反应,测得剩余物质的质量为110.6g.试计算该稀盐酸的溶质质量分数。