北京市平谷区2021年中考化学一模试卷
试卷更新日期:2021-06-23 类型:中考模拟
一、单选题
-
1. 下列物质的性质,属于化学性质的是( )A、颜色 B、密度 C、可燃性 D、沸点2. 地壳中含量最高的元素是( )A、氧 B、铝 C、硅 D、铁3. “含氟牙膏”中的“氟”指的是( )A、分子 B、原子 C、离子 D、元素4. 发酵粉的主要成分是碳酸氢钠,它的俗称是( )A、烧碱 B、纯碱 C、小苏打 D、熟石灰5. 铁元素是人体必需微量元素,缺铁会导致( )A、佝偻病 B、贫血 C、坏血病 D、骨质疏松6. 下列含金属元素的物质是( )A、H2SO4 B、Al2O3 C、NO2 D、P2O57. 铁丝在氧气中燃烧的实验现象描述错误的是( )A、生成四氧化三铁 B、火星四射 C、放出大量的热 D、生成黑色固体8. 下表是日常生活中常见物质的pH,其中碱性最强的是( )A、酱油(4~5) B、牛奶(6~7) C、鸡蛋清(7~8) D、炉具清洁剂(12~13)9. 下列金属不能与CuSO4溶液反应的是( )A、Ag B、Fe C、Zn D、Al10. 下列净化水的操作,单一操作相对净化程度较高的是( )A、沉淀 B、过滤 C、消毒 D、蒸馏11. 下列方法能区分氧气和二氧化碳两瓶气体的是( )A、闻气味 B、观察颜色 C、倒入适量氢氧化钠溶液 D、将燃着的木条伸入集气瓶中12. 下列物质中能够放入可回收垃极箱的是( )A、旧书、旧报纸 B、果皮 C、口香糖 D、鱼骨头13. 实验室蒸发食盐水,不需要用到的仪器是( )A、蒸发皿 B、玻璃棒 C、酒精灯 D、漏斗14. 一种铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为( )A、58 B、24 C、82 D、14015. 下列实验操作正确的是()A、
 取用固体
B、
取用固体
B、 滴加液体
C、
滴加液体
C、 加热液体
D、
加热液体
D、 检查气密性
16. 下列不属于新能源的是( )A、
检查气密性
16. 下列不属于新能源的是( )A、 煤
B、
煤
B、 风能
C、
风能
C、 太阳能
D、
太阳能
D、 地热能
17. 下列物质含有氢分子的是()A、H2 B、H2O2 C、H2CO3 D、H2O18. 下列关于物质用途的描述错误的是( )A、铜丝可用作导线 B、生石灰可用作食品干燥剂 C、大理石可用作建筑材料 D、氢氧化钠可用于治疗胃酸过多症19. 下列物质不需密封保存的是( )A、氯化钠 B、烧碱 C、浓硫酸 D、浓盐酸20. 用下图装置进行实验。下列现象能证明空气中O2的含量的是( )
地热能
17. 下列物质含有氢分子的是()A、H2 B、H2O2 C、H2CO3 D、H2O18. 下列关于物质用途的描述错误的是( )A、铜丝可用作导线 B、生石灰可用作食品干燥剂 C、大理石可用作建筑材料 D、氢氧化钠可用于治疗胃酸过多症19. 下列物质不需密封保存的是( )A、氯化钠 B、烧碱 C、浓硫酸 D、浓盐酸20. 用下图装置进行实验。下列现象能证明空气中O2的含量的是( )
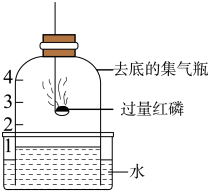 A、红磷燃烧,产生白烟 B、瓶中液面先下降,后上升 C、瓶中液面最终上升至1处 D、水槽中液面下降21. 根据图所示实验,不能达到实验目的的是( )A、
A、红磷燃烧,产生白烟 B、瓶中液面先下降,后上升 C、瓶中液面最终上升至1处 D、水槽中液面下降21. 根据图所示实验,不能达到实验目的的是( )A、 检验CH4燃烧生成CO2和H2O
B、
检验CH4燃烧生成CO2和H2O
B、 探究分子在不断运动
C、
探究分子在不断运动
C、 稀释浓硫酸
D、
稀释浓硫酸
D、 区分硬水和软水
22. 如图所示,将二氧化碳缓慢倒入烧杯中,蜡烛熄灭的主要原因是( )
区分硬水和软水
22. 如图所示,将二氧化碳缓慢倒入烧杯中,蜡烛熄灭的主要原因是( ) A、隔绝空气 B、移走可燃物 C、降低蜡烛的着火点 D、降低温度到蜡烛的着火点以下23. 利用催化剂可消除室内装修材料释放的甲醛,如图所示为该反应的微观示意图。下列说法错误的是( )
A、隔绝空气 B、移走可燃物 C、降低蜡烛的着火点 D、降低温度到蜡烛的着火点以下23. 利用催化剂可消除室内装修材料释放的甲醛,如图所示为该反应的微观示意图。下列说法错误的是( ) A、甲醛的化学式为CH2O B、生成物丙和丁质量比为22:9 C、生成物丙由1个碳原子和2个氧原子构成 D、参加反应的甲和生成的丁分子个数比为1:1
A、甲醛的化学式为CH2O B、生成物丙和丁质量比为22:9 C、生成物丙由1个碳原子和2个氧原子构成 D、参加反应的甲和生成的丁分子个数比为1:1二、综合题
-
24. 下表是 NaOH、Na2CO3、NaCl 的溶解度。依据表中数据和实验回答以下问题。
温度/℃
NaOH
Na2CO3
NaCl
20
109g
21.8g
36.0g
30
119g
39.7g
36.3g
20℃时,向下列 3 只盛有 100g 水的烧杯中,分别加入 30g 三种固体,充分溶解。
 (1)、上述溶液为饱和溶液的是( )A、② B、①③ C、②③ D、①②③(2)、将②加热至 30℃,溶液的溶质质量分数( )A、变小 B、变大 C、不变 D、无法判断25.(1)、为保障主会场、酒店及周边5000户居民的需求,共修建7条天然气管线。天然气主要成分燃烧的化学方程式为。(2)、早露蟠桃在休闲大会期间将进入盛果期,届时将以鲜桃款待中外游客,蟠桃富含的营养素是。
(1)、上述溶液为饱和溶液的是( )A、② B、①③ C、②③ D、①②③(2)、将②加热至 30℃,溶液的溶质质量分数( )A、变小 B、变大 C、不变 D、无法判断25.(1)、为保障主会场、酒店及周边5000户居民的需求,共修建7条天然气管线。天然气主要成分燃烧的化学方程式为。(2)、早露蟠桃在休闲大会期间将进入盛果期,届时将以鲜桃款待中外游客,蟠桃富含的营养素是。 (3)、金海湖国际会展中心是休闲大会主场馆,其主体钢结构的主要成分是铁,写出一氧化碳还原氧化铁的化学方程式为。在钢材中加入铬元素可增强抗腐蚀能力。研究铬含量对某钢材腐蚀程度的影响,测定结果如图,可得到的结论是。
(3)、金海湖国际会展中心是休闲大会主场馆,其主体钢结构的主要成分是铁,写出一氧化碳还原氧化铁的化学方程式为。在钢材中加入铬元素可增强抗腐蚀能力。研究铬含量对某钢材腐蚀程度的影响,测定结果如图,可得到的结论是。 26.(1)、“沉睡三千年,一醒惊天下”,我国三星堆遗址最新出土的金面具备受瞩目。该面具为一整块金箔制作,最薄处仅有0.2毫米,这说明金属具有良好的性。
26.(1)、“沉睡三千年,一醒惊天下”,我国三星堆遗址最新出土的金面具备受瞩目。该面具为一整块金箔制作,最薄处仅有0.2毫米,这说明金属具有良好的性。 (2)、青铜是一种铜合金,本色原是“古铜色”,因组成的差别,锈蚀产物不相同,导致出土的青铜器呈现不同颜色。以下锈蚀产物的主要成分中属于氧化物的是。
(2)、青铜是一种铜合金,本色原是“古铜色”,因组成的差别,锈蚀产物不相同,导致出土的青铜器呈现不同颜色。以下锈蚀产物的主要成分中属于氧化物的是。A红色:Cu2O B黑色:Cu2S C绿色:
27.(1)、新疆是我国棉花的主要产地,所产棉花纤维柔长、洁白有光,是棉花中的上品。棉花属于(填“天然纤维”或“合成纤维”)。(2)、熔喷布是口罩最核心的材料,主要以聚丙烯为主要原料。聚丙烯是丙烯通过加聚反应而成的聚合物,丙烯(C3H8)中碳、氢元素的质量比为。28. 用图装置进行实验。实验时,先将浓氢氧化钠溶液挤入盛有CO2的试管中,振荡;然后将止水夹K打开。 (1)、A中发生反应的化学方程式为。(2)、打开止水夹 K后,试管A中观察到的现象是。29. 阅读下面科普短文。
(1)、A中发生反应的化学方程式为。(2)、打开止水夹 K后,试管A中观察到的现象是。29. 阅读下面科普短文。自热火锅、自热米饭发热包的主要成分是:焙烧硅藻土、铁粉、铝粉、焦炭粉、活性炭、生石灰、盐、氢化钙(CaH2)等。往发热包中加水,放热原理主要包括生石灰与水反应快速放热、原电池(金属粉、碳粉、盐)反应持续放热、金属发生氧化反应和金属氧化物发生反应放热。硅藻土孔隙较大,可起到缓冲反应的作用,为发热包的安全性提供保障,氢化钙能与水反应(生成氢氧化钙和氢气)用来吸收渗入包装内的微量水分,防止氧化钙逐渐失效。
表为不同发热剂(均为30g)对不同食物加热效果表(加热时间为5min),图为自热米饭在不同测温点的温度变化曲线。
试剂种类
理论放热量/kJ
矿泉水(250g)
八宝粥(250g)
△T/℃
吸热量/kJ
△T/℃
吸热量/kJ
H2O(30g)+MgCl2
43.48
25
26.17
22
20.14
H2O(30g)+Al2(SO4)3
45.53
26
27.21
23
21.06
H2O(30 g)+ AlCl3
73.29
38
39.77
32
29.31
注:△T=加热后食物温度一加热前温度

使用加热包加热时应该注意:发热包中反应较为复杂,会产生一定量的氢气和一氧化碳;加热过程中,要将自热锅盖上的透气孔打开;发热包里不能改加热水;不能在汽车等密闭、狭小环境中使用,使用时避免明火;使用后的发热包按有害垃圾分类处置。
依据文章内容,回答下列问题:
(1)、发热包中所含硅藻土的作用是。(2)、表中等量的八宝粥与矿泉水比较,八宝粥的吸热量更(填“高”或“低”)。(3)、写出氢化钙(CaH2)与水反应的化学方程式。(4)、推测发热包里不能改加热水的原因是。(5)、阅读文章,下列说法错误的是(填序号)。A动车上可以多人同时制作不同口味的自热火锅
B为快速使自热火锅升温,应密封锅盖上的透气孔
C自热米饭“自热”后保温时间极短,“自热”后需立即食用
D等质量的MgCl2和AlCl3作发热剂为相同食物加热时,AlCl3“发热”效果更好
30. 以镁矿石(主要成分MgCO3、SiO2)为原料生产MgO的主要工艺流程如下: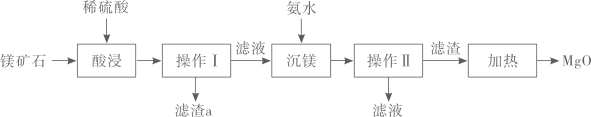
已知:SiO2难溶于水和常见的酸;“沉镁”过程中有Mg(OH)2生成。
(1)、操作Ⅰ、Ⅱ的名称是。(2)、滤渣a的主要成分是(填化学式);(3)、“酸浸”时稀硫酸与镁矿石主要成分发生反应的化学方程式是。(4)、“加热”过程中发生反应(填基本反应类型)。31. 高锰酸钾是一种重要的化工产品,在化学、生产、生活等场境中都有重要的用途。某工厂生产高锰酸钾的流程如图所示。
请回答下列问题:
(1)、I中混合加热时发生了变化(填“物理”或“化学”)。(2)、请将Ⅱ中发生反应的化学方程式补充完整。(3)、Ⅲ中反应前后化合价发生变化的元素有Mn和。32. 用图装置进行实验(夹持仪器略去;气密性已检验)。 (1)、高锰酸钾分解的化学方程式为。(2)、能说明木炭燃烧产物为二氧化碳的现象是。33. 用图所示实验装置进行实验。
(1)、高锰酸钾分解的化学方程式为。(2)、能说明木炭燃烧产物为二氧化碳的现象是。33. 用图所示实验装置进行实验。 (1)、试管1中生成的气体为。(2)、该反应的化学方程式为。34. 用如图装置进行二氧化碳的制取和性质实验。
(1)、试管1中生成的气体为。(2)、该反应的化学方程式为。34. 用如图装置进行二氧化碳的制取和性质实验。 (1)、A处发生反应的化学方程式为;(2)、能证明二氧化碳与水反应的实验现象是。35. 从图选择仪器,配制90 g溶质质量分数为10%的NaCl溶液。
(1)、A处发生反应的化学方程式为;(2)、能证明二氧化碳与水反应的实验现象是。35. 从图选择仪器,配制90 g溶质质量分数为10%的NaCl溶液。 (1)、需要称量NaCl的质量为 g。(2)、图中还缺少的玻璃仪器是。(3)、若将NaCl转移至烧杯中时有部分固体洒出,则会使配制的溶液溶质质量分数(填“偏大”“偏小”或“不变”)。36. 如图所示,在白色点滴板1-6的孔穴中,分别滴加适量稀盐酸。
(1)、需要称量NaCl的质量为 g。(2)、图中还缺少的玻璃仪器是。(3)、若将NaCl转移至烧杯中时有部分固体洒出,则会使配制的溶液溶质质量分数(填“偏大”“偏小”或“不变”)。36. 如图所示,在白色点滴板1-6的孔穴中,分别滴加适量稀盐酸。 (1)、反应后溶液颜色有变化的是(填序号)。(2)、孔穴3中发生反应的化学方程式为。(3)、再向孔穴4中滴加氢氧化钠溶液,溶液不变色,此时溶液中一定有的溶质是。37. 请从A~D中任选三个作答,若均作答,按前三个计分。如图,在Y形管中进行实验。补全实验方案。
(1)、反应后溶液颜色有变化的是(填序号)。(2)、孔穴3中发生反应的化学方程式为。(3)、再向孔穴4中滴加氢氧化钠溶液,溶液不变色,此时溶液中一定有的溶质是。37. 请从A~D中任选三个作答,若均作答,按前三个计分。如图,在Y形管中进行实验。补全实验方案。
序号
目的
操作
现象
结论
A
探究金属活动性
A:放入铁片;
B:放入铜片;
向A、B处加入
A中有气泡产生,溶液变为浅绿色;B中无明显变化
金属活动性:铁>铜
B
验证可燃物的燃烧条件
A、B分别加入等量红磷,
用酒精灯在A底部加热
A中红磷燃烧;
B中红磷无明显变化
C
探究分子的性质
A:滴入几滴酚酞溶液;
B:滴入几滴浓氨水;
并塞紧橡胶塞
分子在不断运动
D
比较
A:加入5mL水;
B:加入5mL酒精;
再向其中各加入一小粒碘
A中固体几乎不溶解;B中固体溶解形成红棕色溶液
相同条件下,碘在酒精中的溶解能力比在水中强
38. 化学小组同学在查阅温室效应的相关资料时,了解到除了二氧化碳外,水蒸气等气体也能产生温室效应。(实验目的)验证二氧化碳是温室气体并探究水蒸气的温室效应。
(查阅资料)硅胶和浓硫酸均具有吸水性,可用作某些气体的干燥剂。
(实验设计)用太阳灯模拟日光,对气体进行照射,利用温度传感器采集瓶内气体温度数据。
(实验准备)利用如图装置收集气体。
编号
1
2
3
4
实验装置




(进行实验)甲同学利用编号为1、3、4的实验装置,收集三瓶气体进行实验,结果如图1所示(曲线序号与上述装置编号一致);乙同学利用编号为1、2、4的实验装置,收集三瓶气体进行实验,结果如图2所示。

(解释与结论)
(1)、能用向上排空气法收集CO2的原因。(2)、编号为3的实验装置连接顺序为a→→d 。(3)、甲同学实验中选择1、3号气体的目的是。(4)、乙同学得到“水蒸气可以引起温室效应”的结论,其依据的曲线是(填序号)。(5)、(反思与评价)通过分析,甲、乙两位同学的实验均能达到实验目的,你认为利用编号进行实验也可以。
(6)、下列降低大气中二氧化含量的措施中,合理的是(填序号)。A开发利用新能源 B植树造林
C二氧化碳循环利用 D禁止使用化石燃料
三、计算题
-
39. 84消毒液是家庭常用的消毒产品,有效成分是次氯酸钠(NaClO),其工业制法的反应原理是: 。计算:将142gCl2通入足量NaOH溶液中,求可制得多少g次氯酸钠?