河北省唐山市2021年高考化学三模试卷
试卷更新日期:2021-06-17 类型:高考模拟
一、单选题
-
1. 化学与生活、社会发展息息相关。下列说法错误的是( )A、将生活垃圾分类投放,分类处理 B、“世间丝、麻、裘皆具素质……”,这里丝、麻的主要成分是蛋白质 C、三星堆发现的金箔,体现了金属的延展性 D、“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应2. 代表阿伏加德罗常数的值。下列说法正确的是( )A、将0.1 溶于足量水,转移的电子总数为0.1 B、常温常压下,36g 中所含的中子数为18 C、2.24L(标准状况)乙烯被溴的四氯化碳溶液完全吸收,断裂的共价键总数为0.1 D、7.8g 与 的混合物中,离子总数为0.33. 下列离子方程式正确的是( )A、 溶液中通入少量氯气: B、石灰石溶于醋酸: C、 与足量 溶液反应: D、钠与水反应:4. 下列实验设计能达到实验目的的是( )
 A、①用于测量氯水的 B、②可以探究正戊烷( )催化裂化 C、③可用于探究温度对 平衡移动的影响 D、④用 溶液制备 晶体5. 下列实验目的对应的实验操作和实验原理均正确的是( )
A、①用于测量氯水的 B、②可以探究正戊烷( )催化裂化 C、③可用于探究温度对 平衡移动的影响 D、④用 溶液制备 晶体5. 下列实验目的对应的实验操作和实验原理均正确的是( )实验目的
实验操作
实验原理
A
提纯混有少量硝酸钾的氯化钠
在较高温度下制得浓溶液再冷却结晶、过滤、干燥
氯化钠溶解度随温度升高变化不大,而硝酸钾溶解度随温度升高显著增大
B
比较 、 的 相对大小
向 的 溶液中加入 溶液,再滴加5~6滴 溶液,观察沉淀的生成及其颜色的变化
C
探究化学反应的限度
取 的 溶液,滴加 溶液5~6滴,充分反应,观察
根据溶液中既含 又含 的实验事实判断该反应是可逆反应
D
检验溶液中是否含有
取少量试液于试管中,加入 溶液并加热,用湿润的红色石蕊试纸检验产生的气体
溶于水后溶质的主要存在形式是 、
A、A B、B C、C D、D6. 从海水中提取溴的工业流程如图,下列说法错误的是( ) A、海水晒盐利用的是蒸发结晶法 B、步骤I利用了氯气的强氧化性 C、步骤II中溴与碳酸钠反应中氧化剂与还原剂物质的量之比为1:1 D、实验室分离溴还可以用溶剂萃取法,四氯化碳可以用作溴的萃取剂7. 温度 ℃,反应 中所有物质均为气态。在起始温度、体积相同( ℃、2L密闭容器)时,发生反应的部分数据见下表:
A、海水晒盐利用的是蒸发结晶法 B、步骤I利用了氯气的强氧化性 C、步骤II中溴与碳酸钠反应中氧化剂与还原剂物质的量之比为1:1 D、实验室分离溴还可以用溶剂萃取法,四氯化碳可以用作溴的萃取剂7. 温度 ℃,反应 中所有物质均为气态。在起始温度、体积相同( ℃、2L密闭容器)时,发生反应的部分数据见下表:反应条件
反应时间
反应Ⅰ:
恒温恒容
0
2
6
0
0
10
4.5
20
1
30
1
反应Ⅱ:
绝热恒容
0
0
0
2
2
下列说法正确的是( )
A、对反应I,前10 内的平均反应速率 B、在其他条件不变的情况下,若30 时只向容器中再充入1 和1 ,则平衡正向移动 C、对于反应I,进行30 时, 所占的体积分数为30% D、达到平衡时,反应I、II对比:平衡常数8. 以 为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
下列说法正确的是( )
A、过程①中钛氧键断裂会释放能量 B、该反应中,光能和热能转化为电能 C、使用 作催化剂可以降低反应的活化能,从而提高化学反应速率 D、 分解反应的热化学方程式为9. 工业上利用 对烟道气进行脱硝(除氮氧化物)的 技术具有效率高、性能可靠的优势。 技术的原理为 和 在催化剂( )表面转化为 和 ,反应进程中的相对能量变化如图所示。下列说法正确的是( ) A、总反应方程式为 B、 是脱硝反应的催化剂 C、升高温度,脱硝反应的正反应速率的增大程度大于其逆反应速率的增大程度 D、决定反应速率的步骤是“ 的转化”10. 全钒液流电池是目前最成熟的电池技术,该电池是将具有不同价态的钒离子溶液分别作为正极和负极的活性物质,储存在各自的酸性电解液储罐中。其结构原理如图所示:
A、总反应方程式为 B、 是脱硝反应的催化剂 C、升高温度,脱硝反应的正反应速率的增大程度大于其逆反应速率的增大程度 D、决定反应速率的步骤是“ 的转化”10. 全钒液流电池是目前最成熟的电池技术,该电池是将具有不同价态的钒离子溶液分别作为正极和负极的活性物质,储存在各自的酸性电解液储罐中。其结构原理如图所示:
下列有关电池叙述错误的是( )
A、放电时,电子由a经负载流向b B、放电时,电池总反应为: C、充电时,阴极电极反应式为: D、充电时, 由右侧电极室经交换膜移向左侧二、多选题
-
11. 短周期主族元素X、Y、Z、W原子序数依次增大,X与Z可以形成两种常见液态化合物,W的原子半径在矩周期主族元素中最大,由Y、Z、W三种元素形成的化合物A的结构如图所示。下列叙述错误的是( )
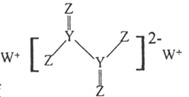 A、Y的氢化物沸点一定低于Z的氢化物 B、X与Z可能形成由极性键与非极性键构成的极性分子 C、化合物 可以与乙二醇在一定条件下发生缩聚反应 D、0.1 化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是0.112. 根皮素常用于治疗分泌旺盛型粉刺,同时对各种皮肤色斑有淡化作用。关于该有机物下列说法正确的是( )
A、Y的氢化物沸点一定低于Z的氢化物 B、X与Z可能形成由极性键与非极性键构成的极性分子 C、化合物 可以与乙二醇在一定条件下发生缩聚反应 D、0.1 化合物A与足量酸性高锰酸钾溶液完全反应转移电子数是0.112. 根皮素常用于治疗分泌旺盛型粉刺,同时对各种皮肤色斑有淡化作用。关于该有机物下列说法正确的是( ) A、该有机物易溶于水和 B、该有机物能发生取代反应和加成反应 C、该有机物分子中所有碳原子可能在同一平面 D、该有机物与 溶液反应可以生成 气体13. 常温下,向 溶液中逐滴加入0.2 溶液10.0 ,溶液中微粒的物质的量(挥发的 未画出)随 的变化如下图所示。下列说法正确的是( )
A、该有机物易溶于水和 B、该有机物能发生取代反应和加成反应 C、该有机物分子中所有碳原子可能在同一平面 D、该有机物与 溶液反应可以生成 气体13. 常温下,向 溶液中逐滴加入0.2 溶液10.0 ,溶液中微粒的物质的量(挥发的 未画出)随 的变化如下图所示。下列说法正确的是( ) A、随着盐酸的加入,溶液中水的电离程度先减小后增大 B、 的水解常数 的数量级约为 C、a点对应溶液中离子浓度: D、b点对应溶液中:
A、随着盐酸的加入,溶液中水的电离程度先减小后增大 B、 的水解常数 的数量级约为 C、a点对应溶液中离子浓度: D、b点对应溶液中:三、非选择题
-
14. 某研究小组用炼锌废渣制备 。炼锌产生的废渣中含钴10~18%、锌15~20%左右,还含有少量锰、铁、铜、镉等金属。
 已知: (1)、滤渣1的成分是 , 提高“酸浸”浸出率的措施有。(任写一条措施)(2)、“控电位浸出”是控制合适的氧化电位电解除锰,将溶液中 变为 除去,写出阳极电极反应式。(3)、已知浸出液含金属离子为 、 、 、 ,试剂a是 和 的悬浊液,试剂a除铁的原理是(文字表述);滤渣2成分是。(写化学式)(4)、“沉钴”的离子方程式是 , 该步骤选择 ,而不用 的原因是。(5)、 与 按一定比例在700℃下烧结,可得重要的电极材料钴酸锂( ),烧结反应化学方程式是。15. 某课外小组探究食品添加剂 (焦亚硫酸钠)制备原理,实验操作如下:
已知: (1)、滤渣1的成分是 , 提高“酸浸”浸出率的措施有。(任写一条措施)(2)、“控电位浸出”是控制合适的氧化电位电解除锰,将溶液中 变为 除去,写出阳极电极反应式。(3)、已知浸出液含金属离子为 、 、 、 ,试剂a是 和 的悬浊液,试剂a除铁的原理是(文字表述);滤渣2成分是。(写化学式)(4)、“沉钴”的离子方程式是 , 该步骤选择 ,而不用 的原因是。(5)、 与 按一定比例在700℃下烧结,可得重要的电极材料钴酸锂( ),烧结反应化学方程式是。15. 某课外小组探究食品添加剂 (焦亚硫酸钠)制备原理,实验操作如下:实验步骤
实验操作
第一步
连接实验装置并检查装置气密性
第二步
A、C、D中装入药品,加热A中试管,通过pH数据采集器控制C中反应至 时停止加热,将A中铜丝外移脱离浓硫酸;
第三步
将C中所得溶液转移至蒸发装置中,加热,结晶脱水、过滤、洗涤、干燥制得焦亚硫酸钠( )。
已知: ; ,实验装置如下:

回答下列问题:
(1)、写出A中反应的化学方程式为。装置B的作用是。(2)、第二步控制C中 ,若C中溶质只有一种,C中反应的离子方程式是。(3)、第三步加热过程中若温度过高可能会生成 和M两种正盐,M的化学式是 , 鉴别M中阴离子的方法是 , 过滤操作用到的玻璃仪器有。(4)、用于D处合理的装置是(填标号)。 (5)、该小组通过下述方法检测某饮料中残留的 :
(5)、该小组通过下述方法检测某饮料中残留的 :①取100.00 饮料于锥形瓶中,加入 的 溶液,塞紧瓶塞充分反应。
②打开瓶塞,将锥形瓶内液体调至接近中性,滴加4~5滴淀粉溶液变蓝。用 的 溶液滴定,滴定至终点时,消耗 ;溶液39.80 ,饮料中残留的 为 (计算结果保留两位小数)。
16. 某科研组对 气体深入研究,发现 很不稳定,经过实践提出如下反应机理:回答下列问题
(1)、 。(2)、①已知 ,起始时 为35.8 ,分解的反应速率 。恒温恒容时, 测得体系中 ,则此时的分解的反应速率 。②T温度时,向2L密闭容器中加入 , 时 完全分解,体系达平衡状态,气体压强是反应前的2倍,则该温度下 的平衡常数K=。
③ ,在体积均为 的容器中,不同温度下二氧化氮浓度变化与反应时间的关系如图所示,下列说法错误的是(填标号)。
 A.
A. B.a点逆反应速率小于c点正反应速率
c。 ℃ 10 时二氧化氮速率为0.05
D. ℃ 20 时改变的条件可能是充入一定量的
(3)、①氯气和硝酸银在无水环境中可制得 ,同时得到一种气态单质A,该反应的化学方程式是。②Peter提出了一种用惰性电极作阳极硝酸电解脱水法制备 ,其原理如下图所示。阳极制得 和A,其电极反应式为。每生成1 ,两极共产生气体L(标准状况下)。
 17. 青铜器是我国古代瑰宝。目前,在工业上用磷化铜( )制造磷青铜,磷青铜是含少量钪、锡、磷的铜合金,主要用作耐磨零件和弹性合金原件。(1)、基态 原子的核外电子排布式为;其价电子中未成对电子数与成对电子数之比为。(2)、① 中的P原子的杂化方式是。
17. 青铜器是我国古代瑰宝。目前,在工业上用磷化铜( )制造磷青铜,磷青铜是含少量钪、锡、磷的铜合金,主要用作耐磨零件和弹性合金原件。(1)、基态 原子的核外电子排布式为;其价电子中未成对电子数与成对电子数之比为。(2)、① 中的P原子的杂化方式是。②P与N同主族,气态氢化物的沸点: (填“>”或“<”),说明理由:。
(3)、磷青铜中的锡、磷两种元素电负性的大小为 P(填“>”“<”或“=”)。(4)、某立方磷青铜晶胞结构如下图所示。
①则其化学式为。
②该晶体中距离 原子最近的 原子有个,在晶胞中由 原子构成的八面体与由 和 原子构成的八面体的个数之比为。
③若晶体密度为 ,最近的 原子核间距为 (用含 、 的代数式表示)。
18. 以有机物A为原料制备离子交换树脂M和新型聚酯材料N等的合成路线如下: 已知:①
已知:① 

②
 OHCR’
OHCR’③H结构中含有一个甲基。
(1)、A的结构简式为 , 反应③的反应类型是;F中含氧官能团的名称是。(2)、E与新制 浊液反应的化学方程式是。(3)、下列关于D的说法正确的是(填字母序号)。a.不溶于水b.能与 发生还原反应
c.能被酸性重铬酸钾溶液氧化d.与金属 发生置换反应
(4)、H的结构简式为;同时符合下列条件的H的同分异构体有种。(不考虑顺反异构)①苯环上有两个取代基;②含有碳碳双键;③能发生银镜反应。
(5)、反应②的化学方程式为。(6)、模仿上述反应,写出由环己烯和其它无机试剂(任选)三步制取1,6-己二醛的流程图:。