北京市海淀区2021年高考化学二模试卷
试卷更新日期:2021-06-17 类型:高考模拟
一、单选题
-
1. 下列安全标识不适合在加油站张贴的是( )A、
 B、
B、 C、
C、 D、
D、 2. 下列化学用语正确的是( )A、氨的电子式:
2. 下列化学用语正确的是( )A、氨的电子式: B、中子数为20的Cl的核素:
C、甲烷的球棍模型:
B、中子数为20的Cl的核素:
C、甲烷的球棍模型:  D、
D、 ,的系统命名:3-甲基-2-丁醇
3. 下列说法错误的是( )A、水泥、玻璃和陶瓷均属于无机非金属材料 B、麦芽糖在酸或酶的催化下可水解为葡萄糖 C、煤的干馏是实现煤综合利用的主要途径之一 D、利用油脂在碱性条件下的水解反应可获得人造脂肪4. 某品牌牙膏的成分含水、丙三醇、二氧化硅、苯甲酸钠、十二烷基硫酸钠和氟化钠等。已知:牙釉质中含有羟基磷酸钙 ,是牙齿的保护层。在牙齿表面存在平衡:
,的系统命名:3-甲基-2-丁醇
3. 下列说法错误的是( )A、水泥、玻璃和陶瓷均属于无机非金属材料 B、麦芽糖在酸或酶的催化下可水解为葡萄糖 C、煤的干馏是实现煤综合利用的主要途径之一 D、利用油脂在碱性条件下的水解反应可获得人造脂肪4. 某品牌牙膏的成分含水、丙三醇、二氧化硅、苯甲酸钠、十二烷基硫酸钠和氟化钠等。已知:牙釉质中含有羟基磷酸钙 ,是牙齿的保护层。在牙齿表面存在平衡:
下列说法错误的是( )
A、若使牙膏呈弱酸性,更有利于保护牙釉质 B、丙三醇的俗称是甘油 C、 是摩擦剂,有助于去除牙齿表面的污垢 D、NaF能将 转化为更难溶的 ,减少龋齿的发生5. 用下列仪器或装置进行相应实验,能达到实验目的的是( )



A.蒸发结晶制备 晶体
B.分离苯和溴苯
C.实验室制取蒸馏水
D.配制100mL 溶液
A、A B、B C、C D、D6. 下列方程式与所给事实不相符的是( )A、向 酸性溶液中滴加 溶液,溶液褪色: B、向沸水中滴加饱和 溶液, 胶体: C、向银氨溶液中滴加乙醛,水浴加热,析出光亮银镜: D、 用作潜水艇供氧剂: ;7. 下表是周期表中5种元素的相关信息,其中Q、W、X位于同一周期。元素
信息
元素
信息
Q
位于周期表的第3周期第ⅢA族
Y
焰色反应为紫色
W
最高正化合价为+7价
Z
原子结构示意图为

X
本周期中原子半径最大
下列说法正确的是( )
A、Q在地壳中含量最高 B、元素的金属性: C、气态氢化物的稳定性: D、Q的最高价氧化物对应的水化物既能与NaOH反应,又能与HCl反应8. 糠醛( )与苯酚可以发生聚合反应,得到糠醛树脂,其结构类似于酚醛树脂,糠醛树脂可用作砂轮、砂纸、砂布的黏合剂。下列说法错误的是( ) A、糠醛的分子式为 B、糠醛的同分异构体可能含羧基 C、合成糠醛树脂的反应属于缩聚反应 D、线型糠醛树脂的结构简式为
)与苯酚可以发生聚合反应,得到糠醛树脂,其结构类似于酚醛树脂,糠醛树脂可用作砂轮、砂纸、砂布的黏合剂。下列说法错误的是( ) A、糠醛的分子式为 B、糠醛的同分异构体可能含羧基 C、合成糠醛树脂的反应属于缩聚反应 D、线型糠醛树脂的结构简式为 9. 催化加氢制备 是 资源化利用的重要途径。已知下图所示的反应的能量变化。
9. 催化加氢制备 是 资源化利用的重要途径。已知下图所示的反应的能量变化。
下列说法错误的是( )
A、由图1推知反应物断键吸收的能量小于生成物成键释放的能量 B、图2中,若生成的 为液态,则能量变化曲线为① C、 D、制备 的反应使用催化剂时,其 不变10. 工业上用氨水作为沉淀剂去除酸性废水中的铅元素。除铅时,体系中含铅微粒的物质的量分数(d)与溶液pH的关系如图。[已知:Pb(OH)2难溶于水]
下列说法错误的是( )
A、氨水中: B、酸性废水中的含铅微粒有Pb2+、Pb(OH)+ C、 时,溶液中的离子有且仅有 和 D、 时,除铅效果最好11. 在体积恒为1L的密闭容器中发生反应: 。测得不同条件下A的平衡转化率a(A)如下表。实验序号
实验温度
初始投料量
1
10
10
50
2
10
10
a
3
15
10
40
下列说法正确的是( )
A、当容器内压强不变时,反应达到化学平衡状态 B、 时,反应的化学平衡常数值为2 C、若 ,则 D、12. 化学家利用“自然化学连接法”提高蛋白质合成的效率,反应机理如图(其中—和…各表示一种多肽片段)。下列说法错误的是( ) A、过程1中有 键和 键的断裂 B、a、b生成c的同时还生成RH C、c和d互为同分异构体 D、总反应的化学反应速率主要取决于过程213. 下图是“海水河水”浓差电池装置示意图(不考虑溶解氧的影响),其中a、b均为 复合电极,b的电极反应式为 。下列说法正确的是( )
A、过程1中有 键和 键的断裂 B、a、b生成c的同时还生成RH C、c和d互为同分异构体 D、总反应的化学反应速率主要取决于过程213. 下图是“海水河水”浓差电池装置示意图(不考虑溶解氧的影响),其中a、b均为 复合电极,b的电极反应式为 。下列说法正确的是( ) A、a的电极反应式为 B、内电路中, 由b极区向a极区迁移 C、工作一段时间后,两极NaCl溶液的浓度差减小 D、电路中转移 时,理论上a极区模拟海水的质量减少23g14. 同学们探究不同金属和浓硫酸的反应。向三等份浓硫酸中分别加入大小相同的不同金属片,加热,用生成气体进行下表实验操作并记录实验现象。
A、a的电极反应式为 B、内电路中, 由b极区向a极区迁移 C、工作一段时间后,两极NaCl溶液的浓度差减小 D、电路中转移 时,理论上a极区模拟海水的质量减少23g14. 同学们探究不同金属和浓硫酸的反应。向三等份浓硫酸中分别加入大小相同的不同金属片,加热,用生成气体进行下表实验操作并记录实验现象。实验操作
实验现象
金属为铜
金属为锌
金属为铝
点燃
不燃烧
燃烧
燃烧
通入 酸性溶液
褪色
褪色
褪色
通入 溶液
无明显变化
无明显变化
出现黑色沉淀
通入品红溶液
褪色
褪色
不褪色
已知: (CuS为黑色固体); 可燃
下列说法错误的是( )
A、加入铜片的实验中,使 酸性溶液褪色的气体是 B、加入铝片的实验中,燃烧现象能证明生成气体中一定含 C、加入锌片的实验中,生成的气体一定是混合气体 D、金属与浓硫酸反应的还原产物与金属活动性强弱有关二、非选择题
-
15. 氧族元素(O、S、Se等)及其化合物在生产生活中发挥着巨大作用。(1)、实验室用 溶液和 粉末在常温下反应制备 ,装置如图。

①将虚线框a内的仪器补充完整(夹持装置可省略)。
②b为尾气吸收装置,其中的试剂为。
(2)、生物浸出法可有效回收含硫矿石中的有色金属,某种生物浸出法中主要物质的转化路径如图。
①步骤Ⅰ反应的离子方程式为。
②生物浸出法的总反应的氧化剂是。
(3)、以工业硒为原料制备高纯硒的流程如图。①下列说法正确的是(填字母序号)。
a.过程i到过程ⅲ均为氧化还原反应
b. 既有氧化性,又有还原性
c. 能与NaOH反应生成 和
d.Se与 化合比S与 化合容易
②过程ⅲ中使用的还原剂为 ,对应产物是 。理论上,过程i消耗的 与过程消耗的 的物质的量之比为(工业硒中杂质与 的反应可忽略)。
16. 实验小组探究不同浓度 溶液的电解反应。分别用石墨电极电解 溶液和 溶液,记录实验现象如下表。实验装置
实验编号及试剂
实验现象

① 溶液(蓝色)
阳极:产生有刺激性气味的气体
阴极:电极上有红色固体析出
② 溶液(绿色)
阳极:产生有刺激性气味的气体
阴极:电极上有少量红色固体和白色固体析出,同时电极附近液体变为黑色
(1)、经检验,阳极产生的气体能使湿润的淀粉KI试纸变蓝。①中电解反应的化学方程式为。(2)、Ⅰ.探究②中产生白色固体的原因。查阅资料:
i.阴极附近的白色固体为 ;
ii. 在水溶液中单独存在时不稳定,容易发生反应: 。
结合资料分析CuCl产生的路径有如下两种可能:
路径1:阴极发生电极反应分两步:
i.
ⅱ. ,同时伴随反应 ,生成白色沉淀。
(3)、路径2:阴极发生电极反应 ,而后发生反应a:(写出离子方程式),生成白色沉淀。同学们通过实验证明反应a可以发生,其实验操作和现象是。(4)、Ⅱ.探究②中阴极区液体中黑色物质的成分。进一步查阅资料,提出以下猜想。
猜想1.生成氢氧化铜,进而转化为极细小的氧化铜;
猜想2.生成铜的速率快,形成黑色纳米铜;
猜想3.发生反应 (棕黑色)。
若猜想1成立,则阴极一定还存在的电极反应是。
取2mL黑色液体于试管中,分别加入不同试剂,记录实验现象如下表。
实验编号
③
④
⑤
加入试剂
4mL浓
4mL浓HCl
实验现象
溶液变澄清,呈绿色,试管口有浅红棕色气体生成
黑色液体颜色变深
溶液变澄清,呈绿色,同时出现少量白色沉淀
(5)、甲同学根据实验③产生的现象得出结论:黑色液体中一定有纳米铜。乙同学认为甲同学的结论不合理,他做出判断的依据是。(6)、由上述实验可得到的关于黑色物质成分的结论是。17. 合理利用废旧铅蓄电池可缓解铅资源短缺,同时减少污染。(1)、Ⅰ.一种从废旧铅蓄电池的铅膏中回收铅的生产流程如下图(部分产物已略去)。
已知:①不同铅化合物的溶度积(25℃): ;
②PbSiF6和 均为能溶于水的强电解质。
过程i中,物质a表现(填“氧化”或“还原”)性。
(2)、过程ⅱ需要加入 溶液,从化学平衡的角度解释其作用原理:。(3)、过程ⅲ发生反应的离子方程式为。(4)、Ⅱ.工业上用PbSiF6、 混合溶液作电解液,用电解法实现粗铅(主要杂质为Cu、Ag、Fe、Zn,杂质总质量分数约为4%)提纯,装置示意图如下。
下列说法正确的是(填字母序号)。
a.阴极为粗铅,纯铅在阳极析出
b.电解产生的阳极泥的主要成分为Cu和Ag
c.工作一段时间后,需要补充Pb2+以保持溶液中c(Pb2+)的稳定
(5)、铅的电解精炼需要调控好电解液中的 。其他条件相同时,测得槽电压(槽电压越小,对应铅产率越高)随起始时溶液中 的变化趋势如图。由图可推知,随 增大,铅产率先增大后减小,减小的原因可能是。 18. 具有十八面体结构的Ag3PO4晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。(1)、Ⅰ.配位-沉淀法制备 高效光催化剂
18. 具有十八面体结构的Ag3PO4晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。(1)、Ⅰ.配位-沉淀法制备 高效光催化剂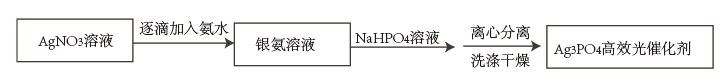
已知:i.Ag3PO4难溶于水,可溶于硝酸;
ii.Ag3PO4沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能;
iii.银氨溶液中存在:
配制银氨溶液时的反应现象是。
(2)、加入 溶液时,发生以下反应,请将离子方程式补充完整:□ +□+□=□NH3+□+□
(3)、 和 在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:。(4)、Ⅱ.Ag3PO4光催化剂的使用和再生已知:Ag3PO4晶体在光照条件下发挥催化作用时,首先引发反应。a.
Ag3PO4光催化CO2制备甲醇可实现“碳中和”,a的后续反应: , ,则由CO2制备甲醇的总反应的化学方程式为。
(5)、Ag3PO4光催化降解RhB(代表有机污染物),RhB被氧化成CO2和H2O。a的后续反应注:Ag3PO4在该催化过程中可能发生光腐蚀,生成单质银,影响其光催化性能。
用Ag3PO4依次降解三份相同的废水,测得3次降解过程中RhB的残留率( :即时浓度与起始浓度之比)随时间变化的曲线如图。
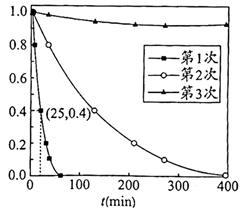
①下列说法正确的是(填字母序号)。
a. 和 是降解RhB的重要氧化剂
b.第1次使用后Ag3PO4的光催化性能降低
c.该实验条件下,Ag3PO4使用两次即基本失效
②第1次光降解时, 内的反应速率为 (废水中RhB初始浓度 为 ,RhB的摩尔质量为 )
19. 普瑞巴林(K)是一种抗癫痫药物,可用异戊二烯(A)为原料来合成,路线如图。 已知:i.RCHO+
已知:i.RCHO+ 
 +H2O
+H2Oii.
(1)、A的官能团是(写中文名称)。(2)、C的结构简式为。(3)、D→E的化学方程式是。(4)、F→G的反应类型为。(5)、I中含有一个六元环,H生成I的化学方程式是。(6)、若H未发生脱水缩合生成L根据H的酸性推断其直接与过量 反应的产物是。(7)、将K中的碳原子编号标记为 。其中由 提供的碳原子的编号为(填字母序号)
。其中由 提供的碳原子的编号为(填字母序号) a.1,2,3,4 b.1,3,4 c.2,3,4 d.1,2,3