重庆市2021年中考化学二模试卷
试卷更新日期:2021-06-11 类型:中考模拟
一、单选题
-
1. 春暖花开正是人们外出游玩的好时节。下列春游活动中一定发生化学变化的是( )A、漫步赏花 B、划船观湖 C、生火野炊 D、放飞风筝2. 生活中许多物质能给人体提供所需的营养素,下列物质中能为人体提供能量的是( )A、水 B、米饭 C、蔬菜 D、食盐3. “绿色生活”是一种低碳环保的生活理念,下列做法不符合该理念的是( )A、废旧电池分类回收 B、禁止使用化肥和农药 C、使用太阳能路灯,既节能又环保 D、多乘坐公共交通工具,减少尾气排放4. 下列实验操作正确且能达到实验目的的是( )A、
 稀释浓硫酸
B、
稀释浓硫酸
B、 测定pH
C、
测定pH
C、 称量10.05g固体
D、
称量10.05g固体
D、 量9.5mL液体
5. 下列不属于化石燃料的是()A、天然气 B、石油 C、煤 D、乙醇6. 下列关于氧气的说法正确的是( )A、液态氧可用作火箭的助燃剂 B、氧气在空气中的体积分数为78% C、硫在氧气中燃烧发出黄色火焰 D、鱼类能在水中生存,证明氧气易溶于水7. 将pH=10的氢氧化钠溶液加水稀释后,所得溶液的pH可能是( )A、6 B、8 C、11 D、148. 下列物质由离子构成的是( )A、二氧化碳 B、金刚石 C、氯化钠 D、硅9. 下列物质的用途主要利用其物理性质的是( )A、生石灰用作干燥剂 B、氮气常用作袋装食品的填充气 C、竹炭除冰箱中的异味 D、液氧用作火箭助燃剂10. 若用实验证明FeSO4溶液显浅绿色不是由 离子造成的,下列实验无意义的是( )A、观察K2SO4溶液的颜色 B、向FeSO4溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液浅绿色消失 C、向FeSO4溶液中滴加适量无色氯化钡溶液,振荡后静置,溶液浅绿色未消失 D、往FeSO4溶液中加水稀释,溶液颜色变浅11. 分别将下列各组物质同时加入水中,最终能得到无色透明溶液的是( )A、H2SO4(过量)、HCl、AgNO3 B、HCl(过量)、MgSO4、KOH C、HCl(过量)、KOH、CuSO4 D、KNO3(过量)、NaCl、BaCO312. 在混有少量CuO的铁粉中加入一定量的稀盐酸,充分反应过滤,再向滤液中放入一枚洁净的铁钉,足够时间后取出,铁钉表面无变化,下列判断正确的是( )A、过滤出的不溶物只有铜 B、过滤出的不溶物只有铁 C、过滤出的不溶物中一定含有铜,可能含有铁 D、滤液中一定含有氯化亚铁,可能含有氯化铜13. 如图为锶原子在元素周期表中的相关信息及锶原子的原子结构示意图,据此判断下列说法正确的是( )
量9.5mL液体
5. 下列不属于化石燃料的是()A、天然气 B、石油 C、煤 D、乙醇6. 下列关于氧气的说法正确的是( )A、液态氧可用作火箭的助燃剂 B、氧气在空气中的体积分数为78% C、硫在氧气中燃烧发出黄色火焰 D、鱼类能在水中生存,证明氧气易溶于水7. 将pH=10的氢氧化钠溶液加水稀释后,所得溶液的pH可能是( )A、6 B、8 C、11 D、148. 下列物质由离子构成的是( )A、二氧化碳 B、金刚石 C、氯化钠 D、硅9. 下列物质的用途主要利用其物理性质的是( )A、生石灰用作干燥剂 B、氮气常用作袋装食品的填充气 C、竹炭除冰箱中的异味 D、液氧用作火箭助燃剂10. 若用实验证明FeSO4溶液显浅绿色不是由 离子造成的,下列实验无意义的是( )A、观察K2SO4溶液的颜色 B、向FeSO4溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液浅绿色消失 C、向FeSO4溶液中滴加适量无色氯化钡溶液,振荡后静置,溶液浅绿色未消失 D、往FeSO4溶液中加水稀释,溶液颜色变浅11. 分别将下列各组物质同时加入水中,最终能得到无色透明溶液的是( )A、H2SO4(过量)、HCl、AgNO3 B、HCl(过量)、MgSO4、KOH C、HCl(过量)、KOH、CuSO4 D、KNO3(过量)、NaCl、BaCO312. 在混有少量CuO的铁粉中加入一定量的稀盐酸,充分反应过滤,再向滤液中放入一枚洁净的铁钉,足够时间后取出,铁钉表面无变化,下列判断正确的是( )A、过滤出的不溶物只有铜 B、过滤出的不溶物只有铁 C、过滤出的不溶物中一定含有铜,可能含有铁 D、滤液中一定含有氯化亚铁,可能含有氯化铜13. 如图为锶原子在元素周期表中的相关信息及锶原子的原子结构示意图,据此判断下列说法正确的是( )
 A、锶的原子序数为38 B、锶属于非金属元素 C、锶的相对原子质量是87.62g D、锶原子在化学反应中易得到电子14. 过氧碳酸钠(Na2CO4) 是一种新型氧系漂白剂。下列有关过氧碳酸钠的说法正确的是( )A、过氧碳酸钠由三个元素组成 B、过氧碳酸钠中各元素的质量比为2∶1∶4 C、过氧碳酸钠是氧化物 D、过氧碳酸钠的相对分子质量是12215. 除去下列物质中的杂质,选用的方法或试剂正确的是( )
A、锶的原子序数为38 B、锶属于非金属元素 C、锶的相对原子质量是87.62g D、锶原子在化学反应中易得到电子14. 过氧碳酸钠(Na2CO4) 是一种新型氧系漂白剂。下列有关过氧碳酸钠的说法正确的是( )A、过氧碳酸钠由三个元素组成 B、过氧碳酸钠中各元素的质量比为2∶1∶4 C、过氧碳酸钠是氧化物 D、过氧碳酸钠的相对分子质量是12215. 除去下列物质中的杂质,选用的方法或试剂正确的是( )选项
物质
杂质
除去杂质所用的试剂和方法
A
氯化铁固体
氯化铜固体
铁粉 过滤
B
二氧化碳
氧气
点燃混合气体
C
铁
氧化铁
加盐酸 蒸发
D
碳酸钠粉末
碳酸钙粉末
加水 过滤、蒸发
A、A B、B C、C D、D16. 下列图象不能正确反映其描述的是( )A、 加热高锰酸钾固体
B、
加热高锰酸钾固体
B、 在密闭容器中点燃炭
C、
在密闭容器中点燃炭
C、 等质量的镁和氧气充分反应
D、
等质量的镁和氧气充分反应
D、 发生的反应为
发生的反应为
二、填空题
-
17. 如图是某包装袋上的部分文字说明。
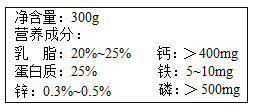 (1)、这里的钙、铁、磷、锌指的是(填“分子”、“原子”或“元素”)。(2)、这袋奶粉中蛋白质的质量为g。(3)、微量元素在人体内不能合成,但是对人体健康的影响很大,下列元素中属于微量元素的有。
(1)、这里的钙、铁、磷、锌指的是(填“分子”、“原子”或“元素”)。(2)、这袋奶粉中蛋白质的质量为g。(3)、微量元素在人体内不能合成,但是对人体健康的影响很大,下列元素中属于微量元素的有。A 钠 B 铁 C 锌 D 钙
(4)、该包装的外壳是铝合金制成,它属于材料。A 合成材料 B 金属材料 C 无机非金属材料 D 复合材料
18. 如图是某化肥包装袋上的部分说明: (1)、碳酸氢铵属化学肥料中的______ (填字母)A、钾肥 B、氮肥 C、磷肥 D、复合肥(2)、碳酸氢铵应具有的性质是______(填字母)A、易溶于水 B、有挥发性 C、受热易分解(3)、碳酸氢铵与熟石灰反应的方程式为NH4HCO3+Ca(OH)2═CaCO3+2X+NH3↑,则X的化学式是;施用该类肥料时,要避免与(填“酸”或“碱”)性物质混用,否则会减低肥效。19. 如图为生活中常见“暖贴”的部分标签。撕开暖贴包装即可自行发热,可以贴于身体某个部位用于取暖或热敷。根据所学回答下列问题。
(1)、碳酸氢铵属化学肥料中的______ (填字母)A、钾肥 B、氮肥 C、磷肥 D、复合肥(2)、碳酸氢铵应具有的性质是______(填字母)A、易溶于水 B、有挥发性 C、受热易分解(3)、碳酸氢铵与熟石灰反应的方程式为NH4HCO3+Ca(OH)2═CaCO3+2X+NH3↑,则X的化学式是;施用该类肥料时,要避免与(填“酸”或“碱”)性物质混用,否则会减低肥效。19. 如图为生活中常见“暖贴”的部分标签。撕开暖贴包装即可自行发热,可以贴于身体某个部位用于取暖或热敷。根据所学回答下列问题。 (1)、暖贴主要成分中属于氧化物的是(填名称)。(2)、暖贴中活性炭具有作用,以便于空气进入暖贴,使暖贴中的铁粉、水和发生反应放出热量,供人取暖。(3)、使用后的暖贴中常有红色物质出现,将该红色物质投入稀盐酸中,发生反应的化学方程式为。20. 甲、乙两种物质的溶解度曲线如图所示。请回答下列问题。
(1)、暖贴主要成分中属于氧化物的是(填名称)。(2)、暖贴中活性炭具有作用,以便于空气进入暖贴,使暖贴中的铁粉、水和发生反应放出热量,供人取暖。(3)、使用后的暖贴中常有红色物质出现,将该红色物质投入稀盐酸中,发生反应的化学方程式为。20. 甲、乙两种物质的溶解度曲线如图所示。请回答下列问题。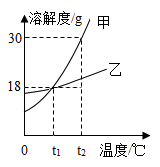 (1)、t2℃时,将100g水加入盛有40g甲物质的烧杯中,充分溶解后,得到甲的(填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,甲溶液的溶质质量分数(填“变大”“不变”或“变小”)。(2)、t2℃时,将甲和乙的饱和溶液降到t1℃,析出晶体的质量关系正确的是。(填字母)
(1)、t2℃时,将100g水加入盛有40g甲物质的烧杯中,充分溶解后,得到甲的(填“饱和”或“不饱和”)溶液。保持温度不变,往该烧杯中再加入10g水,充分搅拌后,甲溶液的溶质质量分数(填“变大”“不变”或“变小”)。(2)、t2℃时,将甲和乙的饱和溶液降到t1℃,析出晶体的质量关系正确的是。(填字母)A a>b B a=b C a<b D 不能确定
(3)、现有t1℃时甲的饱和溶液m1g和乙的饱和溶液m2g,下列关系一定成立的是(填字母)。A 两溶液中溶质的质量分数相等
B 分别升温至t2℃,所得溶液中溶质的质量分数相等(不考虑水的挥发)
C 保持t1℃不变,分别加入等质量的水,所得溶液中溶质的质量分数相等
三、流程题
-
21. 垃圾分类,全民行动,重庆也将逐步实行生活垃圾分类。(1)、废旧电池和过期药品都属于(填字母)。
A 、餐厨垃圾 B 、有害垃圾 C 、可回收垃圾 D、 其余垃圾
(2)、分类后的垃圾如何进一步利用或处理?如图所示为可回收垃圾的部分再利用途径。
①稀硫酸“溶解”步骤中共发生了三个化学反应,其中Fe与某物质发生化合反应生成FeSO4 , 写出该反应的化学方程式:。
② “溶解”过程中不会出现的现象是(填字母)。
A 固体逐渐减少 B 溶液颜色改变 C 有气泡生成 D 有红褐色沉淀生成
③若生锈铁制品中含有80kg的Fe2O3 , 56kg的Fe,假设所有铁元素都能转化成FeSO4·7H2O(相对分子质量为278),则得到FeSO4·7H2O的质量为kg。
④查阅资料得知,FeSO4容易被空气中的O2氧化。后续处理包括将所得到的FeSO4溶液在氮气环境中蒸发浓缩、降温结晶、过滤等,其中氮气的作用是。
22. 下图为初中常见的化学实验仪器和装置,请根据所学回答下列问题。 (1)、图1实验中铁丝网罩前作用是。(2)、写出图1用酒精灯加热的试管中发生反应的化学方程式:。(3)、若将上述装置用作实验室制取氧气的气体发生装置,所选的最佳药品为(填字母)。
(1)、图1实验中铁丝网罩前作用是。(2)、写出图1用酒精灯加热的试管中发生反应的化学方程式:。(3)、若将上述装置用作实验室制取氧气的气体发生装置,所选的最佳药品为(填字母)。A 过氧化氢溶液与二氧化锰 B 高锰酸钾
C 氯酸钾与二氧化锰 D 水
(4)、若按(3)中所选药品制取氧气,则该反应的化学方程式为。(5)、若要收集(3)中制取的氧气,需移除装有澄清石灰水的试管,同时还需添加图2中的仪器为(填序号),此时收集氧气的方法为法。23. 实验室常用的气体制取装置如下。请回答: (1)、写出编号仪器的名称:Ⅱ。(2)、实验室既可以制取CO2 , 又可以制取O2的发生、收集装置的组合为(填装置编号),并写用该发生装置制取O2的化学方程式。为得到一瓶较纯净的O2可以选用的收集装置是。(填装置编号)。(3)、某同学利用空塑料输液袋收集二氧化碳(如图),验满时,把燃着的木条放在玻璃管(填“a”或“b”)端,如果熄灭则满了。
(1)、写出编号仪器的名称:Ⅱ。(2)、实验室既可以制取CO2 , 又可以制取O2的发生、收集装置的组合为(填装置编号),并写用该发生装置制取O2的化学方程式。为得到一瓶较纯净的O2可以选用的收集装置是。(填装置编号)。(3)、某同学利用空塑料输液袋收集二氧化碳(如图),验满时,把燃着的木条放在玻璃管(填“a”或“b”)端,如果熄灭则满了。
四、计算题
-
24. 已知金属X可能是镁、铝、锌中的一种金属,它与稀盐酸反应的化学方程式为 。将3g该金属分5次投入100g稀盐酸中,其加入金属与产生氢气的关系如下表所示。根据所学回答下列问题。
次数
第一次
第二次
第三次
第四次
第五次
加入金属X的质量/g
0.6
0.6
0.6
0.6
0.6
生成氢气质量/g
0.05
0.05
0.05
0.03
0
(1)、通过计算可知,金属X的相对原子质量为 , 确定金属X为。(2)、求所用稀盐酸的溶质质量分数。(结果保留0.1%)。