四川省宜宾市2021年中考化学二模试卷
试卷更新日期:2021-06-11 类型:中考模拟
一、单选题
-
1. 空气中约占 体积的气体是( )A、氧气 B、氮气 C、水蒸气 D、二氧化碳2. 小红出现腹泻症状,医生建议她暂时不要吃富含蛋白质和油脂的食物。据此,小红应该选择的早餐是( )A、馒头和稀饭 B、鸡蛋和牛奶 C、油条和豆浆 D、炸鸡块和酸奶3. 下列物质属于氧化物的是( )A、高锰酸钾 B、氯酸钾 C、臭氧 D、过氧化氢4. 下列化学用语表示正确的是( )A、氯原子结构示意图:
 B、2个氢氧根:2OH2-
C、氧化镁的化学式:MgO2
D、60个氮原子:N60
5. 如图所示的实验操作中正确的是( )A、点燃酒精灯
B、2个氢氧根:2OH2-
C、氧化镁的化学式:MgO2
D、60个氮原子:N60
5. 如图所示的实验操作中正确的是( )A、点燃酒精灯 B、加热液体
B、加热液体  C、称量固体
C、称量固体  D、倾倒液体
D、倾倒液体  6. 水是重要资源,下列说法正确的是:( )A、过滤或加热均能使硬水转化为软水 B、利用活性炭的吸附性可使海水转化为淡水 C、电解水得到的氢气和氧气的质量比是2:1 D、水的蒸馏是物理变化7. 下列说法中,错误的是( )A、防止铁制品生锈,最常用的方法是在铁制品的表面涂一层保护膜 B、生铁是含碳量在2%~4.3%之间的铁合金 C、铁可以在氧气中燃烧,生成四氧化三铁 D、铁在自然界的分布很广,铁元素是地壳中含量最多的金属元素8. 下列盐的用途叙述错误的是( )A、碳酸氢钠用于烘焙糕点 B、碳酸钠用于造纸、纺织 C、碳酸钙用于配制农药波尔多液 D、氯化钠用于消除道路积雪9. “84”消毒液(主要成分是NaClO)是日常生活中常用的消毒液。下列有关说法正确的是( )A、“84”消毒液属于纯净物 B、NaClO中氯元素的化合价为-1 C、NaClO是一种钠盐 D、NaClO中Na、Cl、O的原子个数比为23∶35.5∶1610. 如图所示,20 ℃时,将盛有饱和硝酸钾溶液(底部有硝酸钾固体剩余)的小试管放入盛水的烧杯中,向烧杯中加入某物质后,试管中固体继续溶解。加入的物质是( )
6. 水是重要资源,下列说法正确的是:( )A、过滤或加热均能使硬水转化为软水 B、利用活性炭的吸附性可使海水转化为淡水 C、电解水得到的氢气和氧气的质量比是2:1 D、水的蒸馏是物理变化7. 下列说法中,错误的是( )A、防止铁制品生锈,最常用的方法是在铁制品的表面涂一层保护膜 B、生铁是含碳量在2%~4.3%之间的铁合金 C、铁可以在氧气中燃烧,生成四氧化三铁 D、铁在自然界的分布很广,铁元素是地壳中含量最多的金属元素8. 下列盐的用途叙述错误的是( )A、碳酸氢钠用于烘焙糕点 B、碳酸钠用于造纸、纺织 C、碳酸钙用于配制农药波尔多液 D、氯化钠用于消除道路积雪9. “84”消毒液(主要成分是NaClO)是日常生活中常用的消毒液。下列有关说法正确的是( )A、“84”消毒液属于纯净物 B、NaClO中氯元素的化合价为-1 C、NaClO是一种钠盐 D、NaClO中Na、Cl、O的原子个数比为23∶35.5∶1610. 如图所示,20 ℃时,将盛有饱和硝酸钾溶液(底部有硝酸钾固体剩余)的小试管放入盛水的烧杯中,向烧杯中加入某物质后,试管中固体继续溶解。加入的物质是( ) A、浓硫酸 B、氯化钠 C、硝酸铵 D、蔗糖11. 如图是某反应的微观示意图,其中不同的球代表不同的原子。下列说法正确的是( )
A、浓硫酸 B、氯化钠 C、硝酸铵 D、蔗糖11. 如图是某反应的微观示意图,其中不同的球代表不同的原子。下列说法正确的是( ) A、分子是化学变化中的最小粒子 B、生成物可能都是氧化物 C、参加反应的两物质的分子个数比为3∶2 D、图示可能表示反应:12. 下列除杂试剂和操作都正确的是(括号内的物质为杂质)( )
A、分子是化学变化中的最小粒子 B、生成物可能都是氧化物 C、参加反应的两物质的分子个数比为3∶2 D、图示可能表示反应:12. 下列除杂试剂和操作都正确的是(括号内的物质为杂质)( )选项
物质
除杂试剂(足量)
操作
A
CO2(CO)
NaOH溶液
将气体通过盛有足量NaOH溶液的洗气瓶
B
铜粉(铁粉)
稀盐酸
加入足量稀盐酸,过滤,洗涤,干燥
C
NaOH溶液(Na2CO3)
石灰水
加足量石灰水,过滤
D
Na2SO4溶液(NaCl)
BaCl2溶液
加入足量BaCl2溶液,过滤
A、A B、B C、C D、D13. 如图是元素周期表的一部分信息,下列说法错误的是( )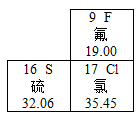 A、氟原子的核外电子数为9 B、硫元素的相对原子质量是32.06 C、氟、硫、氯三种元素都属于非金属元素 D、氟元素和氯元素位于元素周期表的同一周期14. 甲、乙两种物质的溶解度曲线如图。下列说法正确的是( )
A、氟原子的核外电子数为9 B、硫元素的相对原子质量是32.06 C、氟、硫、氯三种元素都属于非金属元素 D、氟元素和氯元素位于元素周期表的同一周期14. 甲、乙两种物质的溶解度曲线如图。下列说法正确的是( ) A、常温下,物质乙易溶于水 B、甲的溶解度大于乙的溶解度 C、t1℃时,两种溶液中溶质的质量分数一定相等 D、当乙中混有少量的甲时,可以采用降温结晶的方法提纯乙
A、常温下,物质乙易溶于水 B、甲的溶解度大于乙的溶解度 C、t1℃时,两种溶液中溶质的质量分数一定相等 D、当乙中混有少量的甲时,可以采用降温结晶的方法提纯乙二、填空题
-
15. 化学与生产、生活密切相关。回答下列问题:(1)、“自热火锅”“自热米饭”给人们生活带来方便。“自热火锅”主要由料包和发热包(主要成分为生石灰、焙烧硅藻土、活性炭、铁粉、铝粉、碳酸钠等)组成,使用方法如图所示。

①向发热包中加水后,会释放出大量的热。发热的原理之一是生石灰与水反应放热,此反应的化学方程式是 , 基本反应类型为。
②“自热火锅”的内、外盒由聚丙烯塑料制成。聚丙烯塑料属于(填字母序号)。
a金属材料 b有机合成材料 c复合材料
(2)、表为某自热米饭的营养成分表。营养物质
蛋白质
油脂
糖类
钠
钙
每份含量
29.6 g
23.5 g
104.7 g
814 mg
130 mg
①该自热米饭的营养物质中,能提供能量的有;从均衡膳食的角度考虑,该自热米饭中,除水外还缺少的营养素是。
②表中“钠”“钙”指的是(填“原子”或“元素”)。
(3)、能源问题是困扰人类可持续发展的一个重要因素,能源的开采、开发、储存和综合利用是目前世界各国科学家研究的重大课题。①人类目前使用的化石燃料有煤、和天然气。煤燃烧会产生大量的二氧化碳、二氧化硫和一氧化碳等气体,这些气体中会导致酸雨的是(填化学式)。
②天然气是常见的燃料,写出其燃烧的化学方程式:。
三、综合题
-
16. 阅读下面的科普短文。
在离地面约25 km高空处有一层厚度极薄的气体层,其主要成分是臭氧(O3)。它是地球上一切生命的保护层。与O2不同,通常状况下O3是淡蓝色气体,有难闻的鱼腥味。O3不太稳定,一旦受热极易转化成O2 , 并放出大量的热。O3比O2活泼得多,它能跟很多物质(如SO2、CO、NO、氟利昂等)发生反应。一种除去工业废气中的SO2的方法就是在微热条件下通入O3 , O3与SO2化合生成SO3 , SO3再与H2O化合生成H2SO4。
依据短文内容,回答下列问题:
(1)、写出O3的物理性质:。(2)、O3与O2化学性质不同的原因是;O3中氧元素的化合价是。(3)、除去工业废气中SO2时,O3与SO2反应的化学方程式为。17. 根据图所示的实验装置图,回答有关问题。 (1)、写出标号仪器的名称:a。(2)、实验室制取CO2的化学方程式为。若要获得干燥的CO2 , 除发生装置外,还应选用D装置,并在该装置中盛放(填试剂名称,下同)。如果用D装置检验CO2 , 其中应盛放。用E装置收集该气体,则气体从(填“b”或“c”)端进入。(3)、工业上以NH3为原料制备HNO3的过程如图1所示。某课外兴趣小组认真分析了图1的流程及反应原理,设计了利用NO2制备HNO3的实验装置(如图2所示)。试回答下列问题:
(1)、写出标号仪器的名称:a。(2)、实验室制取CO2的化学方程式为。若要获得干燥的CO2 , 除发生装置外,还应选用D装置,并在该装置中盛放(填试剂名称,下同)。如果用D装置检验CO2 , 其中应盛放。用E装置收集该气体,则气体从(填“b”或“c”)端进入。(3)、工业上以NH3为原料制备HNO3的过程如图1所示。某课外兴趣小组认真分析了图1的流程及反应原理,设计了利用NO2制备HNO3的实验装置(如图2所示)。试回答下列问题:

①完成工业上用NH3制取NO的化学方程式: ,。
②图2中通入的a气体是氧气,其目的是。
18. 某同学配制50g15%的氯化钠溶液,整个操作过程如图所示,回答下列问题: (1)、配制溶液的正确操作顺序为(填序号,后同),其中操作错误的是。(2)、该实验中所需食盐的质量是g。(3)、溶解过程中玻璃棒的作用是。(4)、对配置的溶液进行检测,发现溶质质量分数偏小,其原因可能是(选填字母)。
(1)、配制溶液的正确操作顺序为(填序号,后同),其中操作错误的是。(2)、该实验中所需食盐的质量是g。(3)、溶解过程中玻璃棒的作用是。(4)、对配置的溶液进行检测,发现溶质质量分数偏小,其原因可能是(选填字母)。A 氯化钠固体不纯 B 转移配置好的溶液时,有少量液体洒出
C 量取水的体积时,俯视读数 D 称量时,药品与砝码放反了
(5)、把50g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是g。19. 国家对化学实验室废弃药品的处理有严格要求,处理关键是确定其成分。某校化学实验室有一包固体废弃物,可能由铁粉、炭粉、碳酸钠、氧化铜、氯化钠、氢氧化钾中的一种或几种组成。为确定其成分,同学们取样进行了如图所示实验: (1)、操作Ⅰ的名称是。(2)、向固体A中加入足量稀盐酸,没有气泡冒出,充分反应后,固体未完全溶解,溶液由无色变成蓝色,说明原废弃物中一定有(填化学式,下同),一定没有。(3)、混合物D中有白色沉淀,取上层清液少许,滴加酚酞溶液,溶液变红。原废弃物中一定有的物质是。(4)、向混合物D中加入过量稀硝酸的现象是 , 加入稀硝酸后一定发生反应的化学方程式是(写一个)。(5)、混合物F中有白色沉淀,其上层清液中一定含有的溶质是。
(1)、操作Ⅰ的名称是。(2)、向固体A中加入足量稀盐酸,没有气泡冒出,充分反应后,固体未完全溶解,溶液由无色变成蓝色,说明原废弃物中一定有(填化学式,下同),一定没有。(3)、混合物D中有白色沉淀,取上层清液少许,滴加酚酞溶液,溶液变红。原废弃物中一定有的物质是。(4)、向混合物D中加入过量稀硝酸的现象是 , 加入稀硝酸后一定发生反应的化学方程式是(写一个)。(5)、混合物F中有白色沉淀,其上层清液中一定含有的溶质是。四、计算题
-
20. 某化学兴趣小组参观了一个石灰厂,带回了一些石灰石样品。同学们利用这些石灰石样品做了如下实验:取10 g样品放入烧杯中,将50 g稀盐酸分5次加入,实验过程所得的数据如下表所示(已知石灰石样品中的杂质不参与反应,也不溶于水)。
实验次数
1
2
3
4
5
加入稀盐酸的质量/g
10
10
10
10
10
剩余固体的质量/g
8
6
4
2
2
根据实验数据计算:
(1)、第次加入稀盐酸后,CaCO3恰好完全反应。(2)、石灰石样品中CaCO3的质量分数为。(3)、所用稀盐酸中溶质的质量分数。(写出计算过程)
-