初中化学人教版模拟试卷五
试卷更新日期:2021-06-09 类型:中考模拟
一、单选题
-
1. 实验仪器们展开了热烈的讨论,其中发生了化学变化的是( )A、玻璃棒:“我被摔成了两段。 ” B、蒸发皿:“看!食盐水冷却析出了晶体。 C、铁架台:“好难受啊! 我在潮湿的空气中生锈了。” D、酒精灯:“帽子哪里去了? 我的燃料跑掉了。”2. 下列场所挂的图标与“消防安全”不相符的是( )A、
 B、
B、 C、
C、 D、
D、 3. 下图为初中化学常见气体的发生与收集装置。有关这些装置的说法错误的是()
3. 下图为初中化学常见气体的发生与收集装置。有关这些装置的说法错误的是()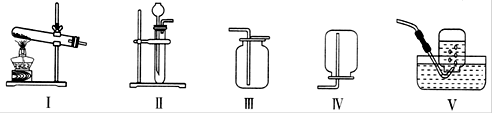 A、装置I可作为固体加热制取气体的发生装置 B、装置Ⅱ中长颈漏斗可以用分液漏斗、医用注射器代替 C、装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应的气体 D、装置Ⅴ可以用于收集H2、O2 , 也可以用于实验室收集CO24. 分类是学习和研充化学的常用方法。下列物质的分类正确的是( )A、混合物:碘酒、生铁、冰水 B、氧化物:CO2、MgO、水 C、有机物:甲烷、葡萄糖、碳酸钙 D、酸:H2SO4、HCl、H2O25. 利用物质在空气中燃烧,可以测定空气中氧气的含量。某化学兴趣小组想探究用不同物质在空气中燃烧测定氧气含量方法的优劣。他们用足量的蜡烛、红磷和白磷分别在相同体积与状态的空气中燃烧,用氧气探测器测定容器中剩余氧气与时间的关系如"题图”。下列说法正确的是( )
A、装置I可作为固体加热制取气体的发生装置 B、装置Ⅱ中长颈漏斗可以用分液漏斗、医用注射器代替 C、装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应的气体 D、装置Ⅴ可以用于收集H2、O2 , 也可以用于实验室收集CO24. 分类是学习和研充化学的常用方法。下列物质的分类正确的是( )A、混合物:碘酒、生铁、冰水 B、氧化物:CO2、MgO、水 C、有机物:甲烷、葡萄糖、碳酸钙 D、酸:H2SO4、HCl、H2O25. 利用物质在空气中燃烧,可以测定空气中氧气的含量。某化学兴趣小组想探究用不同物质在空气中燃烧测定氧气含量方法的优劣。他们用足量的蜡烛、红磷和白磷分别在相同体积与状态的空气中燃烧,用氧气探测器测定容器中剩余氧气与时间的关系如"题图”。下列说法正确的是( ) A、测定空气中氧气含量效果最好的是蜡烛,因为它反应速率快 B、该实验证明氧气的浓度较低时,红磷与白磷还能与之发生反应 C、三个实验中均为氧气过量 D、若用这三种物质做实验,测得空气中氧气含量偏高6. 镍铁双金属纳米颗粒催化剂可以提高电解水制氢的效率。铁、镍元素在元素周期表中的基本信息及它们的原子结构示意图如“题图"所示,下列说法错误的是( )
A、测定空气中氧气含量效果最好的是蜡烛,因为它反应速率快 B、该实验证明氧气的浓度较低时,红磷与白磷还能与之发生反应 C、三个实验中均为氧气过量 D、若用这三种物质做实验,测得空气中氧气含量偏高6. 镍铁双金属纳米颗粒催化剂可以提高电解水制氢的效率。铁、镍元素在元素周期表中的基本信息及它们的原子结构示意图如“题图"所示,下列说法错误的是( )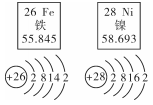 A、镍、铁都是金属元素 B、镍的核内质子数为28 C、铁的相对原子质量为55.845 D、镍、铁原子核外电子排布相同7. 下列事实与相应的解释不一致的是( )A、水通电分解——在化学变化中分 子可以再分 B、湿衣服晾在太阳底下干得快——温度升高 ,分子运动速率加快 C、6000 L氧气在加压的情况下可装人容积为40L钢瓶中——增大压强可使氧分 子变小 D、通常情况下,氧气支持燃烧,氮气不支持燃烧——不同种分子的化学性质不同8. 搞怪化学衫、创意元素钟表等也有化学用语,以下分析正确的是( )A、
A、镍、铁都是金属元素 B、镍的核内质子数为28 C、铁的相对原子质量为55.845 D、镍、铁原子核外电子排布相同7. 下列事实与相应的解释不一致的是( )A、水通电分解——在化学变化中分 子可以再分 B、湿衣服晾在太阳底下干得快——温度升高 ,分子运动速率加快 C、6000 L氧气在加压的情况下可装人容积为40L钢瓶中——增大压强可使氧分 子变小 D、通常情况下,氧气支持燃烧,氮气不支持燃烧——不同种分子的化学性质不同8. 搞怪化学衫、创意元素钟表等也有化学用语,以下分析正确的是( )A、 衬衫1的“2Fe"表示:两个铁离子
B、
衬衫1的“2Fe"表示:两个铁离子
B、 创意钟表里全是非金属元素
C、
创意钟表里全是非金属元素
C、 衬衫2表示的化学方程式:Mg+ZnSO4= MgSO4+Zn
D、
衬衫2表示的化学方程式:Mg+ZnSO4= MgSO4+Zn
D、 图4对应的微粒符号:Na+
9. DHA (C22H32O2)是一种不饱和脂肪酸,俗称“脑黄金”,具有增强记忆与思维能力、提高智力等作用、下列关于DHA的说法中正确的是( )A、它是一种有机高分子化合物 B、DHA中氢、氧元素的质量比为1 : 1 C、它是由碳、氢、氧三种元素的原子构成 D、每一个DHA分子中含有56个质子10. 甲酸(CH2O2)具有清洁制氢的巨大潜力,其反应微观示意图如下。说法正确的是( )
图4对应的微粒符号:Na+
9. DHA (C22H32O2)是一种不饱和脂肪酸,俗称“脑黄金”,具有增强记忆与思维能力、提高智力等作用、下列关于DHA的说法中正确的是( )A、它是一种有机高分子化合物 B、DHA中氢、氧元素的质量比为1 : 1 C、它是由碳、氢、氧三种元素的原子构成 D、每一个DHA分子中含有56个质子10. 甲酸(CH2O2)具有清洁制氢的巨大潜力,其反应微观示意图如下。说法正确的是( )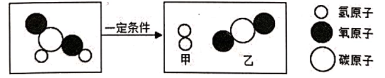 A、甲酸属于氧化物、有机物 B、甲酸由5个原子构成 C、甲酸中含有1个H分子 D、生成甲、乙的质量比为1:2211. 利用数据传感技术可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图所示。下列有关说法正确的是( )
A、甲酸属于氧化物、有机物 B、甲酸由5个原子构成 C、甲酸中含有1个H分子 D、生成甲、乙的质量比为1:2211. 利用数据传感技术可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶,使试管内的稀盐酸流入瓶中与碳酸钙发生反应,测得瓶内气压随时间的变化如图所示。下列有关说法正确的是( )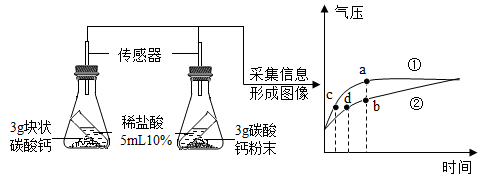 A、碳酸钙粉末产生的 质量多 B、块状碳酸钙产生的 质量多 C、对比分析a、b点可知,曲线①表示粉末状碳酸钙与稀盐酸反应 D、对比分析 C、d点可知,相同的气压时,块状碳酸钙需要时间短12. 氯化钾和氯酸钾两种物质的溶解度随温度变化曲线如"题图"所示。下列说法正确的是( )
A、碳酸钙粉末产生的 质量多 B、块状碳酸钙产生的 质量多 C、对比分析a、b点可知,曲线①表示粉末状碳酸钙与稀盐酸反应 D、对比分析 C、d点可知,相同的气压时,块状碳酸钙需要时间短12. 氯化钾和氯酸钾两种物质的溶解度随温度变化曲线如"题图"所示。下列说法正确的是( )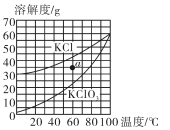 A、30℃时,KClO3饱和溶液的溶质质量分数为10% B、60℃时,a点对应KCl溶液恒温蒸发掉部分水可变饱和 C、40℃时,质量相同的KCl和KClO3饱和溶液中水的质量大小是:KCl> KClO3 D、将90℃的KClO3溶液降温,一定有KClO3晶体析出13. 身边一些物质的pH如图所示,下列说法正确的是( )
A、30℃时,KClO3饱和溶液的溶质质量分数为10% B、60℃时,a点对应KCl溶液恒温蒸发掉部分水可变饱和 C、40℃时,质量相同的KCl和KClO3饱和溶液中水的质量大小是:KCl> KClO3 D、将90℃的KClO3溶液降温,一定有KClO3晶体析出13. 身边一些物质的pH如图所示,下列说法正确的是( ) A、蚊虫叮咬后可涂牙膏减轻痛痒 B、厕所清洁剂不会腐蚀大理石地面 C、西瓜的酸性强于苹果汁 D、pH试纸浸入溶液中测其酸碱度14. 下列物质的鉴别和除杂方案正确的是( )
A、蚊虫叮咬后可涂牙膏减轻痛痒 B、厕所清洁剂不会腐蚀大理石地面 C、西瓜的酸性强于苹果汁 D、pH试纸浸入溶液中测其酸碱度14. 下列物质的鉴别和除杂方案正确的是( )选项
实验目的
实验方案
A
鉴别 CH4和 H2
点燃后分别在火焰上方罩一个冷而干燥的烧杯
B
鉴别羊毛和涤纶
分别取样,灼烧,闻气味
C
除去 KNO3溶液中的 KCl
加入过量 AgNO3溶液,过滤
D
除去铁粉中的少量铜粉
加入足量稀盐酸,充分反应后过滤、洗涤、干燥
A、A B、B C、C D、D15. 某小组用图表对所学知识进行归纳,其中甲包含乙和丙,不包含丁(如图所示)。下列表格中的各组物质或变化符合这种关系的是( )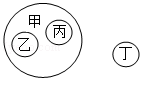
选项
甲
乙
丙
丁
A
化合物
盐酸
MnO2
铁粉
B
合成材料
合金
合成纤维
合成橡胶
C
化学变化
置换反应
化合反应
复分解反应
D
放热反应
硫在空气中燃烧
NaOH溶液与稀H2SO4反应
高温分解石灰石
A、A B、B C、C D、D二、填空题
-
16. 化学与我们的生活生产息息相关,生活处处有化学。(1)、Ⅰ.化学与生活:
野炊食谱如下:主食:馒头;配菜:红烧肉、豆腐汤、牛肉干。从营养角度来看,你认为食谱中还应添加下列食品中的(填序号)。
A 黄瓜 B 面条 C 炒鸡蛋 D 糖醋鱼
(2)、(填“聚乙烯”或“聚氯乙烯”)薄膜可用于食品的包装。(3)、在引燃细枯枝后,如果迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,说明可燃物充分燃烧需要的条件是。(4)、山药中含有碱性皂角素,皮肤沾上会奇痒难耐。你认为可涂用厨房中的来止痒。(5)、Ⅱ.化学与生产:工业上规模制氮主要有三类。①深冷空气制氮。利用空气各成分的沸点不同,使液态空气中的氧气和氮气分离,液态氧的沸点是-183℃,液态氮的沸点是-196℃,则分离出来某气体后,剩下的主要是。
②变压吸附制氮。利用碳分子筛对氮气进行吸附,可见碳分子筛与一样具有疏松多孔的结构,可用于水的净化。
③膜分离制氮。利用中空纤维膜分离空气制取氮气。中空纤维膜还常用于自来水、地下水除菌除浊净化,使水中的微粒、细菌等不能通过滤膜而被去除。
(6)、Ⅲ.化学与新技术:12C、13C、14C分别表示碳元素的三种原子,可简写成12C、13C、14C。请据图回答:
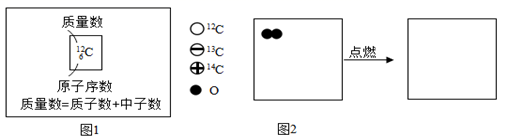
①12C、13C、14C三种原子中,数目不等(填“质子”或“中子”或“电子”)。
②12C与O2反应生成的一氧化碳可表示为12CO。写出13CO在O2中燃烧的化学方程式 , 在图2所示的小方框中,把13CO与O2反应的反应物和生成物微观粒子补画齐全。(画在答题卡上)
17. “比较归纳法”是学习化学的一种重要方法.(“﹣”表示相连的两种物质能发生反应,“﹣”表示某种物质可通过一步反应转化为另一种物质.)(1)请以表2中序号Ⅰ为示例,填写序号Ⅱ、Ⅲ中的空格:
项目
序号
举例
物质类别间的相互反应
物质类别间的相互转化
Ⅰ
CaCl2+Na2CO3=CaCO3↓+2NaCl
盐1﹣盐2
盐→新盐
Ⅱ
写出硫酸与氯化钡反应的化学方程式
酸﹣盐
酸→
Ⅲ
写出氢氧化钠转变成另一种碱的
碱﹣
碱→新碱
(2)室温下,氯化镁与下列物质的变化关系,正确的是 (填标号).
A.MgCl2﹣AgNO3
B.KNO3﹣MgCl2
C.MgCl2﹣HCl
D.Mg(OH)2﹣MgCl2 .
三、实验探究题
-
18. 化学是一门以实验为基础的学科。题 18-1 图是六种可以制得氧气的途径,如图为实验室制气常用的装置。
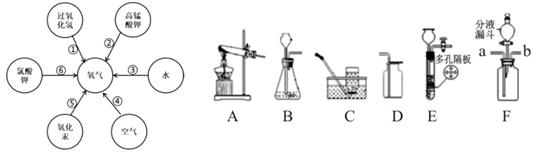 (1)、“绿色化学”倡导节约资源和节能环保等理念,根据“绿色化学”理念,在图中选择实验室制取氧气的最佳途径是.(填序号),该反应的化学方程式为.。
(1)、“绿色化学”倡导节约资源和节能环保等理念,根据“绿色化学”理念,在图中选择实验室制取氧气的最佳途径是.(填序号),该反应的化学方程式为.。途径⑥需要添加 Mn2 作催化剂,若反应结束后回收 MnO2 固体,需进行的操作是溶解、.、洗涤、烘干。
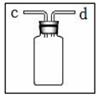
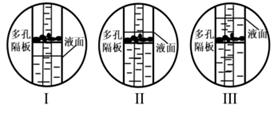
(2)、若选择题图中的途径②制备并收集较为纯净的氧气,应图中选择的发生和收集装置分别为;图中装置用于排空气法收集氧气,c 为进气口,请将瓶内导管补画完整。(3)、图是使用图 装置制取二氧化碳时液面变化的情景。当液面变化按→→顺序时(填序号),导管上的活塞是在被.状态(填“打开”或“关闭”)。(4)、若用图中 F 装置验证二氧化碳使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的以下实验操作顺序是(填序号,可重复选用)。①从 b 端通氮气;②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中;③从 a 端通二氧
化碳;④从分液漏斗中滴加适量水。
 19. 实验室使用块状石灰石和稀盐酸制CO2 , 当观察不到有气泡产生,固体仍有剩余时,某兴建小组对此进行了以下探究:(1)、取上层清液,用测得溶液pH=2说明溶液显性。(2)、为探究“剩余液pH=2的原因”,该小组同学开展了如下活动:
19. 实验室使用块状石灰石和稀盐酸制CO2 , 当观察不到有气泡产生,固体仍有剩余时,某兴建小组对此进行了以下探究:(1)、取上层清液,用测得溶液pH=2说明溶液显性。(2)、为探究“剩余液pH=2的原因”,该小组同学开展了如下活动:[提出假设]
假设1:生成CO2造成的。
假设2:生成CaCl2造成的。
假设3:剩余稀盐酸造成的。
[设计实验]
实验编号
实验操作
实验现象
①
取氯化钙溶于水,测定溶液的pH
测得pH=7
②
将CO2通入蒸馏水中至饱和,测定溶渡的pH
测得pH>5
[设计实验]
剩余液pH=2的原因是。
(3)、试管中剩余固体中是否仍含有CaCO3?小组同学向试管中继续加入稀盐酸,又有大量气泡产生。①由此得出的结论是:写出反应的化学方程式:。
②比较稀盐酸加入前后的实验现象,解释 “又有大量气泡产生”的原因:。
(4)、[拓展延伸]假如用100 g 14. 6%的稀盐酸和足量的石灰石反应,观察不到气泡产生时,停止收集气体,收集到的CO2质量(填“> ”“<”或“=”)8.8g。
(5)、实验室用块状石灰石和适量稀盐酸反应至气泡逸出不明显后,测得其残留液pH等于2.此时取适量反应后溶液,逐滴滴入碳酸钠溶液。并用pH数字探测仪连续监测,得曲线如图所示(pH为纵坐标,时间为横坐标)。BC段的化学方程式是。
四、综合题
-
20. “题1图”是工业上利用黄铁矿(主要成分FeS2)制取硫的流程。“题2图"为硫元素的价类图,“→"表示物质之间可以转化,A 、B 、C、D、E、F ,C是常见的化学物质。请回答:
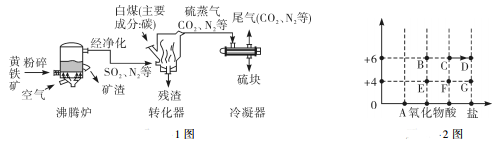
已知:沸腾炉中的主要反应为4FeS2+11O2 2Fe2O3+8SO2。
(1)、投入沸腾炉前将黄铁矿粉碎的目的是。(2)、在加热条件下,转化器中发生反应的化学方程式是 , 请在“题2图"用“→"表示这一转化过程。(3)、冷凝器中发生的变化是(填"物理变化”或“化学变化”)。(4)、以上流程中产生的矿渣和尾气均可再利用,其可能的用途是 (答一条即可)。(5)、图2中已知E+H2O=F,则F是 (写化学式);B的名称是 , D 可用于制造波尔多液,写出C转化为D的化学方程式: 。五、计算题
-
21. 现有H2SO4与CuSO4的混合溶液,为了分析混合溶液中H2SO4与CuSO4的质量分数,设计了如图1实验方案;
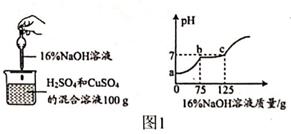 (1)、根据图1坐标,推测CuSO4溶液呈(填“酸”“碱”“中”)性;c点溶液中的溶质为(写化学式)。(2)、请计算该混合溶液中的CuSO4的溶质质量分数。(3)、若在100g混合溶掖中不断加入上述氢氧化钠溶液,请你在图2中画出加人氢氧化钠溶液的质量与产生沉淀的质量的关系图。
(1)、根据图1坐标,推测CuSO4溶液呈(填“酸”“碱”“中”)性;c点溶液中的溶质为(写化学式)。(2)、请计算该混合溶液中的CuSO4的溶质质量分数。(3)、若在100g混合溶掖中不断加入上述氢氧化钠溶液,请你在图2中画出加人氢氧化钠溶液的质量与产生沉淀的质量的关系图。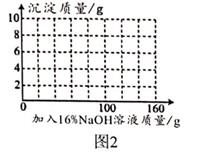 (4)、根据该方案的实验现象就能证明硫酸和氢氧化钠发生了中和反应的原因是 。
(4)、根据该方案的实验现象就能证明硫酸和氢氧化钠发生了中和反应的原因是 。
-