上海市普陀区2021年高考化学二模试卷
试卷更新日期:2021-05-24 类型:高考模拟
一、单选题
-
1. 原子是一种很小的微粒。钠原子半径为 ,则a等于( )A、9 B、10 C、11 D、122. 关于电解质的说法错误的是( )A、能电离的物质是电解质 B、强电解质在水溶液中完全电离 C、能导电的物质不一定是电解质 D、水是一种极弱的电解质3. 下列晶体中,任何一个原子都被相邻四个原子包围,以共价健形成正四面体,并向空间伸展成网状结构的是( )A、金刚石 B、石墨 C、足球烯 D、水晶4. 火箭燃料肼( )的一种制备原理: 。下列表述错误的是( )A、 的结构式:
 B、 的电子式:
C、 的球棍模型:
B、 的电子式:
C、 的球棍模型:  D、 燃烧的化学方程式:
5. 关于有机物甲和乙的叙述正确的是( )
D、 燃烧的化学方程式:
5. 关于有机物甲和乙的叙述正确的是( ) A、甲与乙互为同分异构体 B、甲分子中所有碳原子均共面 C、乙的一氯取代物共有3种 D、甲与乙均能使溴的四氯化碳溶液褪色6. 下列物质间的每次转化都能通过一步反应实现的是( )A、 B、 C、 D、7. 下列过程中,共价键被破坏的是( )A、干冰升华 B、氯气被活性炭吸附 C、酒精溶于水 D、碘化氢气体溶于水8. 接触法制硫酸工业中,无需用到的设备是( )A、沸腾炉 B、接触室 C、过滤器 D、吸收塔9. 将摩擦带电的玻璃棒接近液流,实验现象如图。该实验能说明( )
A、甲与乙互为同分异构体 B、甲分子中所有碳原子均共面 C、乙的一氯取代物共有3种 D、甲与乙均能使溴的四氯化碳溶液褪色6. 下列物质间的每次转化都能通过一步反应实现的是( )A、 B、 C、 D、7. 下列过程中,共价键被破坏的是( )A、干冰升华 B、氯气被活性炭吸附 C、酒精溶于水 D、碘化氢气体溶于水8. 接触法制硫酸工业中,无需用到的设备是( )A、沸腾炉 B、接触室 C、过滤器 D、吸收塔9. 将摩擦带电的玻璃棒接近液流,实验现象如图。该实验能说明( ) A、 分子带电, 分子不带电 B、 是由非极性键形成的极性分子 C、 是正四面体形分子 D、 分子中正负电荷的重心是重合的10. 实验室按如下过程测量海带中碘的含量,不需要使用的实验装置是( )
A、 分子带电, 分子不带电 B、 是由非极性键形成的极性分子 C、 是正四面体形分子 D、 分子中正负电荷的重心是重合的10. 实验室按如下过程测量海带中碘的含量,不需要使用的实验装置是( ) A、
A、 B、
B、 C、
C、 D、
D、 11. 在反应前后固体质量不变的化学反应是( )A、 通过灼热的 粉末 B、 通过 粉末 C、 与 发生铝热反应 D、将铁钉投入 溶液12. 有关卤素性质的判断符合题意,且可用元素周期律解释的是( )A、相对原子质量: B、稳定性: C、密度: D、酸性:13. 将体积为 的某一元强酸溶液与体积为 的某一元碱溶液混合,恰好完全反应。则以上两溶液中一定相等的是( )A、溶质物质的量 B、溶液质量 C、 和 的物质的量 D、物质的量浓度14. 少量小苏打溶液与足量石灰水反应的离子方程式正确的是( )A、 B、 C、 D、15. 已知共价键的键能与热化学方程式信息如下表:
11. 在反应前后固体质量不变的化学反应是( )A、 通过灼热的 粉末 B、 通过 粉末 C、 与 发生铝热反应 D、将铁钉投入 溶液12. 有关卤素性质的判断符合题意,且可用元素周期律解释的是( )A、相对原子质量: B、稳定性: C、密度: D、酸性:13. 将体积为 的某一元强酸溶液与体积为 的某一元碱溶液混合,恰好完全反应。则以上两溶液中一定相等的是( )A、溶质物质的量 B、溶液质量 C、 和 的物质的量 D、物质的量浓度14. 少量小苏打溶液与足量石灰水反应的离子方程式正确的是( )A、 B、 C、 D、15. 已知共价键的键能与热化学方程式信息如下表:共价键
键能/( )
436
463
热化学方程式
则 的Q为( )
A、428 B、-428 C、498 D、-49816. 向CuSO4溶液中加入H2O2溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。下列关于上述过程的说法错误的是( )A、Cu2+将H2O2还原为O2 B、H2O2既表现氧化性又表现还原性 C、Cu2+是H2O2分解反应的催化剂 D、发生了反应Cu2O+H2O2+4H+═2Cu2++3H2O17. 在潮湿的深层土壤中,钢管主要发生厌氧腐蚀,厌氧细菌可促使土壤中的 与H2反应生成S2- , 加速钢管的腐蚀,其反应原理如下图所示。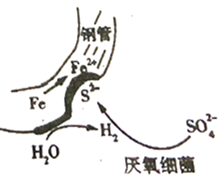
下列说法正确的是( )
A、正极的电极反应式为:2H2O+O2+4e-=4OH- B、钢管腐蚀的直接产物中含有FeS、Fe(OH)2 C、在钢管表面镀锌或镀铜均可减缓钢管的腐蚀 D、 与H2的反应可表示为:4H2+ -8e- S2-+4H2O18. 恒温密闭容器中加入一定量的A,发生反应 ( ),达到平衡。以下分析正确的是( )A、加入少量B,平衡就会逆向移动 B、达到平衡的标志之一: C、若开始时向容器中加入1 A,达到平衡时吸收热量Q D、缩小容器体积,重新达到平衡时, 的浓度与原平衡浓度相等19. 室温下,向 0.01 mol·L-1 的醋酸溶液中滴入 pH=7 的醋酸铵溶液,溶液 pH 随滴入醋酸铵溶液体积变化的曲线示意图如图所示。下列分析正确的是( ) A、a点,pH = 2 B、b点,c(CH3COO-) > c(NH4+) C、c点,pH可能大于7 D、ac段,pH的增大仅是因为醋酸电离平衡逆向移动20. 已知某100 溶液中含有的部分离子的浓度大小如图所示,该溶液呈无色、透明、均一状态,可能还含有 、 、 、 。为了进一步确认,加入足量 溶液,生成23.3g白色沉淀,再加稀盐酸,沉淀不消失。对原溶液说法错误的是( )
A、a点,pH = 2 B、b点,c(CH3COO-) > c(NH4+) C、c点,pH可能大于7 D、ac段,pH的增大仅是因为醋酸电离平衡逆向移动20. 已知某100 溶液中含有的部分离子的浓度大小如图所示,该溶液呈无色、透明、均一状态,可能还含有 、 、 、 。为了进一步确认,加入足量 溶液,生成23.3g白色沉淀,再加稀盐酸,沉淀不消失。对原溶液说法错误的是( ) A、肯定不存在 、 B、 的物质的量浓度为2 C、加入含0.2 的溶液时,沉淀质量达到最大量 D、加入少量 溶液,反应的离子方程式为
A、肯定不存在 、 B、 的物质的量浓度为2 C、加入含0.2 的溶液时,沉淀质量达到最大量 D、加入少量 溶液,反应的离子方程式为二、填空题
-
21. 工业烟气可用氯酸氧化法脱硫,涉及反应:_______ _______ _______ =_______ (未配平)。完成下列填空:(1)、写出N原子核外电子排布的轨道表示式。(2)、用含字母a、b的代数式配平上述化学方程式 , 标出电子转移的方向和数目。该化学方程式配平系数不唯一,请说明理由。(3)、氯酸是一元强酸,可由氯酸钡溶液和稀硫酸反应得到。写出该反应的化学方程式。(4)、工业烟气中的 也可用 和 的混合液脱除。
① 脱除 的离子方程式为;
② 溶液呈碱性的原因是。
三、综合题
-
22. 丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。正丁烷脱氢制丁烯的热化学方程式为: ( )。完成下列填空:(1)、T1℃时,5mol 在100L容器内脱氢,30min达到平衡转化了30%。则30min内的平均反应速率 。为提高反应的平衡转化率,可采取的一条措施是。(2)、T2℃时,该反应平衡常数K=1.2,则T1T2 (选填“>”“<”或“=”)。(3)、如图为反应平衡时丁烯产率和反应温度的关系曲线。丁烯的产率在590℃之前随温度升高而增大的原因可能是;590℃之后,丁烯的产率快速降低的主要原因可能是。
 (4)、已知:
(4)、已知:则 。
(5)、写出2-丁烯在一定条件下发生聚合反应的化学方程式。23. 碳酸镧[ , ]可用于治疗肾病患者的高磷酸盐血症。其制备反应的原理为: 。利用下列装置在实验室中模拟制备 。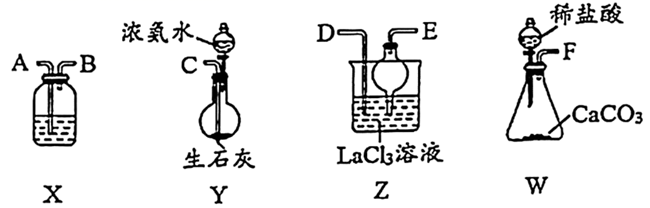
完成下列填空:
(1)、Y中盛放浓氨水的仪器名称为。(2)、制备 实验流程中装置接口的连接顺序为F→→→;C→。(3)、Y中发生反应的化学方程式为。(4)、X中盛放的试剂是。(5)、Z中应先通 ,后通入过量的 ,原因是。(6)、 质量分数的测定(杂质不与盐酸反应):准确称取10.000g产品试样,溶于足量稀盐酸中,将生成的 全部通入过量的 溶液中,得到沉淀8.865g。 的质量分数为。24. 一种合成解热镇痛类药物布洛芬方法如下:

完成下列填空:
(1)、A与C互称为 , B→C的反应类型是。(2)、D的结构简式是。(3)、E→F的化学方程式为。(4)、写出检验F中溴原子的实验方法。(5)、布洛芬分子中的含氧官能团的结构简式为 , 写出一种满足以下条件的布洛芬的同分异构体。①含有苯环;②能发生银镜反应和水解反应;③分子中有4种不同化学环境下的氢原子。
(6)、设计一条以丙醇为主要原料合成 的合成路线。
-