山东省淄博市张店区2021年中考化学一模试卷
试卷更新日期:2021-05-24 类型:中考模拟
一、单选题
-
1. 下列自然资源的变化利用过程中,发生了化学变化的是( )A、海水蒸发 B、粮食酿酒 C、风力发电 D、空气液化2. 溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是( )A、碘酒 B、蒸馏水 C、医用酒精 D、生理盐水3. 下列关于O2和CO2的说法正确的是( )A、都含有氧元素 B、都不易溶于水 C、都含有氧气分子 D、都能使带有火星的木条复燃4. 下列有关操作错误的是( )A、读
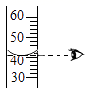 B、闻
B、闻  C、拿
C、拿 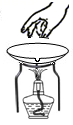 D、滴
D、滴 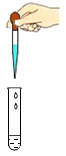 5. 下列有关燃烧和灭火的说法正确的是( )A、物质跟氧气的反应就是燃烧 B、可燃性气体中混有空气,遇明火一定发生爆炸 C、通过降低可燃物的着火点可以灭火 D、煤加工成粉末状,可使煤燃烧更充分6. 稀土是不可再生的重要战略资源,铈(Ce)是一种常见的稀土元素,铈元素在元素周期表中的信息如图所示。下列叙述错误的是( )
5. 下列有关燃烧和灭火的说法正确的是( )A、物质跟氧气的反应就是燃烧 B、可燃性气体中混有空气,遇明火一定发生爆炸 C、通过降低可燃物的着火点可以灭火 D、煤加工成粉末状,可使煤燃烧更充分6. 稀土是不可再生的重要战略资源,铈(Ce)是一种常见的稀土元素,铈元素在元素周期表中的信息如图所示。下列叙述错误的是( )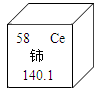 A、铈属于金属元素 B、铈原子中的质子数为58 C、铈的相对原子质量是140.1g D、铈原子中的核外电子数是587. 在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是( )A、CO2 B、CaO C、Cu(NO3)2 D、HCl8. 我国化学家研究出一种新型催化剂,在太阳光照射下实现了水的高效分解。该反应过程的微观示意图如下,下列说法错误的是( )
A、铈属于金属元素 B、铈原子中的质子数为58 C、铈的相对原子质量是140.1g D、铈原子中的核外电子数是587. 在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是( )A、CO2 B、CaO C、Cu(NO3)2 D、HCl8. 我国化学家研究出一种新型催化剂,在太阳光照射下实现了水的高效分解。该反应过程的微观示意图如下,下列说法错误的是( )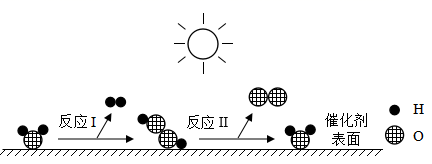 A、
A、 表示的物质属于氧化物
B、反应I 的化学方程式为
C、反应II 中,反应前后原子的种类和数目均不变
D、该成果对氢能源的推广应用有重要的实践意义
9. 宏观辨识与微观探析是化学学科的核心素养之一。下列对宏观事实的微观解释错误的是( )
表示的物质属于氧化物
B、反应I 的化学方程式为
C、反应II 中,反应前后原子的种类和数目均不变
D、该成果对氢能源的推广应用有重要的实践意义
9. 宏观辨识与微观探析是化学学科的核心素养之一。下列对宏观事实的微观解释错误的是( )选项
宏观事实
微观解释
A
液态水受热变为水蒸气时体积增大
温度升高,分子体积变大
B
氧气经压缩可以储存在钢瓶中
压强增大,分子间的间隔变小
C
一氧化碳和二氧化碳化学性质不同
构成二者的分子不同
D
氢氧化钠溶液和氢氧化钙溶液具有相似的化学性质
两种溶液中都含有OH-
A、A B、B C、C D、D10. 豆腐中含有多种人体所需的氨基酸,其中含量最多的是亮氨酸(化学式C6H13NO2),下列说法正确的是( )A、从类别上看:亮氨酸属于氧化物 B、从组成上看:亮氢酸由碳、氢、氮、氧四种元素组成,其中氢元素的质量分数最小 C、从变化上看:亮氨酸完全分解只生成二氧化碳和水 D、从构成上看:亮氨酸由6个碳原子、13个氢原子,1个氮原子,2个氧原子构成11. 每年6月5日是“世界环境日”。造成酸雨的主要物质是( )A、二氧化氮和一氧化碳 B、二氧化硫和一氧化碳 C、二氧化碳和一氧化碳 D、二氧化硫和二氧化氮12. 下列离子能在含有硫酸的溶液中大量共存的是( )A、Mg2+、 B、Na+、 C、K+、OH- D、Ba2+、Cl-13. 实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A、①② B、①③ C、②④ D、③④14. 下列实验方案设计不能达到实验目的是( )A、利用盛有浓硫酸的洗气瓶,可除去CO2气体中混有的少量水蒸气 B、用水电解实验说明水由氢、氧元素组成 C、用灯帽熄灭酒精灯,以说明物质燃烧需要达到着火点 D、用紫色石蕊试液,就可区分盐酸、氢氧化钠溶液和食盐水三种无色溶液15. 时,将a、b两种固体物质(均不含结晶水)各25g,分别加入盛有100g水的烧杯中,充分搅拌后现象如图甲所示;升温到 时,忽略水分蒸发,现象如图乙所示。图丙是a、b两种固体物质在水中的溶解度曲线。下列说法错误的是( )
甲 乙 丙
A、图甲中两烧杯内a、b溶液的溶质质量分数相等 B、图乙中烧杯内b溶液的溶质质量分数为20% C、图丙中曲线M表示a物质的溶解度曲线 D、若a中混有少量b,可将其溶液蒸发结晶、趁热过滤提纯a二、填空题
-
16. 化学用语是学习化学的基本工具。请用合适的化学用语填空。(1)、氖的元素符号。(2)、保持双氧水(过氧化氢)化学性质的最小微粒。(3)、2个氯原子。(4)、由氧和铝两种元素组成的化合物的化学式。17. 宏观和微观相结合是认识物质结构与性质的重要方法。(1)、氧原子的结构示意图为
 ,硫原子的结构示意图为
,硫原子的结构示意图为  。
。 ①原子的核电荷数与核外电子总数的关系是。
②一个硫原子得到二个电子,形成一种新粒子,该粒子的符号为。
(2)、Na2CO3溶液和H2SO4溶液反应的示意图如图所示。该反应中实际参加反应的离子是。 (3)、硫及其化合物的“化合价-物质类别”关系图如图所示。物质X的化学式为 , 由SO3转化为物质Y的化学方程式为。
(3)、硫及其化合物的“化合价-物质类别”关系图如图所示。物质X的化学式为 , 由SO3转化为物质Y的化学方程式为。 18. 科学使用化学物质,可以保障人体健康。(1)、某同学的部分体液的pH如图所示。
18. 科学使用化学物质,可以保障人体健康。(1)、某同学的部分体液的pH如图所示。
①图中碱性最强的体液是。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平(主要成分为Al(OH)3)治疗,其原理是(用化学方程式表示)。
(2)、某84消毒液产品的部分说明如表。84消毒液
(产品特点)主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.1%~6.9%
(餐具消毒)用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。
(注意事项)①外用消毒剂,须稀释后使用。
③不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。
①NaClO中氯元素的化合价是。
②依据表中信息,将有效氯的质量分数为60%的84消毒液10g,配制有效氯的质量分数为0.04%的消毒浸泡液,需要水的质量为。
③洁厕灵(主要成分为盐酸〕与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整: 2HCl+NaClO= +Cl2↑+H2O。
19. 实验室对含有MgCl2的粗盐进行提纯,步骤如图:

⑴步骤①中,用托盘天平称量5.0g粗盐。
⑵步骤②中,玻璃棒的作用是。
⑶步骤③中,滴加过量NaOH溶液除去MgCl2 , 如何判断滴加过量的NaOH溶液。
⑷步骤⑤中,为中和过量的NaOH,应滴加的“试剂a”是(填字母)。
A稀盐酸 B稀硫酸 C稀硝酸 D氯化钠溶液
⑸步骤⑥的操作名称是 , 当时,停止加热。
三、综合题
-
20. 如图为AG(初中常见的物质)的转化关系,其中A是天然气的主要成分,D为单质。

根据以上信息回答下列问题。
(1)、写出反应①化学方程式 , 其常见用途为(写一条).(2)、反应②的现象为。(3)、写出反应③的化学方程式。该反应属于(填基本反应类型)。21. 利用下列实验来探究CO2气体的制取和性质。(1)、A、B、C三套发生装置都可用于实验室制取CO2气体。
①仪器a的名称是。
②实验室制取CO2的化学方程式是;收集CO2可选用的装置是(填序号),检验CO2收集满的方法是。
④利用B装置制取CO2时,反应未停止前关闭止水夹,可观察到的现象是。
④与A装置相比,利用C装置制取CO2的优点是。
(2)、用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是。
A甲中逸出的气体只含CO2
B乙中液体变红,证明CO2能与水反应
C加热后红色不褪去,说明碳酸受热不分解
D欲达到实验目的,可将盐酸改为稀硫酸
22. 化学兴趣小组对某种粗锌(主要成分为锌,杂质不与酸反应)样品中锌的含量进行了测定。如图所示,称20g该粗锌样品置于烧杯(质量为58.8g)中,加入100g足量稀硫酸,待粗锌完全反应后,称得烧杯及烧杯中剩余物总质量为178.4g。 (1)、硫酸(H2SO4)的相对分子质量为。(2)、反应过程中产生氢气的质量为g。(3)、计算该粗锌样品中锌的质量分数(写出计算过程及结果)。23. 学习了MnO2对过氧化氢有催化作用的知识后。某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究。(1)、(猜想)Ⅰ. CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
(1)、硫酸(H2SO4)的相对分子质量为。(2)、反应过程中产生氢气的质量为g。(3)、计算该粗锌样品中锌的质量分数(写出计算过程及结果)。23. 学习了MnO2对过氧化氢有催化作用的知识后。某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究。(1)、(猜想)Ⅰ. CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;Ⅱ. CuO参与反应产生O2 , 反应前后质量和化学性质发生了改变;
Ⅲ. CuO是反应的催化剂,反应前后。
(2)、(实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
填写下表:
步骤③现象
步骤⑥结果
步骤⑦现象
结论
带火星的木条复燃
溶液中有气泡放出
猜想Ⅰ、Ⅱ不成立
猜想Ⅲ成立
(3)、步骤①的目的。(4)、步骤④需用到的实验仪器有:铁甲台(带铁圈)、漏斗、烧杯、。(5)、过氧化氢能被CuO催化分解放出O2的化学方程式为。(拓展)要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是(写一种)。
24. 已知Cu2O是一种红色固体物质,在酸性溶液中可发生反应生成Cu2+和Cu。请用已学过的知识设计一个最简便的实验方案,来检验CuO经氢气还原所得到的红色产物中是否有Cu2O。
实验步骤
实验现象与结论
化学方程式
25. 某品牌干燥剂含有氧化钙、氢氧化钠和氯化钙中的两种物质,为探究其组成,某化学兴趣小组取一定质量的干燥剂样品做了如下实验。(查阅资料)稀硝酸(HNO3)具有酸的通性
(设计实验)流程如图:

(实验分析)
(1)、干燥剂样品溶于水后得到的溶液一定显(填“酸性”或“碱性”或“中性”)。白色沉淀a的化学式是。(2)、生成气体b的反应的化学方程式是。(3)、(结论与反思)①若c处无现象,则该品牌干燥剂的成分为(写化学式)。
②若c处有白色沉淀生成,且沉淀质量为2.87g;白色沉淀a的质量为1.2g。则干燥剂的成分为(写化学式)。写出c处产生白色沉淀的化学方程式。
③该实验过程中,过量稀硝酸不能用过量的稀盐酸代替的原因是。