山东省东营市2021年中考化学二模试卷
试卷更新日期:2021-05-24 类型:中考模拟
一、单选题
-
1. 物质世界充满了变化。下列变化中,只发生了物理变化的是( )A、光合作用
 B、湿法炼铜
B、湿法炼铜  C、压榨果汁
C、压榨果汁  D、火箭发射
D、火箭发射  2. 石油化工厂排放污染物时必贴的图标是( )A、
2. 石油化工厂排放污染物时必贴的图标是( )A、 B、
B、 C、
C、 D、
D、 3. 正确的实验操作对实验结果、人身安全都非常重要。下列实验操作正确的是( )A、
3. 正确的实验操作对实验结果、人身安全都非常重要。下列实验操作正确的是( )A、 熄灭酒精灯
B、
熄灭酒精灯
B、 过滤
C、
过滤
C、 稀释浓硫酸
D、
稀释浓硫酸
D、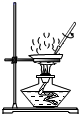 蒸发
4. 安罗替尼是一种小分子多靶点酪氨酸激酶抑制剂,化学式为C23H22FN3O3 , 能有效抑制VEGFR、PDGFR、FGFR、c-Kit等激酶,具有抗肿瘤血管生成和抑制肿瘤生长的作用。在2015年世界肺癌大会(WCLC)、2015年欧洲肺癌大会(ELCC)、2016年中国临床肿瘤学大会(CSCO)、2016及2017年美国临床肿瘤学会年会(ASCO)、2017年世界肺癌大会(WCLC)都进行了相关临床试验结果的报道,其作为中国新药引起了广泛关注。有关安罗替尼的叙述正确的是( )A、安罗替尼中含有23个碳原子、22个氢原子、1个氟原子、3个氮原子、3个氧原子 B、安罗替尼由碳、氢、氮、氧元素的质量比是23:22:3:3 C、安罗替尼中氟元素的含量最少 D、安罗替尼是氧化物5. “见著知微”是化学学科的重要特点,它是通过宏观现象的观察,思考,推理,建立起对微观粒子的认识。下列叙述正确的是( )A、电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的 B、洗衣服一会儿能晾干,说明分子是不断地运动 C、置换反应不一定有元素化合价发生改变 D、能使酚酞试液变红的一定是碱的溶液6. 被称之为“软电池”的纸质电池,采用薄层纸片作为传导体,电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH),避免了传统电池所带来的污染问题,因而废旧的纸质电池可作为一般的废弃物加以处理.下列说法错误的是( )
蒸发
4. 安罗替尼是一种小分子多靶点酪氨酸激酶抑制剂,化学式为C23H22FN3O3 , 能有效抑制VEGFR、PDGFR、FGFR、c-Kit等激酶,具有抗肿瘤血管生成和抑制肿瘤生长的作用。在2015年世界肺癌大会(WCLC)、2015年欧洲肺癌大会(ELCC)、2016年中国临床肿瘤学大会(CSCO)、2016及2017年美国临床肿瘤学会年会(ASCO)、2017年世界肺癌大会(WCLC)都进行了相关临床试验结果的报道,其作为中国新药引起了广泛关注。有关安罗替尼的叙述正确的是( )A、安罗替尼中含有23个碳原子、22个氢原子、1个氟原子、3个氮原子、3个氧原子 B、安罗替尼由碳、氢、氮、氧元素的质量比是23:22:3:3 C、安罗替尼中氟元素的含量最少 D、安罗替尼是氧化物5. “见著知微”是化学学科的重要特点,它是通过宏观现象的观察,思考,推理,建立起对微观粒子的认识。下列叙述正确的是( )A、电解水生成氢气和氧气,说明水是由氢分子和氧分子构成的 B、洗衣服一会儿能晾干,说明分子是不断地运动 C、置换反应不一定有元素化合价发生改变 D、能使酚酞试液变红的一定是碱的溶液6. 被称之为“软电池”的纸质电池,采用薄层纸片作为传导体,电池总反应为:Zn+2MnO2+H2O=ZnO+2MnO(OH),避免了传统电池所带来的污染问题,因而废旧的纸质电池可作为一般的废弃物加以处理.下列说法错误的是( ) A、该电池反应中锌元素化合价升高 B、该电池反应中二氧化锰作催化剂 C、工作原理是将化学能转化为电能 D、开发利用该电池可以减少对环境的污染7. 下列对主题知识的归纳,完全正确的是( )
A、该电池反应中锌元素化合价升高 B、该电池反应中二氧化锰作催化剂 C、工作原理是将化学能转化为电能 D、开发利用该电池可以减少对环境的污染7. 下列对主题知识的归纳,完全正确的是( )选项
应用
A.化学与健康
①食用乳制品、豆制品可补充钙元素
②长期饮用蒸馏水有利于健康
B.化学与环境
①为治理雾霾,禁止使用化石燃料
②为节约和环保,分类回收生活垃圾
C.化学与生活
①霉变的大米多次淘洗后仍不能食用
②用灼烧闻气味的方法鉴别羊毛线与纯棉线
D.化学与农业
①用铁桶配制农药波尔多液
②科学合理地使用化肥能促进粮食增产
A、A B、B C、C D、D8. 某同学梳理归纳了以下知识点①用水灭火的原理是降低了可燃物的着火点;②烧碱和熟石灰都属于碱;③稀释浓硫酸时,先在烧杯内倒入水,再沿烧杯壁缓慢注入浓硫酸,并不断搅拌;④酸碱盐中不一定含有非金属元素;⑤洗涤剂能去除油污是因为洗涤剂可以溶解油污;⑥日常生活中的塑料、合成纤维和合成橡胶都属于合成材料,其中错误的组合是( )A、①⑤⑥ B、①④⑤ C、③⑤⑥ D、③④⑥9.暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源与铁粉的氧化.小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计).下列说法错误的是( )
 A、实验前必须检查装置的气密性 B、通过本次实验数据测得空气中氧气的体积分数为18% C、若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足 D、必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积10. 现有以下曲线,与之对应的叙述错误的是( )A、
A、实验前必须检查装置的气密性 B、通过本次实验数据测得空气中氧气的体积分数为18% C、若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足 D、必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积10. 现有以下曲线,与之对应的叙述错误的是( )A、 用等质量氯酸钾制取氧气
B、
用等质量氯酸钾制取氧气
B、 向稀盐酸中滴加过量的氢氧化钠溶液
C、
向稀盐酸中滴加过量的氢氧化钠溶液
C、 向等质量、等质量分数的两份稀盐酸中分别加入足量的ZnO和Zn(OH)2
D、
向等质量、等质量分数的两份稀盐酸中分别加入足量的ZnO和Zn(OH)2
D、 某温度时,向一定量的饱和石灰水中加入少量的生石灰
11. “NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl”是氨碱法制纯碱的重要反应,下列叙述错误的是( )A、在加压的条件下向饱和氨盐水中通二氧化碳,能加速NaHCO3的生成 B、该条件下NaHCO3的溶解度比NH4Cl的小,因此先析出 C、析出晶体后的溶液为NaHCO3的饱和溶液 D、析出晶体后剩余溶液中只有一种溶质12. 为得到纯净的物质,某同学设计了下表中的除杂方法,其中方法正确的是( )
某温度时,向一定量的饱和石灰水中加入少量的生石灰
11. “NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl”是氨碱法制纯碱的重要反应,下列叙述错误的是( )A、在加压的条件下向饱和氨盐水中通二氧化碳,能加速NaHCO3的生成 B、该条件下NaHCO3的溶解度比NH4Cl的小,因此先析出 C、析出晶体后的溶液为NaHCO3的饱和溶液 D、析出晶体后剩余溶液中只有一种溶质12. 为得到纯净的物质,某同学设计了下表中的除杂方法,其中方法正确的是( )物质
所含杂质
除去杂质的方法
A
NaCl
Na2CO3
加入稀硫酸至不再产生气泡
B
Cu
CuO粉末
加入过量稀盐酸,充分反应,过滤
C
CO
CO2
将气体缓缓通过NaOH溶液
D
KNO3
CuCl2
加入过量氢氧化钾溶液,过滤
A、A B、B C、C D、D二、填空题
-
13. 化学与生产生活密切相关,请用所学知识回答下列问题:(1)、汽车尾气中含有许多有害气体,使用催化转换器可减少有害气体的排放,其中某一反应过程的微观变化如图所示。请你写出该反应的化学方程式;
 (2)、汽车玻璃的主要成分之一是硅酸钠(Na2SiO3),在硅酸钠中硅元素的化合价为价。(3)、车身钢筋容易锈蚀,请写出一种防止铁生锈的方法:。(4)、车上空调的阵阵凉气使小明联想到氟利昂,氟利昂曾经是一种很好的制冷剂,自1987年国际规定禁止使用,因为氟利昂分解出氟原子能引发下列循环反应而破坏臭氧(O3)层:①Cl+O3=ClO+O2;②ClO+O=Cl+O2。在上述循环反应中氯原子起作用,O3和O2的化学性质不同的原因是。14. 厨房中的化学(1)、用新鲜水果榨制成的果汁中,含有人体所需的营养成分,主要有水、无机盐、糖类和。生活中常用鉴别软水、硬水。(2)、要做“翡翠”饺子,可将菠菜榨汁,通过操作将菜渣与菜汁分离,用菜汁和面。(3)、山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的来止痒。(4)、战国《周礼》中记载:“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳,主要成分是碳酸钙)。将“灰”溶于水可得沤浸树皮脱胶的碱液。“灰”溶于水时发生的反应用化学方程式表示为:。15. 硝酸钾、氯化钾的溶解度曲线如图1所示。
(2)、汽车玻璃的主要成分之一是硅酸钠(Na2SiO3),在硅酸钠中硅元素的化合价为价。(3)、车身钢筋容易锈蚀,请写出一种防止铁生锈的方法:。(4)、车上空调的阵阵凉气使小明联想到氟利昂,氟利昂曾经是一种很好的制冷剂,自1987年国际规定禁止使用,因为氟利昂分解出氟原子能引发下列循环反应而破坏臭氧(O3)层:①Cl+O3=ClO+O2;②ClO+O=Cl+O2。在上述循环反应中氯原子起作用,O3和O2的化学性质不同的原因是。14. 厨房中的化学(1)、用新鲜水果榨制成的果汁中,含有人体所需的营养成分,主要有水、无机盐、糖类和。生活中常用鉴别软水、硬水。(2)、要做“翡翠”饺子,可将菠菜榨汁,通过操作将菜渣与菜汁分离,用菜汁和面。(3)、山药中含有碱性皂角素,皮肤沾上会奇痒难忍。你认为可涂厨房中的来止痒。(4)、战国《周礼》中记载:“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳,主要成分是碳酸钙)。将“灰”溶于水可得沤浸树皮脱胶的碱液。“灰”溶于水时发生的反应用化学方程式表示为:。15. 硝酸钾、氯化钾的溶解度曲线如图1所示。 (1)、P点的含义是。(2)、当氯化钾中混有少量硝酸钾时,可用方法提纯氯化钾。(3)、t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是 , 其溶液的溶质质量分数为(结果精确到0.1%)。(4)、图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为。(5)、下列有关说法错误的是___________。A、①与②的溶质质量可能相等 B、②与③的溶质质量分数一定相等 C、等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾 D、等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾16. 元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
(1)、P点的含义是。(2)、当氯化钾中混有少量硝酸钾时,可用方法提纯氯化钾。(3)、t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是 , 其溶液的溶质质量分数为(结果精确到0.1%)。(4)、图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为。(5)、下列有关说法错误的是___________。A、①与②的溶质质量可能相等 B、②与③的溶质质量分数一定相等 C、等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾 D、等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾16. 元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:族
周期
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
2
3Li
锂
6.941
4Be
铍
9.012
5B
硼
10.81
6C
碳
12.01
7N
氮
14.01
8O
氧
16.00
9F
氟
19.00
10Ne
氖
20.18
3
11Na
钠
22.99
12Mg
镁
24.31
13Al
铝
26.98
14Si
硅
28.09
15P
磷
30.97
16S
硫
32.06
17Cl
氯
35.45
18Ar
氩
39.95
(1)、请从上表中查出关于氖元素的一条信息:。(2)、请用化学元素周期表坐标描述第15号元素所处位置 , 其离子符号是。(3)、第12号元素与第17号元素组成的化合物是(填化学式),构成该物质的微粒是(选填“分子”、“原子”或“离子”)。(4)、第9号氟元素和氢元素形成的化合物的水溶液氢氟酸(HF),可用于玻璃雕刻,其主要原理是氢氟酸与玻璃的主要成分二氧化硅(SiO2)发生反应,生成四氟化硅气体(SiF4)和水,该反应的化学方程式为。(5)、根据下列四种粒子的结构示意图回答。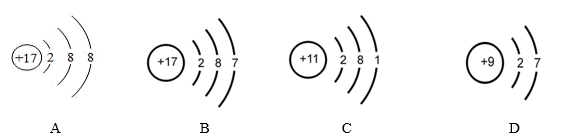
它们属于同种元素的是。
(6)、第13号元素铝在化学反应中易(填“得到”或“失去”)电子。则铝元素和硫元素形成的化合物的化学式为。17. 某实验中学的同学归纳总结了有关酸和碱的化学性质的知识网络如图所示。其中A是一种生活中最常见的金属,B是一种常见的化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请根据图示回答有关问题。 (1)、B可能是(填化学式);(2)、请写出有关反应的化学方程式:反应⑨;(3)、请你用文字描述反应⑤的实验现象;(4)、图中所标的9个反应中,属于置换反应的是。18. 氧气是一种非常重要的化学物质,请回忆初中化学知识,根据所学知识填写下列内容。
(1)、B可能是(填化学式);(2)、请写出有关反应的化学方程式:反应⑨;(3)、请你用文字描述反应⑤的实验现象;(4)、图中所标的9个反应中,属于置换反应的是。18. 氧气是一种非常重要的化学物质,请回忆初中化学知识,根据所学知识填写下列内容。 (1)、(一)氧气的测定:实验室常用图1装置测定空气中氧气的含量。某化学兴趣小组在实验室测定空气中氧气的含量,由注射器和硬质玻璃管组成的密闭系统,其中注射器中存有15mL空气,玻璃管的容积是40mL。
(1)、(一)氧气的测定:实验室常用图1装置测定空气中氧气的含量。某化学兴趣小组在实验室测定空气中氧气的含量,由注射器和硬质玻璃管组成的密闭系统,其中注射器中存有15mL空气,玻璃管的容积是40mL。为了保证氧气全部反应,加入的铜粉应该。气球的作用是:。
(2)、实验中你所看到的硬质玻璃管内的现象是。发生反应的化学方程式为。(3)、瑞典化学家舍勒曾用图2装置对空气中的氧气含量进行测定:将磷放在密闭钟罩内的水面上方燃烧(如图2所示),产生现象,成分为 , 一段时间后观察到钟罩内水面大约上升。(4)、(二)制取氧气

仪器a的名称是。
(5)、选择过氧化氢溶液制取氧气,反应的方程式是。若选择C装置作为发生装置,优点是 , 若需制取一瓶氧气做铁丝燃烧的实验,收集装置最好选择。(6)、混制“富氧空气”用纯氮气及上述实验制取的氧气,混制一瓶(集气瓶容积为250mL)氧气体积分数为40%的“富氧空气”,可使用H装置,先在上图H装置中装满水,再从导管(填“b”或“c”)通入氮气,排出mL水,后再通入氧气排出80mL水。19. 为了测定某碳酸钠样品中杂质氯化钠的质量分数,小东同学进行了三次实验,其实验数据如下表:编号
第1次
第2次
第3次
所取固体样品的质量/g
7
5
5
加入氯化钙溶液的质量/g
50
50
75
反应后生成沉淀的质量/g
4
4
4
(1)、根据表格数据,第次实验样品中碳酸钠与氯化钙恰好完全反应;(2)、计算碳酸钠样品中杂质氯化钠的质量分数是多少?(3)、加入氯化钙溶液的溶质质量分数是多少?