江苏省无锡市惠山区2021年中考化学模拟试卷
试卷更新日期:2021-05-21 类型:中考模拟
一、单选题
-
1. 下列不会造成空气污染的是( )A、燃放烟花 B、光合作用 C、焚烧垃圾 D、汽车尾气2. 贫血缺少的微量元素是( )A、Ca B、I C、Fe D、F3. 下列物质的用途主要利用其化学性质的是( )A、氧气用于医疗急救 B、干冰用于人工降雨 C、铜、铝用于制作导线 D、活性炭用于吸附冰箱异味4. 下列属于纯净物的是( )A、食用醋 B、盐水 C、生铁 D、液氧5. 下列化学用语正确的是( )A、正二价铁元素—Fe+2 B、铜元素—Cu C、2个氯原子—Cl2 D、氧化铝—AlO6. 下列有关水银体温计的说法正确的是( )A、体温计中的汞属于非金属单质 B、体温计中的汞在常温下为固体 C、体温计的原理是温度改变时汞原子间的间隔发生改变 D、当温度升高时汞原子不断运动,温度不变时汞原子静止7. 下列化学肥料中属于复合肥料的是( )A、K2SO4 B、CO(NH2)2 C、NH4NO3 D、NH4H2PO48. 某同学将打磨过的铝丝放入硫酸铜溶液中,意外发现铝丝表面有气泡产生,下列说法错误的是( )
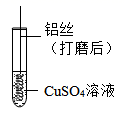 A、点燃气体发出爆鸣声,说明气体是氢气 B、铝丝表面还有银白色固体析出 C、铝在该反应中失去电子 D、向硫酸铜溶液中滴入紫色石蕊试液,石蕊变红,说明硫酸铜溶液呈酸性9. 钛和钛合金被认为是21世纪的重要金属材料。如图是钛元素在元素周期表中信息,下列有关说法错误的是( )
A、点燃气体发出爆鸣声,说明气体是氢气 B、铝丝表面还有银白色固体析出 C、铝在该反应中失去电子 D、向硫酸铜溶液中滴入紫色石蕊试液,石蕊变红,说明硫酸铜溶液呈酸性9. 钛和钛合金被认为是21世纪的重要金属材料。如图是钛元素在元素周期表中信息,下列有关说法错误的是( ) A、钛是金属元素 B、钛原子的核内有22个质子 C、钛的相对原子质量为47.87g D、钛原子核外有22个电子10. 下列物质的转化在给定条件下不能实现的是( )A、 B、 C、 D、11. 下列实验进行中的现象或实验原理正确的是( )
A、钛是金属元素 B、钛原子的核内有22个质子 C、钛的相对原子质量为47.87g D、钛原子核外有22个电子10. 下列物质的转化在给定条件下不能实现的是( )A、 B、 C、 D、11. 下列实验进行中的现象或实验原理正确的是( )
A、 白磷始终不燃烧
B、
白磷始终不燃烧
B、 小气球变瘪
C、
小气球变瘪
C、 U型管内液面左高右低
D、
U型管内液面左高右低
D、 验证Fe、Cu、Ag的金属活动性强弱
12. 如图是甲转化为丙的微观过程,下列说法错误的( )
验证Fe、Cu、Ag的金属活动性强弱
12. 如图是甲转化为丙的微观过程,下列说法错误的( ) A、丙中氢、氮、氧元素的质量比为1:1:3 B、甲和乙均为氧化物 C、该反应中甲、乙的分子个数比为3:1 D、转化中原子的种类和数目不变13. 甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( )
A、丙中氢、氮、氧元素的质量比为1:1:3 B、甲和乙均为氧化物 C、该反应中甲、乙的分子个数比为3:1 D、转化中原子的种类和数目不变13. 甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( ) A、甲物质的溶解度为20g B、t1℃时,30g甲加入到50g水中最多可得70g溶液 C、t2℃时,乙物质的饱和溶液升温变成不饱和溶液 D、t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲<乙14. 某同学利用数据传感技术测定溶液中电导率来辅助探究中和反应,如下图。已知:电导率与溶液中离子浓度(单位体积离子数)成正比。下列说法错误的是( )
A、甲物质的溶解度为20g B、t1℃时,30g甲加入到50g水中最多可得70g溶液 C、t2℃时,乙物质的饱和溶液升温变成不饱和溶液 D、t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲<乙14. 某同学利用数据传感技术测定溶液中电导率来辅助探究中和反应,如下图。已知:电导率与溶液中离子浓度(单位体积离子数)成正比。下列说法错误的是( ) A、A~C过程中电导率降低是由于离子数减少 B、D点时,溶液中离子数大于B点 C、C点时,NaOH溶液与稀盐酸恰好完成反应 D、该实验能证明溶液中始终有带电的离子15. 向一定量的硝酸铜、硝酸亚铁的混合溶液中加入 2.4g 镁粉,充分反应后过滤、洗涤、 干燥,称得固体 6g。则下列分析正确的是( )A、滤液中一定不含有硝酸铜 B、滤液中一定含有硝酸亚铁 C、滤出的固体中可能有铜无铁 D、滤出的固体中可能只有铜和镁
A、A~C过程中电导率降低是由于离子数减少 B、D点时,溶液中离子数大于B点 C、C点时,NaOH溶液与稀盐酸恰好完成反应 D、该实验能证明溶液中始终有带电的离子15. 向一定量的硝酸铜、硝酸亚铁的混合溶液中加入 2.4g 镁粉,充分反应后过滤、洗涤、 干燥,称得固体 6g。则下列分析正确的是( )A、滤液中一定不含有硝酸铜 B、滤液中一定含有硝酸亚铁 C、滤出的固体中可能有铜无铁 D、滤出的固体中可能只有铜和镁二、填空题
-
16. 化学与生活、生产有密切的联系(1)、调节酸性土壤常用。
a 熟石灰 b 氢氧化钠 c 氯化钠
(2)、保鲜膜是聚乙烯塑料,它属于材料。a 金属材料 b 合成材料 c 复合材料
(3)、除去热水瓶内胆上水垢。a 白醋 b 食盐水 c 纯碱溶液
(4)、灼烧法鉴别羊毛和棉花,闻到气味是羊毛。a 烧纸 b 刺激性 c 烧焦羽毛
17. 无锡有夏至吃馄饨的习俗。周日奶奶给玲玲包馄饨,在这一过程中玲玲发现了许多与化学知识有关的问题。(1)、皮:馄饨皮在制作过程中,需要加入食用碱(碳酸钠和碳酸氢钠的混合物),使馄饨皮更美味。碳酸氢钠俗称。(2)、馅:包馄饨的馅料中主要有:牛肉、芹菜、青椒,食盐、植物油等,其中,青椒、芹菜等蔬菜富含的营养素是。(3)、煮:煮馄饨的炊具是不锈钢锅,不锈钢做炊具是因为它具有良好的性。煮馄饨用水是硬水还是软水,可以用检验。
煮馄饨用燃料是天然气,天然气的主要成分(写化学式)。
(4)、洗:吃完后,玲玲用洗涤剂把餐具洗干净,是利用了洗涤剂的功能。三、实验题
-
18. 请结合如图回答问题:
 (1)、写出有标号仪器的名称:①。(2)、用氯酸钾和二氧化锰共热制O2的化学方程式为。
(1)、写出有标号仪器的名称:①。(2)、用氯酸钾和二氧化锰共热制O2的化学方程式为。可选用的装置组合为;若改用高锰酸钾制氧气,需对装置做出的改动为。
(3)、实验室可用装置B或C制CO2的化学方程式为 , C装置的优点是 , 用F装置收集CO2 , 气体应从(选填“a”或“b”)端通入。四、科学探究题
-
19. 已知:钠在常温下与水剧烈反应生成氢气和氢氧化钠。小明结合已有知识设计如图装置进行验证,他的操作如下:

①打开止水夹1及分液漏斗活塞,待液体充满大试管后,关闭止水夹1及分液漏斗活塞.观察到液体分层,钠熔成银白色小球,产生大量气泡,下层溶液变成红色,并逐渐被压入B中;
②打开止水夹2,待B中部分溶液进入C中,迅速关闭止水夹2,A中反应的化学方程式为;
③打开止水夹3,稀盐酸进入C中,并观察到(填实验现象),说明二氧化碳能与氢氧化钠溶液反应且进入的稀盐酸过量;
④将燃着的木条伸到导管尖嘴处,打开止水夹1,气体燃烧,产生色火焰。
20. “废物利用”既节约资源又保护环境。某研究小组利用废铁屑(含少量硫化物)来制备硫酸亚铁铵[(NH4)2Fe(SO4)2·xH2O]以及确定x值进行如下的实验探究。查阅资料:
Ⅰ:硫酸亚铁铵,俗称摩尔盐,是一种重要的化工原料。易溶于水,不溶于酒精,在100-110℃时分解,110℃完全失去结晶水。温度升高,(NH4)2Fe(SO4)2会继续分解。
Ⅱ:硫酸亚铁,容易被氧气缓慢氧化,铁粉能防止溶液中的硫酸亚铁被氧化,能与硫酸铵反应生成硫酸亚铁铵。
Ⅲ:铁屑中硫化物与稀硫酸反应会产生酸性硫化氢(H2S)气体,要净化处理。
(1)、一、制备硫酸亚铁铵晶体小组同学设计了如下图1流程制备硫酸亚铁铵晶体:

根据流程回答下列问题:
步骤①中用热碱性溶液浸泡废铁屑目的是除去铁屑上面的油污,可以选择的浸泡液是。
A 碳酸钠溶液 B 氯化钠溶液 C 稀盐酸
(2)、写出步骤②中铁与硫酸溶液反应的化学方程式;实验中采用微热的目的是。(3)、步骤④的实验操作是。(4)、步骤②③实验装置图如下图2:
根据装置图回答下列问题:
B装置中产生大量氢气作用:一是可以将装置及溶液中氧气排走,防止硫酸亚铁被氧化,该操作是;二是通过关闭活塞b、c,打开a,将反应后B中溶液压入A中。
(5)、C瓶中氢氧化钠溶液的作用是通过中和反应吸收硫化氢,防止污染空气。写出该反应的化学方程式。(6)、二、测定(NH4)2Fe(SO4)2·xH2O中x的值小组同学设计了图3实验装置来测定x值:

实验步骤:
①连接好装置,检查装置气密性,在A中放入一定质量的硫酸亚铁铵
②打开弹簧夹,通入一段时间的N2后,称量B装置质量
③关闭弹簧夹,将恒温加热器控制在110℃进行加热至晶体完全失水: (NH4)2Fe(SO4)2·xH2O=(NH4)2Fe(SO4)2+ xH2O
④打开弹簧夹,继续缓缓通入一段时间的N2 , 再次称量B装置质量,两次称量质量差为10.8g
⑤称量A中反应后固体质量为28.4g
……
根据实验装置图和实验步骤回答下列问题
将加热温度控制在110℃的目的是。
(7)、计算x值(写出计算过程)__。(8)、以下说法正确的是。A 步骤2中先称量,再通入一段时间的N2 , 会导致x值偏大
B 步骤3中如果加热时间不够,会导致x值偏小
C 步骤4中缓缓通入一段时间的N2 , 目的是将装置中残留的水蒸气被B装置充分的吸收
D C装置作用是吸收空气中二氧化碳,防止进入B中
五、流程题
-
21. 方铅矿的主要成分是PbS,以方铅矿为原料制备铅酸蓄电池的电极材料PbO2的工艺流程如下图所示:
 (1)、PbO2中铅元素的化合价为。(2)、步骤①方铅矿焙烧后排放的气体主要成分是(填化学式)。(3)、步骤②中体现了焦炭具有性质(填化学性质)。(4)、写出步骤⑤的化学方程式;过滤后要用蒸馏水洗涤PbO2 , 设计实验证明已洗涤干净的方法(填操作和现象)。
(1)、PbO2中铅元素的化合价为。(2)、步骤①方铅矿焙烧后排放的气体主要成分是(填化学式)。(3)、步骤②中体现了焦炭具有性质(填化学性质)。(4)、写出步骤⑤的化学方程式;过滤后要用蒸馏水洗涤PbO2 , 设计实验证明已洗涤干净的方法(填操作和现象)。
-