江苏省南京市秦淮区2021年中考化学一模试卷
试卷更新日期:2021-05-21 类型:中考模拟
一、单选题
-
1. 下列过程中,只发生物理变化的是( )A、动植物的呼吸 B、酒和醋的酿造 C、石蜡的熔化 D、金属的腐蚀2. 下列元素在人体中属于常量元素的是( )A、镁 B、铁 C、硒 D、碘3. 下列仪器中,用作配制溶液和较大量试剂的反应容器,在常温或加热时使用的是( )A、试管 B、烧杯 C、量筒 D、集气瓶4. 下列化肥中,属于钾肥的是( )A、尿素 B、氨水 C、硫酸钾 D、过磷酸钙5. 下列有关物质用途的说法中,错误的是( )A、干冰用于人工降雨 B、锡用于制灯泡里的灯丝 C、制糖工业中利用活性炭来脱色制白糖 D、农业上可以用氯化钠溶液来选种6. 下列说法错误的是( )A、墙内开花墙外香,说明分子在不断运动 B、分子是由原子构成的,说明分子比原子大 C、气体可压缩储存于钢瓶中,说明分子之间存在间隔 D、氧化汞受热分解,说明分子在化学变化中可以再分7. 下列气体与空气混合后遇明火,可能发生爆炸的是( )
A、甲烷 B、氮气 C、氧气 D、二氧化碳8. 相比于传统石墨负极材料电池,硅氧负极材料让电池能量密度与充电速度都得到了显著的提升。硅元素的某些信息如图,下列说法错误的是( ) A、硅属于金属元素 B、硅的原子序数是14 C、硅是地壳中含量居于第二位的元素 D、硅的相对原子质量是28.099. 实验室制取气体的常见装置如图,下列说法正确的是( )
A、硅属于金属元素 B、硅的原子序数是14 C、硅是地壳中含量居于第二位的元素 D、硅的相对原子质量是28.099. 实验室制取气体的常见装置如图,下列说法正确的是( ) A、装置①中的棉花是为了防止冷凝水回流到热的试管底部,炸裂试管 B、装置②中的仪器包括分液漏斗、锥形瓶、双孔橡胶塞和玻璃导管 C、装置④和⑤均可用于收集氧气 D、装置⑥用于收集氢气时,应从导管a处通入氢气10. 探究燃烧条件的实验装置如图,下列说法错误的是( )
A、装置①中的棉花是为了防止冷凝水回流到热的试管底部,炸裂试管 B、装置②中的仪器包括分液漏斗、锥形瓶、双孔橡胶塞和玻璃导管 C、装置④和⑤均可用于收集氧气 D、装置⑥用于收集氢气时,应从导管a处通入氢气10. 探究燃烧条件的实验装置如图,下列说法错误的是( ) A、加热一段时间,煤粉先燃烧起来 B、本实验使用铜片是利用其导热性 C、用完酒精灯后用灯帽盖灭,灭火原理是隔绝空气 D、本实验能够证明可燃物燃烧需要温度达到着火点11. 图示为合成醋酸的某反应的微观示意图,下列说法正确的是( )
A、加热一段时间,煤粉先燃烧起来 B、本实验使用铜片是利用其导热性 C、用完酒精灯后用灯帽盖灭,灭火原理是隔绝空气 D、本实验能够证明可燃物燃烧需要温度达到着火点11. 图示为合成醋酸的某反应的微观示意图,下列说法正确的是( ) A、反应物和生成物均为有机化合物 B、两种反应物中碳元素的化合价相同 C、醋酸由碳、氢、氧三种原子构成 D、醋酸中碳元素的质量分数为40%12. 用图示装置进行实验,滴入甲,浸有丙的棉花不变红的是( )
A、反应物和生成物均为有机化合物 B、两种反应物中碳元素的化合价相同 C、醋酸由碳、氢、氧三种原子构成 D、醋酸中碳元素的质量分数为40%12. 用图示装置进行实验,滴入甲,浸有丙的棉花不变红的是( )
选项
甲
乙
丙
A
烧碱溶液
氯化铵
酚酞溶液
B
石灰水
纯碱
酚酞溶液
C
稀硫酸
小苏打
石蕊溶液
D
浓盐酸
锌粒
石蕊溶液
A、A B、B C、C D、D13. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是( )A、N2气体(O2)一通过灼热的氧化铜 B、NaCl溶液(MgCl2)一加入适量的硫酸钠溶液,过滤 C、CaO固体(CaCO3)一高温充分煅烧 D、Fe粉(Fe2O3)一加入足量的稀盐酸,过滤14. 向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,充分反应后过滤,得到固体甲和溶液乙,下列说法错误的是( )A、固体甲中一定含有银,溶液乙中一定含有硝酸锌 B、若溶液乙中呈现无色,则溶液乙中只含有一种溶质 C、向溶液乙中再加锌粉,若有红色固体析出,则固体甲的组成有两种可能 D、向溶液乙中滴加稀盐酸,若有白色沉淀生成,则溶液乙中含有两种溶质15. 高温下,置于密闭容器中的碳和氧气充分反应,碳和氧气的质量比如图,下列关于反应后密闭容器中的剩余物的说法中,错误的是( ) A、甲点对应的剩余物是二氧化碳和氧气 B、乙点对应的剩余物是二氧化碳 C、丙点对应的剩余物是二氧化碳和一氧化碳 D、丁点对应的剩余物是一氧化碳
A、甲点对应的剩余物是二氧化碳和氧气 B、乙点对应的剩余物是二氧化碳 C、丙点对应的剩余物是二氧化碳和一氧化碳 D、丁点对应的剩余物是一氧化碳二、填空题
-
16. 人类的生活离不开化学。(1)、要解决“白色污染”问题,下列做法正确的是(填字母)。
A 减少使用不必要的塑料制品 B 重复使用某些塑料制品
C 使用一些新型的、可降解的塑料 D 回收各种废弃塑料
(2)、百香果是一种热带水果,含有蛋白质、糖类、油脂、维生素A、维生素C等物质。其中,是由多种氨基酸构成的极为复杂的化合物,缺乏会引起夜盲症。(3)、现代防弹材料的发展如下图所示。
在钛合金、聚酰胺纤维、碳纳米管中,属于金属材料的是 , 属于有机高分子材料的是。
(4)、早在春秋战国时期,我国就开始生产和使用铁器。请用化学方程式表示以磁铁矿为原料炼铁的原理:17. 工业生产硝酸的简要流程如下图所示。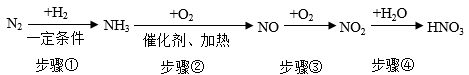 (1)、步骤①利用氮气与氢气在一定条件下合成氨气。通过分离液态空气可以得到氮气,其原理是利用液态氮和液态氧的不同;将水蒸气通过赤热的焦炭层可以得到氢气,其原理是 ,该反应属于(写基本反应类型)。(2)、步骤②发生反应的化学方程式为 , 使用催化剂的目的是。(3)、步骤③和④也可以表示硝酸型酸雨的形成原理。我们把的降雨称为酸雨。(4)、请写出在实验室甲用pH试纸测定溶液酸碱度的具体操作:。18. 氧气和二氧化碳都是空气的成分。(1)、写出化学方程式:
(1)、步骤①利用氮气与氢气在一定条件下合成氨气。通过分离液态空气可以得到氮气,其原理是利用液态氮和液态氧的不同;将水蒸气通过赤热的焦炭层可以得到氢气,其原理是 ,该反应属于(写基本反应类型)。(2)、步骤②发生反应的化学方程式为 , 使用催化剂的目的是。(3)、步骤③和④也可以表示硝酸型酸雨的形成原理。我们把的降雨称为酸雨。(4)、请写出在实验室甲用pH试纸测定溶液酸碱度的具体操作:。18. 氧气和二氧化碳都是空气的成分。(1)、写出化学方程式:①实验室用氯酸钾和二氧化锰制取氧气。
②实验室用大理石和稀盐酸制取二氧化碳。
(2)、这三种常见化石燃料的燃烧都会产生二氧化碳。大气中二氧化碳的含量不断上升,导致温室效应增强,全球气候变暖。(3)、中国科学院大连化学物理研究所研发的“液态阳光”技术可助力中国完成碳达峰、碳中和目标。“液态阳光”技术的第一步是光能的转化,目前可采用光伏发电的形式:第二步是电解水制取氢气;第三步是二氧化碳和氢气反应制取甲醇。①该技术的第一步实现了将能转化为能。
②该技术的第二步对应的化学方程式为。
③二氧化碳和氢气反应制取甲醇的化学方程式为 。请计算:若生产2t甲醇,消耗二氧化碳的质量是多少? (利用化学方程式进行计算,写出计算过程)
19. 饱和溶液和不饱和溶液是可以相互转化的。(1)、在一般情况下,将饱和溶液转化为不饱和溶液的方法有或升高温度;将不饱和溶液转化为饱和溶液的方法有、蒸发溶剂或降低温度。(2)、已知:20℃时,硝酸钾的溶解度为31.6g;60℃时,硝酸钾的溶解度为110g.20℃时,向烧杯中加入20mL水(水的密度可近似看做lg/cm3),接下来的实验步骤如下表所示:步骤
操作
现象
分析
①
加入5g硝酸钾,搅拌
固体全部溶解
步骤(填序号)形成的溶液是饱和溶液。步骤(填序号)形成的溶液中溶质的质量分数最大,其质量分数为(保留至0.1%)
②
再加5g硝酸钾,搅拌
③
加热至60℃
固体全部溶解
④
再加5g硝酸钾,搅拌
⑤
冷却至20℃
三、推断题
-
20. 图中A~L是初中化学常见的化合物,A、B、F、G、I、L由两种元素组成,其余均由三种元素组成。G可用作大棚蔬菜生产中的气体肥料,K的浓溶液及A、B、E可用作干燥剂,F中各元素的原子个数比为1:3,B与L含有一种相同的元素。图中“一”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去。
 (1)、写出化学式:G。(2)、写出化学方程式:A转化为C。K转化为L。E与F反应。
(1)、写出化学式:G。(2)、写出化学方程式:A转化为C。K转化为L。E与F反应。四、科学探究题
-
21. 酸、碱、盐之间有可能发生复分解反应。(1)、(知识回顾)当两种化合物互相交换成分,生成物中有生成时,复分解反应才可以发生;中和反应属于复分解反应。(2)、(设计实验)请设计实验证明稀盐酸与稀氢氧化钠溶液发生了中和反应,并完成实验报告。实验用品包括烧杯、胶头滴管、玻璃棒、稀盐酸、稀氢氧化钠溶液、酚酞溶液。
实验步骤
实验现象
实验结论
一段时间后溶液由红色变为无色
证明稀盐酸与稀氢氧化钠溶液发生了中和反应
(3)、(查阅资料)电导率传感器用于测量溶液的导电性强弱;一定条件下,电导率的大小能反映离子浓度的大小。(实验探究)取等量的滴有酚酞溶液的氢氧化钡溶液于两个烧杯中,分别向其中逐滴滴加X、Y两种液体,利用磁力搅拌器不断搅拌,利用电导率传感器采集数据,得到图1、图2。


(实验分析)
①根据图1、图2,X、Y两种液体依次为(填字母)。
A 氯化钠溶液 B 硫酸钠溶液 C 蒸馏水 D 稀硫酸
②请填写下表:
图像
烧杯中的现象
化学方程式
相同点
不同点
图1
图2
③图1中,a点所示溶液的溶质是(酚酞除外):图2中,b点所示溶液的电导率不为零的原因。
-