广东省珠海市香洲区2021年中考化学模拟试卷
试卷更新日期:2021-05-21 类型:中考模拟
一、选择题(本大题包括 15 小题,每小题 3 分,共 45 分。每小题列出的四个选项中,只有一个是正确的。请将答题卡上对应题目所选的选项涂黑)
-
1. 酒精在抗击新冠肺炎疫情中发挥了重要作用。下列过程涉及化学变化的是( )A、酒精挥发 B、酒精稀释 C、酒精溶解碘 D、酒精消毒2. 2021 年 6 月 1 日珠海将全面实施垃圾分类管理。餐后用过的纸巾属于( )A、
 B、
B、 C、
C、 D、
D、 3. 下列实验操作正确的是( )A、稀释浓硫酸
3. 下列实验操作正确的是( )A、稀释浓硫酸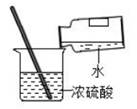 B、配制 NaCl 溶液
B、配制 NaCl 溶液  C、称量 NaOH 固体
C、称量 NaOH 固体  D、蒸发结晶
D、蒸发结晶  4. 每年 5 月 20 日是“中国学生营养日”。下列有关饮食与健康的说法中正确的是( )A、青少年正在长身体,应多吃富含蛋白质的肉类,不吃或少吃蔬菜 B、糖类、油脂、蛋白质都属于人体所需的基本营养素 C、将亚硝酸钠(NaNO2 )用作肉类保鲜剂 D、人体缺乏维生素 C 会引起夜盲症5. 下列物质的用途主要由其物理性质决定的是( )A、活性炭用作冰箱除臭剂 B、氢氧化钠用作炉具清洁剂 C、氮气用作焊接金属的保护气 D、氢氧化铝用于治疗胃酸过多6. 火星上存在针铁矿[FeO(OH)]和黄钾铁矾,从而证明火星表面曾经存在过水。已知两种矿物中铁元素的化合价相同,则黄钾铁矾[KFe3(SO4)2(OH) n ]中 n 值为( )A、4 B、5 C、6 D、77. “如图”所示的实验用于探究可燃物燃烧的条件。下列选项不正确的是( )
4. 每年 5 月 20 日是“中国学生营养日”。下列有关饮食与健康的说法中正确的是( )A、青少年正在长身体,应多吃富含蛋白质的肉类,不吃或少吃蔬菜 B、糖类、油脂、蛋白质都属于人体所需的基本营养素 C、将亚硝酸钠(NaNO2 )用作肉类保鲜剂 D、人体缺乏维生素 C 会引起夜盲症5. 下列物质的用途主要由其物理性质决定的是( )A、活性炭用作冰箱除臭剂 B、氢氧化钠用作炉具清洁剂 C、氮气用作焊接金属的保护气 D、氢氧化铝用于治疗胃酸过多6. 火星上存在针铁矿[FeO(OH)]和黄钾铁矾,从而证明火星表面曾经存在过水。已知两种矿物中铁元素的化合价相同,则黄钾铁矾[KFe3(SO4)2(OH) n ]中 n 值为( )A、4 B、5 C、6 D、77. “如图”所示的实验用于探究可燃物燃烧的条件。下列选项不正确的是( )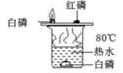 A、铜片上的两处磷发生的现象,得出燃烧的条件为温度要达到可燃物的着火点 B、图中三处磷发生的现象可得出燃烧的条件是:①温度要达到可燃物的着火点;②可燃物要与氧气接触 C、磷燃烧的化学方程式为 4P+5O 2 2P 5 O 2 D、该实验是运用了控制变量法的对比实验8. 下列对化学肥料的认识正确的是( )A、NaNO3 是一种常见的复合肥料 B、铵态氮肥与草木灰混用,不会降低肥效 C、棉花叶片枯黄,应施用磷肥 D、通过闻气味的方法可以区分 NH4HCO3 和 KCl9. 居里夫人发现了放射性元素镭,荣获诺贝尔物理奖和化学奖。如图是镭元素在元素周期表中的信息,下列有关该元素说法正确的是( )
A、铜片上的两处磷发生的现象,得出燃烧的条件为温度要达到可燃物的着火点 B、图中三处磷发生的现象可得出燃烧的条件是:①温度要达到可燃物的着火点;②可燃物要与氧气接触 C、磷燃烧的化学方程式为 4P+5O 2 2P 5 O 2 D、该实验是运用了控制变量法的对比实验8. 下列对化学肥料的认识正确的是( )A、NaNO3 是一种常见的复合肥料 B、铵态氮肥与草木灰混用,不会降低肥效 C、棉花叶片枯黄,应施用磷肥 D、通过闻气味的方法可以区分 NH4HCO3 和 KCl9. 居里夫人发现了放射性元素镭,荣获诺贝尔物理奖和化学奖。如图是镭元素在元素周期表中的信息,下列有关该元素说法正确的是( ) A、镭元素属于非金属元素 B、镭的元素符号为 Ra C、镭的相对原子质量为 226g D、镭原子的中子数为 8810. 医用口罩生产过程中常用环氧乙烷灭菌。有关环氧乙烷的说法正确的是( )
A、镭元素属于非金属元素 B、镭的元素符号为 Ra C、镭的相对原子质量为 226g D、镭原子的中子数为 8810. 医用口罩生产过程中常用环氧乙烷灭菌。有关环氧乙烷的说法正确的是( ) A、环氧乙烷中碳、氢、氧原子个数比 4∶2∶1 B、环氧乙烷的相对分子质量是 42 C、环氧乙烷是一种有机化合物 D、环氧乙烷中氧元素的质量分数最大11. 下列物质的鉴别和除杂方案正确的是( )
A、环氧乙烷中碳、氢、氧原子个数比 4∶2∶1 B、环氧乙烷的相对分子质量是 42 C、环氧乙烷是一种有机化合物 D、环氧乙烷中氧元素的质量分数最大11. 下列物质的鉴别和除杂方案正确的是( )选项
实验目的
实验方案
A
鉴别 CH4和 H2
点燃后分别在火焰上方罩一个冷而干燥的烧杯
B
鉴别羊毛和涤纶
分别取样,灼烧,闻气味
C
除去 KNO3溶液中的 KCl
加入过量 AgNO3溶液,过滤
D
除去铁粉中的少量铜粉
加入足量稀盐酸,充分反应后过滤、洗涤、干燥
A、A B、B C、C D、D12. 实验课上,同学们设计了下面四个实验,其中能达到目的的是( )A、验证分子在不断运动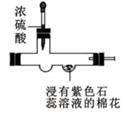 B、实验室制取氢气
B、实验室制取氢气 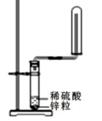 C、验证铁、铜、银金属活动性
C、验证铁、铜、银金属活动性  D、证明酸碱发生反应
D、证明酸碱发生反应  13. 20℃时,甲、乙两固体在水中最多能溶解的质量如图所示。下列描述不正确的是( )
13. 20℃时,甲、乙两固体在水中最多能溶解的质量如图所示。下列描述不正确的是( ) A、20℃时,甲的溶解度比乙大 B、20℃时,20g 水和 40g 水中最多溶解甲的质量不相等,但形成的饱和溶液溶质的质量分数相等 C、20℃时,a 点表示甲、乙两固体所对应的溶液都是不饱和溶液 D、20℃时,乙的溶解度为 60g14. 培养学生的“宏观辨识与微观探析”素养是学习化学必备的思维方式,如图一种工业制备氢气的微观示意图,下列表达完全正确的是( )
A、20℃时,甲的溶解度比乙大 B、20℃时,20g 水和 40g 水中最多溶解甲的质量不相等,但形成的饱和溶液溶质的质量分数相等 C、20℃时,a 点表示甲、乙两固体所对应的溶液都是不饱和溶液 D、20℃时,乙的溶解度为 60g14. 培养学生的“宏观辨识与微观探析”素养是学习化学必备的思维方式,如图一种工业制备氢气的微观示意图,下列表达完全正确的是( ) A、该反应的两种反应物的质量比为 8∶9 B、该反应的生成物有三种 C、反应前后,分子和原子的种类都没有发生改变 D、该反应的化学方程式为 CH4 +H2O =CO+H 215. 图为采用数字化实验,由传感器采集实验相关信息描绘出曲线,其中物质 X 表示能与二氧化碳反应的某液体,纵坐标 Y表示烧杯中某个量。下列对物质 X 与纵坐标 Y 的图像不正确是( )
A、该反应的两种反应物的质量比为 8∶9 B、该反应的生成物有三种 C、反应前后,分子和原子的种类都没有发生改变 D、该反应的化学方程式为 CH4 +H2O =CO+H 215. 图为采用数字化实验,由传感器采集实验相关信息描绘出曲线,其中物质 X 表示能与二氧化碳反应的某液体,纵坐标 Y表示烧杯中某个量。下列对物质 X 与纵坐标 Y 的图像不正确是( ) A、X 是水,Y 是溶液的质量
A、X 是水,Y 是溶液的质量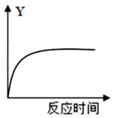 B、X 是水,Y 是溶液的 pH
B、X 是水,Y 是溶液的 pH  C、X是NaOH溶液,Y 是溶质的质量
C、X是NaOH溶液,Y 是溶质的质量  D、X 是 Ca(OH) 2 溶液,Y 是溶液中钙元素的质量
D、X 是 Ca(OH) 2 溶液,Y 是溶液中钙元素的质量 
二、填空题(本大题包括 2 小题,共 16 分)
-
16. 请用化学知识完成以下问题。(1)、水电解生成氢气和氧气,电解水实验可以证明水是由.组成。
水的硬度影响着人们的生活,用.可以鉴别硬水和软水,生活中降低水硬度的方法是。
(2)、中国高铁里程已突破 3.9 万公里,位居世界第一,已经把其他国家远远甩在了身后。高铁无缝钢轨焊接时用到了铝热焊,其反应原理是铝与氧化铁在高温下发生了置换反应,反应的化学方程式为.。
(3)、目前,多数汽车使用的燃料是汽油和柴油,下列说法不正确的是. 。A、石油炼制可获得汽油和柴油,汽油和柴油属于可再生能源 B、在汽油中加入适量乙醇作汽车燃料,可减少汽车尾气的污染 C、氢能源代替汽油和柴油作汽车燃料,具有放热多、无污染等优点(4)、下图中装置可比较两种气体引起温室效应的程度,光照一段时间后,水柱向右移动,说明.引起温室效应的程度更强。
 (5)、4 月 13 日,日本政府决定将福岛核电站的百万吨核废水排放入海。福岛核废水中含有的放射性物质氚是一种危害非常大的放射性核素。下图为氢原子和氚原子的结构示意图,氚原子和氢原子.(填“是”或“否”)同种元素,它们的区别是数不同。
(5)、4 月 13 日,日本政府决定将福岛核电站的百万吨核废水排放入海。福岛核废水中含有的放射性物质氚是一种危害非常大的放射性核素。下图为氢原子和氚原子的结构示意图,氚原子和氢原子.(填“是”或“否”)同种元素,它们的区别是数不同。
 17. 如图表示碳元素的化合价与物质类别关系。
17. 如图表示碳元素的化合价与物质类别关系。 (1)、A 点对应的物质类别是.;C 点对应物质的用途有.;E 点表示物质的化学式为.(任写一种)。(2)、图中具有还原性物质的化学式为.。(3)、C→B 的化学方程式为.。
(1)、A 点对应的物质类别是.;C 点对应物质的用途有.;E 点表示物质的化学式为.(任写一种)。(2)、图中具有还原性物质的化学式为.。(3)、C→B 的化学方程式为.。三、(本大题包括 2 小题,共 19 分)
-
18. 化学是一门以实验为基础的学科。题 18-1 图是六种可以制得氧气的途径,如图为实验室制气常用的装置。
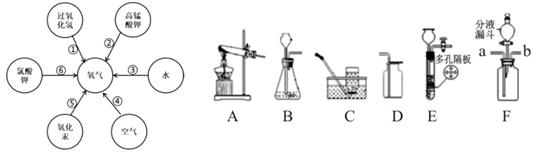 (1)、“绿色化学”倡导节约资源和节能环保等理念,根据“绿色化学”理念,在图中选择实验室制取氧气的最佳途径是.(填序号),该反应的化学方程式为.。
(1)、“绿色化学”倡导节约资源和节能环保等理念,根据“绿色化学”理念,在图中选择实验室制取氧气的最佳途径是.(填序号),该反应的化学方程式为.。途径⑥需要添加 Mn2 作催化剂,若反应结束后回收 MnO2 固体,需进行的操作是溶解、.、洗涤、烘干。
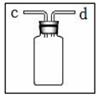
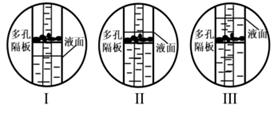
(2)、若选择题图中的途径②制备并收集较为纯净的氧气,应图中选择的发生和收集装置分别为;图中装置用于排空气法收集氧气,c 为进气口,请将瓶内导管补画完整。(3)、图是使用图 装置制取二氧化碳时液面变化的情景。当液面变化按→→顺序时(填序号),导管上的活塞是在被.状态(填“打开”或“关闭”)。(4)、若用图中 F 装置验证二氧化碳使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的以下实验操作顺序是(填序号,可重复选用)。①从 b 端通氮气;②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中;③从 a 端通二氧
化碳;④从分液漏斗中滴加适量水。
 19. 足球比赛会用到“嗅盐”让昏迷球员快速恢复意识。同学们对嗅盐产生了好奇,并对其成分进行如下探究。
19. 足球比赛会用到“嗅盐”让昏迷球员快速恢复意识。同学们对嗅盐产生了好奇,并对其成分进行如下探究。【查阅资料】
①嗅盐是由一种盐类物质和香料(香料不参与以下探究中的任何反应)组成,能释放出氨味气体,对人体神经会产生强烈的刺激作用,过量吸入会危害健康。
②氯化钙稀溶液与碳酸氢铵溶液不发生反应。
③氨气极易溶于水,且能与硫酸化合生成硫酸铵。
【提出问题】嗅盐中盐类物质是什么?
(1)、【实验探究】小 珠 的实验方案
现象
结论

嗅盐与(填俗名)
混合研磨
闻到刺激性气味且试纸变
嗅盐中含有 NH4+

嗅盐中含有 CO 32- ,嗅盐
是(NH4)2CO3
(2)、【反思与评价】小海认为小珠最后的实验结论不严谨,理由是:.。(3)、小海通过补做如下实验,进而确认了小珠的结论。小 海 的实验方案
现象
结论

有白色沉淀出现
小海的实验目的是排除溴盐中含有④(填离子符号)的可能性,该实验确认了嗅盐中所含盐类物质是碳酸铵,小珠的实验结论正确。
(4)、【再探究】小湖利用右图所示装置测定嗅盐中碳酸铵的质量分数(碳酸铵受热分解可生成两种气体和常温下呈液态的一种氧化物)。
【实验步骤】①稍加热溴盐,使其充分分解。
②反应结束后,向双通管通入一段时间的空气。
【数据记录】实验称取溴盐样品质量为 m 1 ,反应前、后烧杯及烧杯内溶液的总质量分别为 m 2和 m 3 。
【实验分析及数据处理】碳酸铵受热分解的化学方程式为:.。通过测得数据计算出嗅盐中碳酸铵的质量分数为.(用 m1 、m 2 、m 3 表示)。
(5)、【反思与评价】小湖的实验装置中倒置的漏斗既可以. , 又可以防止倒吸,同时还可防止氨气污染环境。
四、(本大题包括 1 小题,共 10 分)
-
20. 钢铁锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。
防止钢铁生锈最常用的方法是在钢铁表面涂上一层保护膜。有一种防锈蚀的工艺叫烤蓝,
烤蓝的原理是在钢铁表面生成一定厚度和强度的致密的氧化层。主要工艺流程如下:
 (1)、烤蓝工艺在钢铁表面形成的氧化膜也是磁铁矿的主要成分,其化学式为.。(2)、除锈液与铁锈反应的化学方程式为.。除锈前若无水洗步骤,除锈液的使用量将.(填“增大”、“减小”或“不变”)。(3)、除锈时,工件浸入除锈液 3~5min 就要取出水洗,不能长时间浸在其中的原因是.(用化学方程式表示) 。(4)、烤蓝液为含有氧化剂和苛性钠的混合溶液,该过程发生多个反应,其中一个反应的化学方程式为:8Fe + 3NaNO3 + 5NaOH + 2H2O = 4Na2Fe2O4 + 3。(5)、质检时将工件浸入 2%的硫酸铜溶液里,在室温下保持 20s 后取出,用水洗净表面,若不显示铜色则合格。出现铜色反应的化学方程式为.。(6)、搪瓷,又称珐琅,也是防锈方法之一。它是将无机玻璃质材料(增强材料)通过熔融凝于金属(基体)上并与金属牢固结合在一起。搪瓷是一种.材料。
(1)、烤蓝工艺在钢铁表面形成的氧化膜也是磁铁矿的主要成分,其化学式为.。(2)、除锈液与铁锈反应的化学方程式为.。除锈前若无水洗步骤,除锈液的使用量将.(填“增大”、“减小”或“不变”)。(3)、除锈时,工件浸入除锈液 3~5min 就要取出水洗,不能长时间浸在其中的原因是.(用化学方程式表示) 。(4)、烤蓝液为含有氧化剂和苛性钠的混合溶液,该过程发生多个反应,其中一个反应的化学方程式为:8Fe + 3NaNO3 + 5NaOH + 2H2O = 4Na2Fe2O4 + 3。(5)、质检时将工件浸入 2%的硫酸铜溶液里,在室温下保持 20s 后取出,用水洗净表面,若不显示铜色则合格。出现铜色反应的化学方程式为.。(6)、搪瓷,又称珐琅,也是防锈方法之一。它是将无机玻璃质材料(增强材料)通过熔融凝于金属(基体)上并与金属牢固结合在一起。搪瓷是一种.材料。五、(本大题包括 1 小题,共 10 分)
-
21. 工业生产的氯化钙溶液中常混有盐酸,为测定该溶液中氯化钙的质量分数,某同学做了如下实验:如图,取该溶液 5.0g 于烧杯中,每秒滴入 4 滴质量分数为 5.0%的碳酸钠溶液至过量(1 滴约为 0.05g),溶液 pH 的变化如图所示。
 (1)、图中,A 点溶液中的溶质是.(填化学式)。(2)、请计算该溶液中氯化钙的质量分数(写出计算过程,精确到 0.1%)。(3)、图中 BC 段越长说明该溶液中氯化钙的质量分数越((填“大”或“小”)。
(1)、图中,A 点溶液中的溶质是.(填化学式)。(2)、请计算该溶液中氯化钙的质量分数(写出计算过程,精确到 0.1%)。(3)、图中 BC 段越长说明该溶液中氯化钙的质量分数越((填“大”或“小”)。
-