广东省深圳市福田区2021年中考化学二模试卷
试卷更新日期:2021-05-21 类型:中考模拟
一、单项选择题I (本大题共8小题,每小题1.5分,共12分。在每小题列出的四个选项中,只有一个选项最符合题意。)
-
1. 下列中国传统文化中,没有发生化学变化的是( )A、造纸 B、剪纸 C、酿酒 D、制陶2. 实验是学习化学的重要途径。下列实验操作正确的是( )A、加入铁钉
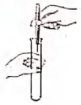 B、过滤
B、过滤 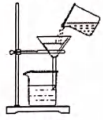 C、称取NaCl
C、称取NaCl  D、测溶液pH
D、测溶液pH  3. 下列化学符号中数字“2”表示的意义不符合的是( )A、 :两个铵根离子 B、H2O:一个水分子中含有一个氢分子 C、Mg2+:一个镁离子带两个单位正电荷 D、 :氧化铜中铜元素化合价为正二价4. 我国自主研发的新冠疫苗,主要原料是胰蛋白酶,其中一种胰蛋白酶的化学式为C6H15O12P3 , 相对分子质量为372。对于该胰蛋白酶说法正确的是( )A、该胰蛋白酶是一种高分子化合物 B、该胰蛋白酶由36种元素组成 C、该胰蛋白酶中碳、氧元素质量比为3:8 D、该胰蛋白酶一个分子的质量为3725. 模型认知是建立宏观与微观联系的重要思维方法。如图为某反应的微观过程,下列说法正确的是( )
3. 下列化学符号中数字“2”表示的意义不符合的是( )A、 :两个铵根离子 B、H2O:一个水分子中含有一个氢分子 C、Mg2+:一个镁离子带两个单位正电荷 D、 :氧化铜中铜元素化合价为正二价4. 我国自主研发的新冠疫苗,主要原料是胰蛋白酶,其中一种胰蛋白酶的化学式为C6H15O12P3 , 相对分子质量为372。对于该胰蛋白酶说法正确的是( )A、该胰蛋白酶是一种高分子化合物 B、该胰蛋白酶由36种元素组成 C、该胰蛋白酶中碳、氧元素质量比为3:8 D、该胰蛋白酶一个分子的质量为3725. 模型认知是建立宏观与微观联系的重要思维方法。如图为某反应的微观过程,下列说法正确的是( )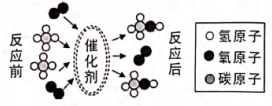 A、反应物分子个数比为1:1 B、此反应属于化合反应 C、反应中两种化合物的质量比为1:1 D、反应前后催化剂的物理性质保持不变6. 下列为某同学对化学知识的归纳,其中有错误的是( )A、空气的组成:氮气、氧气、氢气、稀有气体等 B、常见的合成材料:塑料、合成纤维和合成橡胶等 C、燃烧的三个条件:可燃物、氧气(或空气)、温度达到着火点 D、人类六大基本营养素:蛋白质、糖类、油脂、维生素、无机盐和水7. 学习化学要构建基本理念,对以下基本观念的认识,错误的是( )A、守恒观:化学反应前后,元素的种类不变 B、元素观:一切物质都是由元素组成的 C、微粒观:金刚石是由碳分子构成的 D、结构观:水和过氧化氢的分子构成不同,化学性质也不同8. 氮化镍( GaN )是生产5G芯片的关键材料之一。如图为元素周期表的一部分和镓原子结构示意图,下列说法中正确的是( )
A、反应物分子个数比为1:1 B、此反应属于化合反应 C、反应中两种化合物的质量比为1:1 D、反应前后催化剂的物理性质保持不变6. 下列为某同学对化学知识的归纳,其中有错误的是( )A、空气的组成:氮气、氧气、氢气、稀有气体等 B、常见的合成材料:塑料、合成纤维和合成橡胶等 C、燃烧的三个条件:可燃物、氧气(或空气)、温度达到着火点 D、人类六大基本营养素:蛋白质、糖类、油脂、维生素、无机盐和水7. 学习化学要构建基本理念,对以下基本观念的认识,错误的是( )A、守恒观:化学反应前后,元素的种类不变 B、元素观:一切物质都是由元素组成的 C、微粒观:金刚石是由碳分子构成的 D、结构观:水和过氧化氢的分子构成不同,化学性质也不同8. 氮化镍( GaN )是生产5G芯片的关键材料之一。如图为元素周期表的一部分和镓原子结构示意图,下列说法中正确的是( ) A、图中a=7,b=8 B、氮化镓的相对分子质量约为84g C、镓原子在反应中易得到电子 D、镓元素与氧元素形成的化合物化学式为GaO
A、图中a=7,b=8 B、氮化镓的相对分子质量约为84g C、镓原子在反应中易得到电子 D、镓元素与氧元素形成的化合物化学式为GaO二、单项选择题(本大题共4小题,每小题2分,共8分。在每小题列出的四个选项中,只有一个选项最符合题意。)
-
9. 向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是( )A、
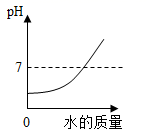 B、
B、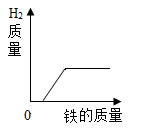 C、
C、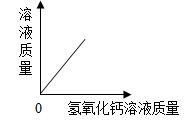 D、
D、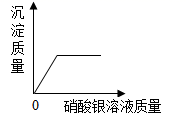 10. 如图是初中化学中常见物质间的转化关系,其中A、B、C、D为氧化物,C是使地球产生温室效应的一种气体,丙是一种紫红色金属。(图中部分生成物已略去)下列叙述错误的是( )
10. 如图是初中化学中常见物质间的转化关系,其中A、B、C、D为氧化物,C是使地球产生温室效应的一种气体,丙是一种紫红色金属。(图中部分生成物已略去)下列叙述错误的是( )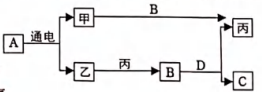 A、A的化学式是H2O B、甲生成丙的化学反应类型为置换反应 C、A与C反应的化学方程式为:CO2+H2O=H2CO3 D、在A生成甲和乙的化学反应中,所得甲乙两种气体的质量比是2:111. 甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是( )
A、A的化学式是H2O B、甲生成丙的化学反应类型为置换反应 C、A与C反应的化学方程式为:CO2+H2O=H2CO3 D、在A生成甲和乙的化学反应中,所得甲乙两种气体的质量比是2:111. 甲、乙、丙三种物质的溶解度曲线如图所示,下列说法正确的是( ) A、t1℃甲、乙两物质溶液的溶质质量分数相等 B、t2℃配制300g甲的饱和溶液,需要固体甲的质量为100g C、t1℃甲、乙、丙三种饱和溶液降温到t1℃,甲析出晶体质量比乙多 D、t1℃等质量的甲、乙、丙三种固体配制成该温度下的饱和溶液,所得溶液的质量大小关系:甲=乙>丙12. 下列设计的实验方案中,你认为不可行的是( )
A、t1℃甲、乙两物质溶液的溶质质量分数相等 B、t2℃配制300g甲的饱和溶液,需要固体甲的质量为100g C、t1℃甲、乙、丙三种饱和溶液降温到t1℃,甲析出晶体质量比乙多 D、t1℃等质量的甲、乙、丙三种固体配制成该温度下的饱和溶液,所得溶液的质量大小关系:甲=乙>丙12. 下列设计的实验方案中,你认为不可行的是( )选项
实验目的
方法或试剂
A
鉴别固体NaOH、NaCl、 NH4NO3
分别加入水.
B
验证Zn、Cu、Ag的金属活动顺序
稀硫酸、AgNO3溶液
C
除去CaO中混有的CaCO3
加入适量的水,过滤
D
区分硬水和软水
加肥皂水,振荡
A、A B、B C、C D、D三、非选择题(4小题,共30分)
-
13. 掌握实验室制取常见气体的方法是初中生必备的化学素养。实验室里现有氯酸钾、二氧化锰、稀硫酸、石灰石和稀盐酸,以及下列仪器:
 (1)、利用上述仪器可以制取二氧化碳,其中发生装置的仪器组合是(填序号) 。写出反应的化学方程式:。(2)、若补充一种仪器(填仪器名称),再利用上述提供的药品和仪器,还可以制取氧气,反应的化学方程式为; 若用如图⑨装置收集氧气,氧气应从(填“a”或“b" )端进入。14. 已知氢氧化锂的化学性质与氢氧化钠相似,请预测氢氧化锂[LiOH]的化学性质,说明预测的依据,并设计实验验证。经查阅资料,锂的化合物相关性质如下:
(1)、利用上述仪器可以制取二氧化碳,其中发生装置的仪器组合是(填序号) 。写出反应的化学方程式:。(2)、若补充一种仪器(填仪器名称),再利用上述提供的药品和仪器,还可以制取氧气,反应的化学方程式为; 若用如图⑨装置收集氧气,氧气应从(填“a”或“b" )端进入。14. 已知氢氧化锂的化学性质与氢氧化钠相似,请预测氢氧化锂[LiOH]的化学性质,说明预测的依据,并设计实验验证。经查阅资料,锂的化合物相关性质如下:物质
LiOH
LiCl
Li2CO3
Li2SO4
在水中的溶解性
易溶
易溶
难溶于水,沉淀呈白色
易溶
限选试剂:酚酞溶液、CuSO4 溶液、NaOH溶液、Na2CO3 溶液、稀盐酸。
预测
预测的依据
实验操作与预期现象
⑴能够与含CO32-的可溶性盐反应
LiOH溶液中含Li+ , Li2CO3难溶于水
取少量LiOH溶液于试管中,加入Na2CO3溶液,如果观察到有生成,则预测成立
⑵能够与含Cu2+的可溶性盐反应
LiOH溶液中含OH- , Cu(OH)2难溶于水
取少量LiOH溶液于试管中,加入溶液,如果观察到有生成,则预测成立
⑶能够与 (填物质类别)发生中和反应
LiOH溶液中含 (填化学符号)
取少最LiOH溶液于试管中,加入 , 如果观察到 , 则预测成立
15. 碲(Te)广泛用于彩色玻璃和陶瓷工艺。用某工业废渣(主要含有TeO2、少量Ag、Au)为原料制备碲的一种工艺流程如下:
请回答下列问题:
(1)、TeO2中氧元素的化合价为-2,则Te元素的化合价为 ;废渣会在“碱浸”前先粉碎,目的是。(2)、实验室进行过滤操作时,用到的玻璃仪器有烧杯、玻璃棒和;(3)、滤液1中的两种溶质是H2SO4和(填化学式);(4)、上述工艺流程中设计“废渣→……→TeO2的目的是;(5)、类比CO2与NaOH的反应,写出“碱浸”时发生反应的化学方程式: ;(6)、“酸溶”后,在所得的TeCl4溶液中通入SO2 , 反应生成固态碲和初中化学中常见的两种酸,则该反应的化学方程式是。16. 实验室有一瓶已经部分变质的Ca(OH)2固体,现向锥形瓶中加入10g这种部分变质的样品,再加入溶质质量分数为10%的稀盐酸溶液,产生气体的质量与加入稀盐酸溶液的质量关系如图所示: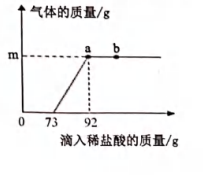 (1)、Ca(OH)2由(填元素名称)元素组成;(2)、与Ca(OH)2反应消耗的稀盐酸的质量为g;(3)、b点溶液中的溶质是(填化学式);(4)、求原样品中Ca(OH)2的质量分数(写出计算过程)。
(1)、Ca(OH)2由(填元素名称)元素组成;(2)、与Ca(OH)2反应消耗的稀盐酸的质量为g;(3)、b点溶液中的溶质是(填化学式);(4)、求原样品中Ca(OH)2的质量分数(写出计算过程)。