浙教版科学八年级下册第三章 空气与生命 综合测试卷
试卷更新日期:2021-05-21 类型:单元试卷
一、单选题
-
1. 如图所示分别为水电解实验的装置图和微观示意图,下列有关说法错误的是( )
 A、图甲中b管产生的气体能使带火星的木条复燃 B、该反应属于分解反应,反应过程中元素化合价不变 C、由图乙可知原子是化学变化的最小微粒 D、该实验证明水是由氢元素和氧元素组成2. 水是化学实验中常见且用途广泛的一种物质。对下列各实验中水的主要作用的解释不合理的是( )A、硫在氧气中燃烧--集气瓶中的水:吸收放出的热量 B、测定空气中氧气含量--量筒中的水:通过水体积变化得到氧气体积 C、细铁丝在氧气中燃烧--集气瓶中的水:防止集气瓶炸裂 D、探究燃烧的条件--烧杯中的水:加热铜片,隔绝空气3. 下列反应中,既属于化合反应,又属于氧化反应的是( )A、铁+氧气→四氧化三铁(点燃) B、水→氢气+氧水(通电) C、锌+稀硫酸→硫酸锌+氢气 D、甲烷+氧气→燃二氧化碳+水(点燃)4. 有M、N、X、Y四种物质,在一定条件下充分反应后,测得反应物和产物在反应前后的质量如表所示,对该反应的下列说法错误的是( )
A、图甲中b管产生的气体能使带火星的木条复燃 B、该反应属于分解反应,反应过程中元素化合价不变 C、由图乙可知原子是化学变化的最小微粒 D、该实验证明水是由氢元素和氧元素组成2. 水是化学实验中常见且用途广泛的一种物质。对下列各实验中水的主要作用的解释不合理的是( )A、硫在氧气中燃烧--集气瓶中的水:吸收放出的热量 B、测定空气中氧气含量--量筒中的水:通过水体积变化得到氧气体积 C、细铁丝在氧气中燃烧--集气瓶中的水:防止集气瓶炸裂 D、探究燃烧的条件--烧杯中的水:加热铜片,隔绝空气3. 下列反应中,既属于化合反应,又属于氧化反应的是( )A、铁+氧气→四氧化三铁(点燃) B、水→氢气+氧水(通电) C、锌+稀硫酸→硫酸锌+氢气 D、甲烷+氧气→燃二氧化碳+水(点燃)4. 有M、N、X、Y四种物质,在一定条件下充分反应后,测得反应物和产物在反应前后的质量如表所示,对该反应的下列说法错误的是( ) A、该反应属于分解反应 B、该反应属于化合反应 C、该反应生成的N、Y的质量比为9:8 D、M在反应中可能作催化剂5. 在自然界中,生物的某些生命活动和生理功能可以通过坐标曲线的方式形象地表达出来。对于下列四个曲线图的分析,正确的是( )
A、该反应属于分解反应 B、该反应属于化合反应 C、该反应生成的N、Y的质量比为9:8 D、M在反应中可能作催化剂5. 在自然界中,生物的某些生命活动和生理功能可以通过坐标曲线的方式形象地表达出来。对于下列四个曲线图的分析,正确的是( ) A、甲图可用来表示从菜豆种子萌发到发育成幼苗过程中水分含量的变化 B、乙图是人体呼吸时肺容积的变化曲线图,bc 段膈顶上升 C、丙图表示人体消化酶活性随温度变化的情况,说明人在寒冷时消化食物的能力减弱 D、丁图是某条食物链上生物含有毒物质的相对数量关系,这条食物链是丙→甲→乙→丁6. 钨丝灯管在使用过程中,由于钨丝(W)的温度可达3000℃以上,导致钨升华而使灯丝变细。加入固态碘(I2)可延缓灯丝变细,其原理如图所示。下列分析正确的是( )
A、甲图可用来表示从菜豆种子萌发到发育成幼苗过程中水分含量的变化 B、乙图是人体呼吸时肺容积的变化曲线图,bc 段膈顶上升 C、丙图表示人体消化酶活性随温度变化的情况,说明人在寒冷时消化食物的能力减弱 D、丁图是某条食物链上生物含有毒物质的相对数量关系,这条食物链是丙→甲→乙→丁6. 钨丝灯管在使用过程中,由于钨丝(W)的温度可达3000℃以上,导致钨升华而使灯丝变细。加入固态碘(I2)可延缓灯丝变细,其原理如图所示。下列分析正确的是( )
 A、该灯管中的钨只发生物理变化 B、该灯管中的W和I2均属于单质 C、反应①中碘元素的化合价升高 D、反应②属于化合反应7. 如图所示,①为制取氧气的发生装置(气密性良好),其中的燃烧匙可以上下移动。②和③为氧气的收集装置。小金欲制取一瓶干燥的氧气,下列分析正确的是( )
A、该灯管中的钨只发生物理变化 B、该灯管中的W和I2均属于单质 C、反应①中碘元素的化合价升高 D、反应②属于化合反应7. 如图所示,①为制取氧气的发生装置(气密性良好),其中的燃烧匙可以上下移动。②和③为氧气的收集装置。小金欲制取一瓶干燥的氧气,下列分析正确的是( ) A、在①中,将MnO2浸入H2O2溶液,MnO2可分解产生氧气 B、若用装置②的方法收集氧气,需等到导管口气泡均匀并连续冒出时才可收集 C、若用装置③的方法收集氧气,可将带火星的木条放入瓶中进行验满 D、将装置①分别与装置②或③连接,均能达到实验目的8. 生物体的结构和功能相适应的实例很多,下列说法不正确的是( )A、肺泡壁由一层扁平上皮细胞构成,利于气体交换 B、小肠的内表面有许多皱襞和绒毛,利于营养吸收 C、肾小管周围缠绕着毛细血管,利于发生滤过作用 D、心脏房室间、静脉内有瓣膜,利于防止血液倒流9. 质量守恒定律是化学反应中的重要规律。在催化、加热的条件下,A与B反应生成C和D,反应前后分子变化的微观示意图如右所示,下列说法正确的是( )
A、在①中,将MnO2浸入H2O2溶液,MnO2可分解产生氧气 B、若用装置②的方法收集氧气,需等到导管口气泡均匀并连续冒出时才可收集 C、若用装置③的方法收集氧气,可将带火星的木条放入瓶中进行验满 D、将装置①分别与装置②或③连接,均能达到实验目的8. 生物体的结构和功能相适应的实例很多,下列说法不正确的是( )A、肺泡壁由一层扁平上皮细胞构成,利于气体交换 B、小肠的内表面有许多皱襞和绒毛,利于营养吸收 C、肾小管周围缠绕着毛细血管,利于发生滤过作用 D、心脏房室间、静脉内有瓣膜,利于防止血液倒流9. 质量守恒定律是化学反应中的重要规律。在催化、加热的条件下,A与B反应生成C和D,反应前后分子变化的微观示意图如右所示,下列说法正确的是( ) A、该化学反应属于复分解反应 B、4种物质中,C,D都属于氧化物 C、反应前后,氮元素化合价保持不变 D、该反应物中反应物A与B分子个数比是1:110. 偏二甲肼(C2H8N2)与N2O4反应放出的能量能把火箭送入太空,该化学方程式为C2H8N2+2N2O4=2X↑+3N2↑+4H2O↑,下列说法不正确的是( )A、X的化学式为CO2 B、偏二甲肼中碳元素的质量分数为40% C、该反应属于分解反应 D、生成N2和H2O的质量比为7∶611. 下列实验现象描述正确的是( )A、硫在氧气中燃烧,发出淡蓝色火焰,生成有刺激性气味的气体 B、红磷在空气中燃烧,会冒白雾 C、木炭在氧气中燃烧,会发出白光 D、向澄清石灰水通入二氧化碳,会产生白色的碳酸钙12. 下列说法中正确的是( )A、当温度达到着火点时,所有物质都可以在空气中燃烧 B、架空烧木材燃烧会更旺,是因为提高了空气中氧气的含量 C、物质发生缓慢氧化最终一定引起自燃 D、爆炸不一定是化学变化13. 小明在学习了元素和物质的知识后,进行了梳理,其中正确的是( )A、铁元素的质量分数由高到低:FeO、Fe2O3、Fe3O4、FeS B、氮元素的化合价由高到低:HNO3、NO2、NH3、NO C、地壳中最多的金属元素和非金属元素组成的化合物为:Al2O3 D、空气中主要气体的体积分数由大到小:O2、N2、CO214. 用红磷燃烧测定空气中氧气含量的实验装置如图所示,实验过程中,下列做法说法中正确的是( )
A、该化学反应属于复分解反应 B、4种物质中,C,D都属于氧化物 C、反应前后,氮元素化合价保持不变 D、该反应物中反应物A与B分子个数比是1:110. 偏二甲肼(C2H8N2)与N2O4反应放出的能量能把火箭送入太空,该化学方程式为C2H8N2+2N2O4=2X↑+3N2↑+4H2O↑,下列说法不正确的是( )A、X的化学式为CO2 B、偏二甲肼中碳元素的质量分数为40% C、该反应属于分解反应 D、生成N2和H2O的质量比为7∶611. 下列实验现象描述正确的是( )A、硫在氧气中燃烧,发出淡蓝色火焰,生成有刺激性气味的气体 B、红磷在空气中燃烧,会冒白雾 C、木炭在氧气中燃烧,会发出白光 D、向澄清石灰水通入二氧化碳,会产生白色的碳酸钙12. 下列说法中正确的是( )A、当温度达到着火点时,所有物质都可以在空气中燃烧 B、架空烧木材燃烧会更旺,是因为提高了空气中氧气的含量 C、物质发生缓慢氧化最终一定引起自燃 D、爆炸不一定是化学变化13. 小明在学习了元素和物质的知识后,进行了梳理,其中正确的是( )A、铁元素的质量分数由高到低:FeO、Fe2O3、Fe3O4、FeS B、氮元素的化合价由高到低:HNO3、NO2、NH3、NO C、地壳中最多的金属元素和非金属元素组成的化合物为:Al2O3 D、空气中主要气体的体积分数由大到小:O2、N2、CO214. 用红磷燃烧测定空气中氧气含量的实验装置如图所示,实验过程中,下列做法说法中正确的是( )
 A、若使用的红磷量不足,将会导致测出结果偏小 B、可以用木炭燃烧代替红磷消耗氧气 C、不打开橡胶塞,可用放大镜聚焦太阳光点燃红磷 D、水由导管进入集气瓶,进入的水体积约占集气瓶体积的15. 今年以来,全国各地出现了几次较为严重的雾霾天气,再次引起人们对空气质量的关注。下列关于空气说法正确的是( )A、空气的成分只有氧气和氮气 B、氟利昂的使用会造成臭氧的减少 C、空气中可吸入颗粒物(PM2.5)的多少不影响人体健康 D、二氧化碳在空气中的含量增多会引起温室效应,属于空气污染物16. 为探究物质的燃烧条件,某同学进行了如图所示的实验,下列说法正确的是( )
A、若使用的红磷量不足,将会导致测出结果偏小 B、可以用木炭燃烧代替红磷消耗氧气 C、不打开橡胶塞,可用放大镜聚焦太阳光点燃红磷 D、水由导管进入集气瓶,进入的水体积约占集气瓶体积的15. 今年以来,全国各地出现了几次较为严重的雾霾天气,再次引起人们对空气质量的关注。下列关于空气说法正确的是( )A、空气的成分只有氧气和氮气 B、氟利昂的使用会造成臭氧的减少 C、空气中可吸入颗粒物(PM2.5)的多少不影响人体健康 D、二氧化碳在空气中的含量增多会引起温室效应,属于空气污染物16. 为探究物质的燃烧条件,某同学进行了如图所示的实验,下列说法正确的是( ) A、现象①③说明物质的燃烧需要达到一定的温度 B、现象①②说明白磷的着火点比红磷的着火点低 C、现象②③说明物质燃烧需要氧气 D、现象③说明红磷不是可燃物17. 依据图①②③④分析,下列说法正确的是( )
A、现象①③说明物质的燃烧需要达到一定的温度 B、现象①②说明白磷的着火点比红磷的着火点低 C、现象②③说明物质燃烧需要氧气 D、现象③说明红磷不是可燃物17. 依据图①②③④分析,下列说法正确的是( )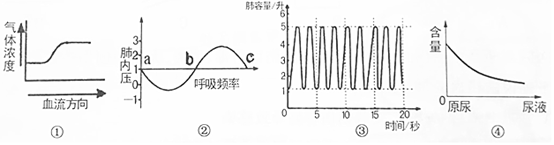 A、图①表示血液流经人体组织细胞氧气含量变化 B、图②曲线a→b段表示肺完成一次吸气过程 C、曲线③表示某人的呼吸频率是20次/分钟 D、图④表示的是水分或无机盐在肾小管中的变化18. 小乐为了检验气体X(纯净物),进行了如图所示实验。观察到实验①中干冷烧杯内壁有水珠,实验②中澄清石灰水变浑浊。则对气体X分析正确的是( )
A、图①表示血液流经人体组织细胞氧气含量变化 B、图②曲线a→b段表示肺完成一次吸气过程 C、曲线③表示某人的呼吸频率是20次/分钟 D、图④表示的是水分或无机盐在肾小管中的变化18. 小乐为了检验气体X(纯净物),进行了如图所示实验。观察到实验①中干冷烧杯内壁有水珠,实验②中澄清石灰水变浑浊。则对气体X分析正确的是( ) A、根据实验①的现象,说明气体X含氢、氧元素 B、根据实验②的现象,说明气体X含碳、氧元素 C、根据实验①②的现象,说明气体X为甲烷气体 D、根据实验①②的现象,说明气体X一定含碳、氢元素19. 如图所示实验中,①、④为用紫色石蕊试液润湿的棉球,②、③为用石蕊试液染成紫色的干燥棉球。下列能说明二氧化碳密度大于空气且能与水反应的现象是( )
A、根据实验①的现象,说明气体X含氢、氧元素 B、根据实验②的现象,说明气体X含碳、氧元素 C、根据实验①②的现象,说明气体X为甲烷气体 D、根据实验①②的现象,说明气体X一定含碳、氢元素19. 如图所示实验中,①、④为用紫色石蕊试液润湿的棉球,②、③为用石蕊试液染成紫色的干燥棉球。下列能说明二氧化碳密度大于空气且能与水反应的现象是( ) A、①变红,③不变红 B、④变红,③不变红 C、①、④变红,②、③不变红 D、④比①先变红,②、③不变红20. 如图,集气瓶中充满二氧化碳,大烧杯中燃着两支高低不等的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( )
A、①变红,③不变红 B、④变红,③不变红 C、①、④变红,②、③不变红 D、④比①先变红,②、③不变红20. 如图,集气瓶中充满二氧化碳,大烧杯中燃着两支高低不等的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( ) A、将观察到高的蜡烛先熄灭 B、不移开玻璃片,实验现象更明显 C、蜡烛会熄灭,是因为二氧化碳降低了蜡烛的着火点 D、去掉烧杯中的1支蜡烛,也能得出同样的实验结论
A、将观察到高的蜡烛先熄灭 B、不移开玻璃片,实验现象更明显 C、蜡烛会熄灭,是因为二氧化碳降低了蜡烛的着火点 D、去掉烧杯中的1支蜡烛,也能得出同样的实验结论二、填空题
-
21. 如图表示空气中各成分所占的体积分数示意图。据此可知:
 (1)、图中A为。(2)、下列有关空气的说法正确的是__________(多选)。A、空气是混合物 B、图中的其他成分指的是稀有气体 C、利用液态空气中各成分的熔点不用,可以分离出A和B D、电流通过充有稀有气体的灯管时,会产生不同颜色的光 E、B气体是一种可燃性气体22. 写出下列反应的化学方程式,并注明反应的基本类型。(1)、铁丝在氧气中燃烧:、。(2)、水在通电的条件下分解:、。23. 无色液体A是一种日常生活中很常见有机燃料,请根据下列转化关系回答:
(1)、图中A为。(2)、下列有关空气的说法正确的是__________(多选)。A、空气是混合物 B、图中的其他成分指的是稀有气体 C、利用液态空气中各成分的熔点不用,可以分离出A和B D、电流通过充有稀有气体的灯管时,会产生不同颜色的光 E、B气体是一种可燃性气体22. 写出下列反应的化学方程式,并注明反应的基本类型。(1)、铁丝在氧气中燃烧:、。(2)、水在通电的条件下分解:、。23. 无色液体A是一种日常生活中很常见有机燃料,请根据下列转化关系回答: (1)、若该液体A在空气中完全燃烧,二氧化碳和水。则该有机物A中一定含有元素,C物质为 (填化学式)。(2)、请写出一个上述关系图中有置换反应的化学方程式。24. 小金为验证稀硫酸的化学性质,分别将铁、氢氧化钠、氧化铜和氯化钡等固体药品加入到四支盛有稀硫酸的试管中。
(1)、若该液体A在空气中完全燃烧,二氧化碳和水。则该有机物A中一定含有元素,C物质为 (填化学式)。(2)、请写出一个上述关系图中有置换反应的化学方程式。24. 小金为验证稀硫酸的化学性质,分别将铁、氢氧化钠、氧化铜和氯化钡等固体药品加入到四支盛有稀硫酸的试管中。 (1)、如图所示为加入某种固体药品后,溶液中主要离子种类及个数比变化的示意图(不考虑离子的大小关系),则加入的固体药品可能是 (填写序号)。A、铁 B、氢氧化钠 C、氧化铜 D、氯化钡(2)、反应后的四支试管中有一支为无色溶液,小金只向试管中加入一种试剂就确定了溶质的成分,则加入的试剂及判断方法为。25. 铁在潮湿空气中易生锈,其反应过程如下:
(1)、如图所示为加入某种固体药品后,溶液中主要离子种类及个数比变化的示意图(不考虑离子的大小关系),则加入的固体药品可能是 (填写序号)。A、铁 B、氢氧化钠 C、氧化铜 D、氯化钡(2)、反应后的四支试管中有一支为无色溶液,小金只向试管中加入一种试剂就确定了溶质的成分,则加入的试剂及判断方法为。25. 铁在潮湿空气中易生锈,其反应过程如下:
 (1)、步骤②中的反应物除Fe(OH)2外,还有(选填“O2”“H2O”或“O2和H2O”)。(2)、已知步骤③为分解反应,若x 为 2,则此分解反应的化学方程式为。26. 下面是“燃烧的条件”实验活动的部分操作示意图:
(1)、步骤②中的反应物除Fe(OH)2外,还有(选填“O2”“H2O”或“O2和H2O”)。(2)、已知步骤③为分解反应,若x 为 2,则此分解反应的化学方程式为。26. 下面是“燃烧的条件”实验活动的部分操作示意图:

(乒乓球的碎片的着火点是180℃,过滤纸碎片的着火点是245℃)
(1)、仪器①的名称为。(2)、实验一加热片刻观察到A中棉球上的酒精燃烧产生蓝色火焰,B中棉球上的水不燃烧,由此得出燃烧的条件之一是。(3)、实验二观察到先燃烧的物质是;若将铜片上的物质换成等量的木屑和煤粉进行实验,观察到木屑先燃烧,说明木屑的着火点比煤粉。(4)、实验三将燃着的蜡烛放在如上图所示的密闭容器中,同时用氧气传感器测出密闭容器中氧气含量的变化,如图所示,下列说法错误的是 (填序号)。A、蜡烛燃烧需要氧气 B、蜡烛燃烧前,密闭容器中氧气的体积分数为21% C、蜡烛熄灭后,密闭容器中还有氧气 D、蜡烛熄灭后,密闭容器中二氧化碳的体积分数为84%三、实验探究题
-
27. 小明设计如图所示的实验装置来同时完成燃烧条件的探究和空气中氧气含量的测定。装置中注射器活塞与内壁摩擦非常小,可忽略不计。实验操作步骤如下:

步骤1:检查装置气密性。
步骤2:将盛有足量白磷的燃烧匙放入空集气瓶中,塞紧塞子,白磷不燃烧。
步骤3:打开集气瓶塞子,往瓶中倒满80℃的热水,并塞紧塞子,白磷仍然不能燃烧。
步骤4:打开K1和K2 , 通过注射器从b管抽水,当瓶中液面刚低于燃烧匙底部时,立即同时关闭K1、K2 , 发现瓶中白磷燃烧,此时读出注射器中水量为V1毫升。
步骤5:待整个装置冷却至室温时,打开K2 , 发现注射器中的水剩余V2毫升。
(1)、结合步骤3、4,说明白磷燃烧需要的条件是。(2)、该实验测得空气中氧气的含量为(用V1、V2来表示)。(3)、小明多次重复上述实验,测得空气中氧气的体积分数远大于21%,原因是。28. 图是实验室制取气体的一些装置,据图回答有关问题。 (1)、写出指定仪器的名称:① ②;(2)、写出用高锰酸钾制取氧气的文字表达式 , 该化学反应的类型是(填基本反应类型),C装置中试管口略向下倾斜的原因是;(3)、若用双氧水(过氧化氢)来制取干燥的氧气,则可选用的发生、收集装置组合为(填字母);(4)、某同学取一段纱窗上的细铁丝,在用自己收集的氧气中做“铁丝在氧气中燃烧”的实验,结果没有观察到“火星四射”的现象。造成此次实验失败的原因不可能是A、收集到的氧气量太少或纯度不高 B、铁丝生锈 C、集气瓶底部没有铺一层细沙 D、铁丝的温度未达到着火点(5)、实验室用高锰酸钾分解制取氧气并用排水法收集的实验。请将下列实验步骤进行正确排序:正确的实验顺序是(填序号)
(1)、写出指定仪器的名称:① ②;(2)、写出用高锰酸钾制取氧气的文字表达式 , 该化学反应的类型是(填基本反应类型),C装置中试管口略向下倾斜的原因是;(3)、若用双氧水(过氧化氢)来制取干燥的氧气,则可选用的发生、收集装置组合为(填字母);(4)、某同学取一段纱窗上的细铁丝,在用自己收集的氧气中做“铁丝在氧气中燃烧”的实验,结果没有观察到“火星四射”的现象。造成此次实验失败的原因不可能是A、收集到的氧气量太少或纯度不高 B、铁丝生锈 C、集气瓶底部没有铺一层细沙 D、铁丝的温度未达到着火点(5)、实验室用高锰酸钾分解制取氧气并用排水法收集的实验。请将下列实验步骤进行正确排序:正确的实验顺序是(填序号)①加热;②检查装置的气密性;③装药品;④用排水法收集氧气;⑤从水槽中取出导管;⑥熄灭酒精灯;⑦固定试管。
29. 氢氧化钠溶液和澄清石灰水具有某些相似的化学性质,但氢氧化钠溶液与二氧化碳反应时没有明显的现象.为了验证氢氧化钠与二氧化碳可以发生化学反应,某小组同学用如图所示装置进行实验.请回答下列问题: (1)、打开止水夹a和c,关闭活塞b,从长颈漏斗向锥形瓶中注入适量的稀盐酸(液封);当观察到烧杯中时,说明集气瓶中已集满二氧化碳气体。(2)、关闭止水夹a,打开活塞b,向集气瓶中加入适量的氢氧化钠溶液,然后关闭活塞b,轻轻摇晃集气瓶,一段时间后可观察到 , 证明氢氧化钠与二氧化碳发生了化学反应;(3)、利用上述实验去验证时氢氧化钠与二氧化碳反应时存在的缺陷有。(4)、为了保证实验的成功,应在实验前检查整套装置的气密性(烧杯中装有适量的水)。小强同学设计的方法为:将最右侧导管放在盛水的烧杯中,打开止水夹a和c,关闭活塞b,向长颈漏斗中缓缓加入一定量的水,若 , 则装置不漏气。30. 植物的光合作用和呼吸作用强度可以用单位时间二氧化碳吸收量内呼吸或释放二氧化碳的量来表示。图甲曲线表示在恒温30℃时,某水藻在不同光照强度下,吸收二氧化碳与释放二氧化碳量的关系。小科为“研究光照强度对植物光合作用速度的影响”,设计如乙图实验装置。此装置的优点在于,可通过控制灯泡功率的大小或调节试管与灯泡的距离,来改变光照的强弱。
(1)、打开止水夹a和c,关闭活塞b,从长颈漏斗向锥形瓶中注入适量的稀盐酸(液封);当观察到烧杯中时,说明集气瓶中已集满二氧化碳气体。(2)、关闭止水夹a,打开活塞b,向集气瓶中加入适量的氢氧化钠溶液,然后关闭活塞b,轻轻摇晃集气瓶,一段时间后可观察到 , 证明氢氧化钠与二氧化碳发生了化学反应;(3)、利用上述实验去验证时氢氧化钠与二氧化碳反应时存在的缺陷有。(4)、为了保证实验的成功,应在实验前检查整套装置的气密性(烧杯中装有适量的水)。小强同学设计的方法为:将最右侧导管放在盛水的烧杯中,打开止水夹a和c,关闭活塞b,向长颈漏斗中缓缓加入一定量的水,若 , 则装置不漏气。30. 植物的光合作用和呼吸作用强度可以用单位时间二氧化碳吸收量内呼吸或释放二氧化碳的量来表示。图甲曲线表示在恒温30℃时,某水藻在不同光照强度下,吸收二氧化碳与释放二氧化碳量的关系。小科为“研究光照强度对植物光合作用速度的影响”,设计如乙图实验装置。此装置的优点在于,可通过控制灯泡功率的大小或调节试管与灯泡的距离,来改变光照的强弱。 (1)、图甲中B点所代表的含义是 。(2)、图乙实验中,每隔5分钟改变一次试管与光源之间的距离,随着距离的增加,密闭的试管中产生气泡减少。造成这一结果的主要原因是:。(写一种即可)(3)、若该植物光合作用和呼吸作用的最适温度分别为25℃和30℃,在其他条件不变的情况下,将温度调节到25℃时,B点将向(选填“左”或“右”)移动。31. 半水煤气是工业合成氨的原料气,其主要成分可能是H2、CO、CO2、N2和水蒸气,某化学兴趣小组为检验半水煤气的某些成分,设计的实验方案如图所示。
(1)、图甲中B点所代表的含义是 。(2)、图乙实验中,每隔5分钟改变一次试管与光源之间的距离,随着距离的增加,密闭的试管中产生气泡减少。造成这一结果的主要原因是:。(写一种即可)(3)、若该植物光合作用和呼吸作用的最适温度分别为25℃和30℃,在其他条件不变的情况下,将温度调节到25℃时,B点将向(选填“左”或“右”)移动。31. 半水煤气是工业合成氨的原料气,其主要成分可能是H2、CO、CO2、N2和水蒸气,某化学兴趣小组为检验半水煤气的某些成分,设计的实验方案如图所示。

查阅资料可知碱石灰是CaO和NaOH的混合物。回答下列问题:
(1)、A瓶中产生白色沉淀,反应的化学方程式是 。(2)、B装置的作用是。(3)、实验过程中观察到A、E中澄清石灰水变浑浊,C中黑色固体变红色,可以得出结论:半水煤气中一定有。32. 小龙通过图示实验装置(夹持部分已略去)及药品,按如下实验步骤,验证了可燃物燃烧的条件。其中实验装置气密性良好,所用药品均足量(已知红磷的着火点为240℃,白磷的着火点为40℃)。

步骤一:向大烧杯中注入足量的冷水,打开K1关闭K2 , 向下压左侧注射器活塞,使生成的氧气持续通入U形管,并观察U形管中现象;
步骤二:关闭K1、打开K2 , 向下压右侧注射器活塞,使生成的二氧化碳将U形管内的氧气排尽,然后将烧杯中的冷水换成等量的80℃的热水,并观察U形管中现象;
步骤三……并观察U形管中现象。
(1)、根据图示信息,写出生成氧气的化学方程式。(2)、简述步骤二中判断U形管内氧气已经排尽的方法。。(3)、补充完整步骤三的操作,并写出U形管中应观察到的现象。。四、解答题
-
33. 某兴趣小组为测定某品牌钙片中碳酸钙含量,取某品牌钙片10克放入烧杯中,每次加入50克稀盐酸充分反应后并用电子天平称量,记录实验数据如下。(除碳酸钙外其他杂质不与盐酸反应)

加入稀盐酸次数
0
1
2
3
4
烧杯和所称物质总质量/克
150
198.9
247.8
297.8
m
(1)、表格中m的数值为。(2)、计算出该品牌钙片中CaCO3的质量分数(要有计算过程)。(3)、经过分析讨论,同学们觉得这样测得的结果有可能偏大,原因是(可多选)A.水会蒸发 B.盐酸会挥发 C.钙片没有充分研磨
34. 某科学兴趣小组对潜艇的制氧原理产生了好奇,通过查阅资料得知,潜艇中制取氧气的主要原料是固体过氧化钠(Na2O2),过氧化钠分别能和二氧化碳、水反应,都能生成氧气,反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2↑为测定潜艇中过氧化钠的质量分数,该小组的同学在教师的指导下,利用下图所示的装置(固定装置已略去)开展探究,并得出正确结论。
已知装置B中盛有饱和NaHCO3溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO组成的混合物。整套装置气密性良好,反应所需试剂均足量。

请回答下列问题:
(1)、装置B的作用是;(2)、在A中不用稀硫酸而用稀盐酸原因;(3)、装置E作用;(4)、装置D中过氧化钠样品的质量为m g,装置D在反应前后质量分别为n1g和n2g,若样品中所含杂质既不溶于水,也不参加化学反应,求样品中过氧化钠的质量分数?35. 清代医学著作《本草纲目拾遗》中“强水”的条目下写到“性最烈,能蚀五金”。“强水”中有硝酸,“五金”是指金、银、铜、铁、锡。其中铜和稀硝酸反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2X↑+4H2O(1)、X 的化学式为。(2)、19.2 克铜完全反应最多可生成Cu(NO3)2多少克?36. 当感染“非典”、新冠肺炎等疾病时,病人最后往往会因为肺部呼吸功能衰竭而危及生命。此时为挽救患者生命只能借助一种俗称“人工肺”的仪器帮助病人进行呼吸。人工肺的主体部分由中空纤维膜制成,可在病人自身肺功能出现衰竭时使用。下图为人工肺的工作原理示意图。请分析回答:
 (1)、人工肺替患者肺完成的生理功能是 。(2)、血液流经人工肺之后,血液中氧气含量变 , 二氧化碳含量变。(3)、与人工肺不同,正常人体肺富有弹性,当肋间内肌和膈肌 时,肺会收缩导致呼气;上图中阶段代表吸气过程中肺内气压变化。(4)、制造人工肺的膜材料要求较高,如所用膜材料应该只允许通过而不能让渗出,所以人工肺的研究与使用进展缓慢。(5)、使用人工肺时,需将患者静脉血引流至体外,经人工肺再回输至患者体内,目前仍面临许多风险。请写出一项使用人工肺时可能导致的风险。37. 在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多。经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)
(1)、人工肺替患者肺完成的生理功能是 。(2)、血液流经人工肺之后,血液中氧气含量变 , 二氧化碳含量变。(3)、与人工肺不同,正常人体肺富有弹性,当肋间内肌和膈肌 时,肺会收缩导致呼气;上图中阶段代表吸气过程中肺内气压变化。(4)、制造人工肺的膜材料要求较高,如所用膜材料应该只允许通过而不能让渗出,所以人工肺的研究与使用进展缓慢。(5)、使用人工肺时,需将患者静脉血引流至体外,经人工肺再回输至患者体内,目前仍面临许多风险。请写出一项使用人工肺时可能导致的风险。37. 在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多。经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)实验序号
温度(℃)
大理石颗粒
盐酸质量分数(%)
实验目的
1
20
粗
5
探究大理石和盐酸的反应速度与石灰石颗粒大小的关系
2
20
细
5
(1)、为了比较反应速度,设计如图一所示装置,其中量筒的作用是:; (2)、两次实验中产生CO2体积随时间的变化关系如图二所示,请结合所学的知识对两次实验的曲线作出合理的解释。(3)、已知20℃该气压下CO2气体密度约1.98 g/L,求大理石中CaCO3的质量(写出计算过程)
(2)、两次实验中产生CO2体积随时间的变化关系如图二所示,请结合所学的知识对两次实验的曲线作出合理的解释。(3)、已知20℃该气压下CO2气体密度约1.98 g/L,求大理石中CaCO3的质量(写出计算过程)