浙教版科学八下第二章 第7节 元素符号表示的量(中等难度)
试卷更新日期:2021-05-19 类型:同步测试
一、单选题
-
1. 维生素C(C6H8O6)主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力,近年来科学家还发现维生素C有防癌作用。下列关于维生素C的说法中错误的是 ( )A、维生素C中氢元素的质量分数约为4.5% B、维生素C由6个碳原子、8个氢原子、6个氧原子构成 C、维生素C中C,H,O三种元素的质量比为9:1:12 D、维生素C的相对分子质量为1762. 某元素R的化合价是奇数(不变化合价),已知其氧化物的相对分子质量为m,其氯化物的相对分子质量为n,则R的化合价为 ( )A、+ B、+ C、+ D、+3. 用以作为相对原子质量标准的碳-12可以写成C-12 。1个C-12的原子的质量为a千克,1个CO2分子的质量为b千克,若以CO2分子中的1个氧原子质量的`1/16作为相对原子质量的标准,则CO2的相对分子质量是( )A、 B、 C、 D、4. 某混合物中只含Na2SO4 、Na2S和Na2SO3 , 已知硫元素的质量分数为16%,则氧元素的质量分数为( )A、16% B、32% C、39% D、61%5. 目前发现“达菲”治疗H7N9病毒是有效的药物,但这个药物最好在36小时之内,不超过48小时之内用药有效,超过这个时间效果就要大打折扣。生产“达非”的主要原料是莽草酸(C7H10O5),下列关于莽草酸的说法正确的是( )A、莽草酸是由22个原子构成的化合物 B、莽草酸中氢元素的质量分数最高 C、莽草酸是由碳、氢、氧三种元素组成的 D、莽草酸的相对分子质量是174克6. 用以作为相对原子质量标准的碳C-12可以写成1个C-12, 1个C-12原子的质量为a千克,1个CO2分子的质量为b千克,若以CO2分子中的1个氧原子质量的1/16作为相对原子质量的标准,则CO2的相对分子质量是( )A、 B、 C、 D、7. 甲醛是室内装璜时产生的主要污染物之一,其化学式为CH2O,下列有关甲醛的说法正确的是( )A、甲醛由碳、氢气、氧构成 B、甲醛由一个碳原子、二个氢原子、一个氧原子构成 C、甲醛由碳、氢、氧三种元素组成 D、甲醛中C、H、O三种元素的质量比为1: 2: 18. 2020新春之际我国出现了罕见的新型冠状病毒疫情,过氧乙酸(CH3COOOH)是杀来病毒的主要消毒剂,下列关于过氧乙酸的说法中不正确的是( )A、过氧乙酸是一种化合物 B、过氧乙酸是由碳、氢、氧三种元素组成 C、过氧乙酸中碳、氢、氧元素的原子个数比为2:4:3 D、过氧乙酸的相对分子质量是76克9. 杭州市盛产茶叶,“西湖龙井”等绿茶享誉省内外。绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46 , 下列说法不正确的是( )A、单宁酸由碳、氢、氧三种元素组成 B、1个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 C、单宁酸分子中碳、氢、氧元素的个数比为38∶26∶23 D、1个单宁酸分子的相对分子质量为170010. 形成酸雨原因之一的氮氧化合物是氮、氧两种元素形成的多种化合物的总称,如NO2、N2O3、NO、N2O等,若将以上四种物质所含氮元素的质量分数绘制成统计图,则其中②表示的物质是( )
 A、NO2 B、N2O3 C、NO D、N2O11. 有一不纯的硫酸铵样品,经分析知道其中氮的质量分数为20%(杂质中不含氮),那么样品里(NH4)2SO4的质量分数为( )A、94.3% B、93.4% C、92.4% D、94.2%12. 经科学测定,某农场的果农原计划每亩施NH4HCO3肥料10kg,现改施NH4NO3肥料,若要达到相同的施肥效果,则每亩所需NH4NO3的质量为( )A、3.5kg B、5.1kg C、10kg D、10.2kg13. 根据物质相对分子质量和所含元素化合价有规律排列的一组化学式:CH4、X、H2O、HF,其中X应选择( )A、HCl B、NH3 C、PH3 D、H2S14. 人的尿液中含氮0.93%,如果这些氮只存在于尿素中,则人尿中含尿素[CO(NH2)2]的质量分数为( )A、0.20% B、1.00% C、1.99% D、0.02%15. 1854年法国化学家德维尔在实验室中意外地发现一种新元素。已知该元素的一个原子中含有40个微粒,其中14个微粒不带电,则该原子的相对原子质量是( )A、27 B、26 C、54 D、3416. 欲使 SO2 和 SO3 两种物质中所含氧元素的质量相等,则 SO2 和 SO3 的质量比为( )A、1∶1 B、2∶3 C、3∶2 D、6∶517. 宁波盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为 C19H19N7O6。下列有关叶酸的说法中正确的是( )A、叶酸的相对分子质量为 441g B、叶酸由 19 个碳原子、19 个氢原子、7 个氮原子和 6 个氧原子构成 C、叶酸中碳、氢、氮、氧四种元素质量比为 19∶19∶7∶6 D、叶酸中氮元素的质量分数大于氧元素的质量分数18. 由于铁丝在氧气中高温燃烧,故部分熔化的铁没有及时反应便融入到生成物中,得到的黑色固体为Fe3O4和Fe。若实验时,铁丝全部用完,测定瓶底黑色固体中氧元素质量分数为24%,则黑色固体中没有反应的Fe占黑色固体的质量分数约为( )A、17% B、63% C、21% D、13%19. 在19世纪,化学家对氧化锆的化学式有争议。经测定,锆(Zr)的相对原子质量为91,其氯化物的式量是233。若氧化锆中锆的化合价与氯化物中的相同,则氧化锆的化学式为( )A、ZrO2 B、Zr2O C、Zr2O3 D、ZrO20. 已知FeO、Fe2O3 和Fe3O4组成的混合物中,铁元素和氧元素的质量比为21∶8,则混合物中Fe2O3、FeO和Fe3O4三种物质的质量比可能是( )A、18∶20∶5 B、9∶20∶33 C、2∶3∶5 D、40∶18∶31
A、NO2 B、N2O3 C、NO D、N2O11. 有一不纯的硫酸铵样品,经分析知道其中氮的质量分数为20%(杂质中不含氮),那么样品里(NH4)2SO4的质量分数为( )A、94.3% B、93.4% C、92.4% D、94.2%12. 经科学测定,某农场的果农原计划每亩施NH4HCO3肥料10kg,现改施NH4NO3肥料,若要达到相同的施肥效果,则每亩所需NH4NO3的质量为( )A、3.5kg B、5.1kg C、10kg D、10.2kg13. 根据物质相对分子质量和所含元素化合价有规律排列的一组化学式:CH4、X、H2O、HF,其中X应选择( )A、HCl B、NH3 C、PH3 D、H2S14. 人的尿液中含氮0.93%,如果这些氮只存在于尿素中,则人尿中含尿素[CO(NH2)2]的质量分数为( )A、0.20% B、1.00% C、1.99% D、0.02%15. 1854年法国化学家德维尔在实验室中意外地发现一种新元素。已知该元素的一个原子中含有40个微粒,其中14个微粒不带电,则该原子的相对原子质量是( )A、27 B、26 C、54 D、3416. 欲使 SO2 和 SO3 两种物质中所含氧元素的质量相等,则 SO2 和 SO3 的质量比为( )A、1∶1 B、2∶3 C、3∶2 D、6∶517. 宁波盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为 C19H19N7O6。下列有关叶酸的说法中正确的是( )A、叶酸的相对分子质量为 441g B、叶酸由 19 个碳原子、19 个氢原子、7 个氮原子和 6 个氧原子构成 C、叶酸中碳、氢、氮、氧四种元素质量比为 19∶19∶7∶6 D、叶酸中氮元素的质量分数大于氧元素的质量分数18. 由于铁丝在氧气中高温燃烧,故部分熔化的铁没有及时反应便融入到生成物中,得到的黑色固体为Fe3O4和Fe。若实验时,铁丝全部用完,测定瓶底黑色固体中氧元素质量分数为24%,则黑色固体中没有反应的Fe占黑色固体的质量分数约为( )A、17% B、63% C、21% D、13%19. 在19世纪,化学家对氧化锆的化学式有争议。经测定,锆(Zr)的相对原子质量为91,其氯化物的式量是233。若氧化锆中锆的化合价与氯化物中的相同,则氧化锆的化学式为( )A、ZrO2 B、Zr2O C、Zr2O3 D、ZrO20. 已知FeO、Fe2O3 和Fe3O4组成的混合物中,铁元素和氧元素的质量比为21∶8,则混合物中Fe2O3、FeO和Fe3O4三种物质的质量比可能是( )A、18∶20∶5 B、9∶20∶33 C、2∶3∶5 D、40∶18∶31二、填空题
-
21.(1)、地壳中含量最多的金属元素与非金属元素形成的物质的化学式为;(2)、元素X的原子获得2个电子,元素Y的原子失去1个电子后,所形成离子的所带电子数均与氖原子相同,由X、Y两元素的离子形成的化合物(具体物质)的化学式为;(3)、相同质量的H2O2和H2O中氢元素的质量比为。(4)、某样品可能由氧化亚铁、氧化铁和四氧化三铁中的一种或几种组成,现测得该样品中铁元素与氧元素的质量比是21:8,则该样品的成分有种可能;若该样品由两种物质混合而成,则一定不含。22. 美国食品与药品管理局为美国吉利德科学公司的瑞德西韦开绿灯,批准该药物用于住院的新冠肺炎患者。瑞德西韦也成为美国首个获准用于新冠患者的药物。瑞德西韦的化学式为[C27H35N6O8P],请根据信息回答:(1)、瑞德西韦由种元素组成;一个瑞德西韦分子中共含有个原子;(2)、瑞德西韦中氢、氮元素质量比为;(3)、301g瑞德西韦中含有g碳元素。23. 使H2O2和H2O中含有相同质量的氧元素,则H2O2和H2O的质量比是;若使H2O2和H2O中含有相同质量的氢元素,则H2O2和H2O的分子个数比为。24. 等质量的H2、O2、N2所含分子数最多的是 , 各取它们的一个分子,则质量大小的排列顺序为 .25.(1)、人类探月的重要目的之一是勘察、获取地球上蕴藏量很小而月球上却极为丰富核聚变燃料−−“He−3”,解决地球能源危机。氦−3原子核里有两个质子,相对原子质量为3,其原子核内中子数为.(2)、某元素的阳离子X2+核外有28个电子,相对原子质量为65,则X原子核内质子数与中子数之差为.26. “烤羊肉串”是许多中小学生所喜爱的食品,但因食物长时间煎炸后所产生的微量的丙烯醛(化学式为C3H4O)是有毒物质,会损害人体健康,中国营养与食品研究所专家提醒广大消费者,远离烧烤,健康生活。丙烯醛中碳、氢、氧元素的质量比是 , 28克丙烯醛中含 克碳元素。27. 萤石是一些光学仪器中使用的镜片材料,萤石的主要成分是CaF2 , 试计算:(1)、CaF2的相对分子质量是。(2)、CaF2中钙元素和氟元素的质量比为。(3)、CaF2中氟元素的质量分数为(结果精确到0.1%)。28. 实验证明:同温同压下,相同体积的任何气体含有相同数目的分子。据此回答下列问题(以下气体均为同温同压下):(1)、将同体积的CO(煤气的主要成分)和C3H8(液化石油气的主要成分)混合,所得混合气体中CO和C3H8的分子个数比是 , 碳原子和氢原子的个数比是。(2)、液化石油气和煤气燃烧的主要反应是C3H8+5O2 3CO2+4H2O、2CO+O2 2CO2。煤气灶由灶体、进气管、进风管、电子开关等部件组成。目前管道煤气的用户迅速增加,重新购置的灶具跟石油液化气的灶具相比,在构造上的最大区别是进风管的粗细不同,重新购置的灶具的进风管应较 (选填“粗”或“细”)。29. 莽草酸是制取防治流感的特效药——达菲的基本原料,可以从常用的一种烹调香料——八角中提取,莽草酸的分子式为C7H10O5 , 则(1)、莽草酸(选填“是”或“不”)属于氧化物。(2)、莽草酸的相对分子质量是。(3)、莽草酸中碳、氢两元素的质量比为。30. m个N2O3分子和n个N2O5分子中所含氧元素的质量比是;若一个N2O3分子的质量为a千克,一个N2O5分子的质量为b千克,则一个氧原子的质量为千克;若以氧原子质量的1/16 作为标准,则N2O3的相对分子质量为。
三、解答题
-
31. 科学家经过多年研究证明,有一些同学爱吃的小包装零食中,含一定量的有毒、有害、致病的化学物质,如某些油炸食品中含有致癌物质丙烯酰胺(C3H5ON)。请你根据丙烯酰胺(C3H5ON)的化学式计算后填写:(1)、丙烯酰胺(C3H5ON)中碳、氢、氮元素的质量比是;(2)、氢元素的质量分数为。(3)、已知亚硝酸钠(NaNO2)也是一种有毒的致癌物质,请计算13.8g亚硝酸钠与多少克丙烯酰胺中含的氮元素质量相等(列式计算)(4)、一份不纯的丙烯酰胺(C3H5ON)样品含碳18%,请计算样品中丙烯酰胺(C3H5ON)的质量分数。(列式计算)32. 仅用5年时间,中国闪亮地跨入引领世界的高铁交通新时代。铺设无缝钢轨,需要用大量的钢铁,钢铁在生活中应用非常广泛。铁有多重氧化物,根据下列信息推断他们的化学式:(1)、某铁的氧化物中铁元素的化合价为+3价,则该铁的氧化物的化学式。(2)、某铁的氧化物化学式为FexOy,相对分子质量为72,则该铁的氧化物的化学方程式为。33. 钙是维持人体正常功能所必需的元素,人每天摄入的食物中含有钙元素,当摄入的钙不足时,需要服用补钙剂满足人体需求,下图分别为两种补钙剂说明书的一部分。
金钙尔奇
【主要原料】 碳酸钙、氧化镁、硫酸锌、
硫酸铜、维生素等
【含量】 每片含钙280 mg,镁99.7 mg,
锌3.08 mg,铜0.51 mg
【用量】 每日2次,一次1片
葡萄糖酸钙片
【主要原料】 葡萄糖酸钙(C12H22O14Ca)0.5 g
相对分子质量:430
【用法】 口服
【用量】 每日3次,一次?片
请回答下列问题。
(1)、按金钙尔奇说明书中的用量服用,每日补充钙元素的质量是mg。(2)、葡萄糖酸钙(C12H22O14Ca)中氢元素和钙元素的质量比为。(3)、葡萄糖酸钙(C12H22O14Ca)中各原子的个数比为 。(4)、张大爷每日需要的补钙量为418 mg,医生建议他服用葡萄糖酸钙片,一日3次,通过计算说明一次应服用几片?(写出计算过程)34. 玫瑰花中含有香茅醇、橙花醇和丁香油酚(C10H12O2)等物质。请计算下列问题。
(1)、丁香油酚的相对分子质量为。(2)、丁香油酚中碳、氢、氧三种元素的质量比为。(3)、丁香油酚中碳元素的质量分数为。(结果精确到0.1%)(4)、16.4 g丁香油酚中含g氧元素。(结果精确到0.1 g)35. 仙居杨梅享誉全国,春季需要给杨梅适当的补充氮肥,小柯和爸爸一起去买化肥。农资店里有多种氮肥,价格不一。最后,爸爸在硝酸铵[NH4NO3]和尿素[CO(NH2)2]两种氮肥之间纠结,这两种氮肥的每千克售价分别为4.0元和5.0元,不知道买哪一种更好。于是小柯就用自己所学的科学知识帮爸爸做了正确的选择。请问小柯选择了哪一种氮肥?他的依据是什么?请通过计算说明。四、实验探究题
-
36. 到19世纪末,经几代科学家对光合作用的不断探索,得到结论:光合作用的反应物是H2O和CO2 , 产物是O2和有机物。为了探究产物O2中的O元素的来源,科学兴趣小组从元素守恒的角度进行了如下猜想。
猜想一:O2中的O元素全部来源于CO2;
猜想二:O2中的O元素全部来自于H2O;
猜想三:O2中的O元素来源于CO2和H2O。
为了求证,他们查阅了以下资料:
资料一:范尼尔通过实验得出紫硫细菌合成有机物的反应式,与高等植物光合作用的
反应式进行比较研究后,建立了猜想。
紫硫细菌:CO2+2H2S (CH2O)(糖类)+2S+H2O
高等植物:CO2+2H2O (CH2O)(糖类)+O2+H2O
资料二:美国科学家鲁宾、卡门给三组小球藻提供含有一定比例180的水和碳酸氢盐(碳酸氢盐给小球藻的光合作用提供全部的CO2 , 而且不产生水,其他条件均相同),光照相同时间后,分别检测小球藻释放氧气中18O的比例,实验结果如表所示。(18O可作为示踪原子)
组别
水中18O的比例(%)
碳酸氢盐中18O的比例(%)
释放的氧气中18O的比例(%)|
1
0.85
0.41
0.84
2
0.85
0.55
0.85
3
0.85
0.61
0.85
资料三:
Ⅰ.16O表示中子数为 8的氧原子,18O是表示中子数为10的氧原子, 所以1个18O的质量是一个16O的质量9/8倍;自然界的氧气在标准状况下的密度为1.43千克/米3 , 其中16O占99.76% (可视为100%) ;
Ⅱ.在相同的温度和压强下,相同体积的气体具有相同的分子数。
Ⅲ.鲁宾和卡门通过测生成氧气的密度来确定氧气中18O含量。
(1)、资料一的实验结论支持猜想(选填 “一”、“二”或“三”)的观点:(2)、根据资料二鲁宾、卡门的实验结果,可得出的结论及相应的依据分别是。(3)、若有一瓶氧气,里面的氧原子全部由18O。结合资料,计算在标准状况下该瓶氧气的密度为千克/米3。37. 用含有二氧化碳和水蒸气杂质的某种还原性气体测定一种铁的氧化物(FexOy)的组成,实验装置如图所示。根据下图,试回答: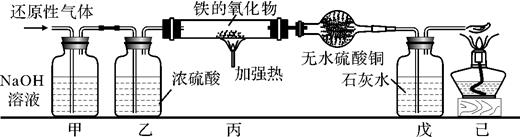 (1)、实验过程中丁装置白色粉末变蓝色,而戊装置中溶液没有明显变化,则该还原性气体是.(2)、当丙装置中的FexOy,全部被还原后,称量剩余固体的质量为11.2克,同时测得丁装置的质量增加了5.4克。则该铁的氧化物的化学式为。(3)、上述实验装置中,如果没有乙装置,将使测定结果中铁元素与氧元素的质量的比值。(填“偏大”、“偏小”或“无影响”)38. 小明为了测定铜和氧化铜混合物中氧化铜的质量分数,设计组装了如图的实验
(1)、实验过程中丁装置白色粉末变蓝色,而戊装置中溶液没有明显变化,则该还原性气体是.(2)、当丙装置中的FexOy,全部被还原后,称量剩余固体的质量为11.2克,同时测得丁装置的质量增加了5.4克。则该铁的氧化物的化学式为。(3)、上述实验装置中,如果没有乙装置,将使测定结果中铁元素与氧元素的质量的比值。(填“偏大”、“偏小”或“无影响”)38. 小明为了测定铜和氧化铜混合物中氧化铜的质量分数,设计组装了如图的实验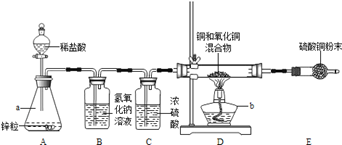 (1)、能除去H2中混有少量HCl气体的装置是(填装置序号)。(2)、装置E中硫酸铜粉末变蓝色,说明硬质试管中反应后有生成。(3)、实验前硬质试管中混合物的质量为5g,充分反应后剩余固体质量为4.2g,则混合物中氧化铜的质量分数为。39. PLA是一种新型可降解塑料,能有效缓解塑料垃圾造成的白色污染。已知PLA由碳、氢、氧三种元素组成,为了测定7.2gPLA样品中的各种元素质量比,某化学兴趣小组进行了以下探究。
(1)、能除去H2中混有少量HCl气体的装置是(填装置序号)。(2)、装置E中硫酸铜粉末变蓝色,说明硬质试管中反应后有生成。(3)、实验前硬质试管中混合物的质量为5g,充分反应后剩余固体质量为4.2g,则混合物中氧化铜的质量分数为。39. PLA是一种新型可降解塑料,能有效缓解塑料垃圾造成的白色污染。已知PLA由碳、氢、氧三种元素组成,为了测定7.2gPLA样品中的各种元素质量比,某化学兴趣小组进行了以下探究。【实验设计】
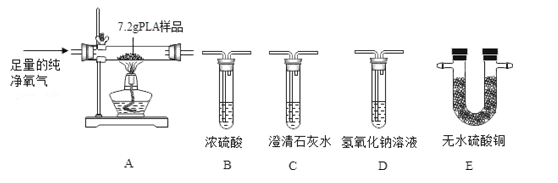
以上实验装置如图正确的连接顺序是:A→→E→→C。
①【分析与结论】实验中选择纯净的氧气而不用空气的原因是。
②装置 C 的作用是。
③正确连接装置后,确认气密性良好。充分燃烧7.2gPLA样品,已知燃烧产物被完全吸收,测得相关实验数据见下表:
装置
B
C
D
E
实验前质量/g
160
150
150
100
实验后质量/g
163.6
150
163.2
100
通过分析与计算,该 PLA 样品中碳、氢、氧三种元素质量比为。
40. 食醋是厨房中常用的调味品、它的主要成分是乙酸,乙酸分子的模型如图所示,其中“ ”代表一个碳原子,“
”代表一个碳原子,“  ”代表一个氢原子,“
”代表一个氢原子,“  ”代表一个氧原子,请计算:
”代表一个氧原子,请计算: 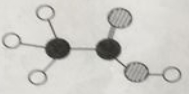 (1)、乙酸分子中的碳原子、氢原子、氧原子的个数比为。
(1)、乙酸分子中的碳原子、氢原子、氧原子的个数比为。
(2)、乙酸中碳元素的质量分数为。