冲刺2021高考化学押题训练(二)化学常用计算
试卷更新日期:2021-05-18 类型:三轮冲刺
一、单选题
-
1. NA为阿伏加德罗常数的值,下列说法正确的是( )A、1L1 molL CH3COOH溶液中含有NA个CH3COOH分子 B、标准状况下,11.2L 臭氧所含质子数为8NA C、0.2 mol NO与0.1 mol O2在密闭容器中充分反应后,容器中含有的氧原子数为0.4NA D、标准状况下,2.24 LCC4中含有的C-Cl 键数为0.4NA2. 设 为阿伏加德罗常数的值,下列说法中正确的是( )A、 正离子所含的电子总数为 B、 与 混合气体中所含原子总数为 C、常温常压下, 和 混合气体中含有 个氧原子 D、电解 溶液共得到 气体(标准状况),理论上转移了 个电子3. 设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )A、2H2S+SO2=3S↓+2H2O反应中,每生成1mol氧化产物时转移电子数为NA B、物质的量相等的重水与水相差2NA个中子 C、乙烯和丙烯组成的28g 混合气体中含氢原子数为4NA D、pH=13的1LBa(OH)2 溶液中所含有OH-数目为0.2NA4. NA为阿伏加德罗常数的值。下列说法正确的是( )A、9g18O2含有的中子数为4NA B、1mol氯气和水充分反应,转移的电子数为2NA C、25℃、101 kPa时,22.4L的N2和CO的混合气体中,原子数为NA D、1L1 mol•L-1 CH3COONa溶液中所含CH3COO-、CH3COOH的总数为NA5. 设NA为阿伏加德罗常数的值,下列叙述正确的是( )A、标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA B、常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA C、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA D、某密闭容器盛有0.1molN2和0.3molH2 , 在一定条件下充分反应,转移电子的数目为0.6NA6. 设NA为阿伏加德罗常数的值。下列说法正确的是( )A、0.1 mol•L-1NH4NO3溶液中含有的氮原子总数为0.2NA B、12g石墨和金刚石的混合物含有4NA个碳原子 C、1molCl2与足量铁充分反应,转移的电子数为2NA D、2.8gCO 和C2H4的混合气体中含有的质子数为1.4NA7. NA代表阿伏加德罗常数的值,下列说法正确的是( )A、10 g CaCO3和KHCO3的固体混合物所含阳离子大于0.1NA B、30 g二氧化硅中含有化学键的数目为NA C、1 mol Na被完全氧化生成Na2O,失去NA个电子 D、1 L 1 mol/LCH3COONa溶液中含有CH3COO-的数目为NA8. 设NA表示阿伏加德罗常数的值。下列叙述错误的是( )A、标准状况下,2.24LN2和O2的混合气体中,分子数目为0.1NA B、常温常压下,16gCH4含有的共价键数月为4NA C、Na2O与Na2O2的混合物共1mol,阴离子的数目为NA D、氨水溶液中NH 的物质的量为1×10-3mol,则该溶液中含有OH-的数目为1×10-3NA9. NA为阿伏加德罗常数的值。下列说法正确的是( )A、12 g NaHSO4晶体中阴离子所带电荷数为 0.2NA B、标准状况下,2.24 L CH3Cl中含有共价键的数目为0.4NA C、1L pH=13 的 Ba(OH)2溶液中 Ba2+数目为 0.1NA D、0.1mol FeI2与 0.1 mol Cl2 反应时转移电子的数目为0.3NA10. 设NA表示阿伏加德罗常数的值。下列叙述正确的是( )A、pH=1的H2SO4溶液,含H+的数目为NA B、78 g苯含有碳碳双键的数目为3NA C、11.2L(标准状况)正戊烷含有的分子数目为0.5NA D、1 mol CH3COONa溶于稀醋酸,溶液呈中性时含CH3COO-数目为NA11. 阿伏加德罗常数约为6.02×1023mol−1 , 下列叙述中正确的是( )A、常温常压下,18.0g重水(D2O)所含的电子数约为10×6.02×1023个 B、一定条件下,46.0g二氧化氮和四氧化二氮的混合气体中含有的氮原子数约为6.02×1023个 C、已知:CO(g)+2H2(g) CH3OH(g)ΔH=-91kJ·mol-1 , 一定条件下若加入6.02×1023个CO和2×6.02×1023个H2 , 则放出91kJ的热量 D、T℃时,1LpH=6纯水中,含10-8×6.02×1023个OH-12. 设 NA为阿伏加德罗常数的值,下列有关叙述正确的是( )A、常温下,78g Na2O2中含有离子数为 4NA B、0.5mol/L 的 AlCl3溶液中所含 Al3+的数目小于 0.5NA C、1mol Cl2与过量 H2O 反应,转移的电子数目为NA D、标准状况下,11.2L N2和 NO 混合气体中的原子数为NA13. 我国“金牌火箭”长征二号用 N2H4做燃料,发生反应:2N2H4+ 2NO2 3N2+4H2O。设 NA 为阿伏加德罗常数的值,下列有关说法正确的是( )A、标准状况下,22.4L H2O 中质子数目为 10 NA B、16g N2H4中含有极性共价键数目为 2.5 NA C、反应生成 1.5molN2时转移的电子数目为 4 NA D、密闭容器中 2molNO 和 1molO2充分反应生成 NO2 , 其分子数目为 2 NA14. 设 NA为阿伏加德罗常数的值。下列说法正确的是( )A、18g D2O 含有 10NA个质子 B、78g Na2O2中存在NA个共价键 C、1mol Cu 和足量热浓硫酸反应可生成 NA个 SO3分子 D、0.1mol FeCl3溶于 1L水中,所得溶液中含有0.1 NA个 Fe3+15. 设 为阿伏加德罗常数的数值。下列说法正确的是( )A、1 H2O2中含有共价键的数目为3 B、23gNa燃烧生成Na2O2失去的电子数为2 C、1L0.1 Na2SO3溶液中含有0.3 个氧原子 D、标准状况下,22.4LHCl溶于水后溶液中含有 个HCl分子16. 设 为阿伏加德罗常数的值。下列说法正确的是( )A、0.1mol苯中含有的碳碳双键数目为0.3 B、常温下, 含有的氧原子数为 C、 溶液中含有的 分子数为 D、标准状况下, 乙烯含有碳碳双键数为17. 设 NA为阿伏加德罗常数的值。下列说法正确的是( )A、标准状况下,22.4 LCH2Cl2 中含有的共用电子对数目为 4NA B、常温下将 5.6 g 的铁块投入到足量的浓硫酸中,转移的电子数为0.3NA C、含 28 g 硅的二氧化硅晶体中存在的共价键总数为 2NA D、AlCl3溶液中 Al3+的物质的量浓度为1mol·L-1 , 则1L溶液中所含 Cl-的数目大于3NA18. Al遇到极稀的硝酸发生反应生成NH4NO3 , 其反应为 。设NA为阿伏加德罗常数的值。下列说法正确的是( )A、将0.2mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中 的数目小于0.2NA B、1L0.1mol/L Al(NO3)3溶液中,阳离子的数目为0.1NA C、1.0g由H218O与D2O组成的混合物中所含有的中子总数为0.5NA D、反应中每消耗2.7g金属Al,转移的电子数为3NA19. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、25℃,pH=13的1.0LBa(OH)2溶液中含有OH-的数目为0.2NA B、60gSiO2晶体中Si—O键数目为2NA C、在K37ClO3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应中,若有212g氯气生成,则反应中转移电子的数目为5NA D、加热条件下,20mL10mol•L-1浓硝酸与足量铜反应转移电子数为0.1NA20. 设NA代表阿伏加德罗常数的数值,下列说法正确的是( )A、22.0 g T2O中含有的中子数为10NA B、一定条件下,6.4 g铜与过量的硫反应,转移电子数目为0.2NA C、在标准状况下,2.8g N2和2.24L CO所含电子数均为1.4NA D、标准状况下,22.4 L CH2Cl2中含C—H键数为2NA21. 设阿伏加德罗常数的值为NA , 下列说法不正确的是( )A、0.1molC6H14中含有的共用电子对数为1.9NA B、10g质量分数为46%的乙醇溶液中所含氧原子的总数为0.4NA C、标准状况下,2.24L己烷中含有的分子数为0.1 NA D、 1mol 苯乙烯(
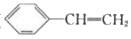 )中含有的碳碳双键数为NA
22. 用NA表示阿伏加德罗常数的值,下列叙述正确的是( )A、1 mol铁粉与1 mol氯气充分反应,转移电子数为3NA B、标准状况下,1.12 L HCHO所含的原子数是0.2NA C、1 L 0.5 mol·L-1 Na2CO3溶液中含有的CO32-数目为0.5NA D、16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA23. NA为阿伏加德罗常数,下列叙述正确的是( )A、18g水中含有的质子数为9NA B、0.1molNa+含有的电子数为NA C、常温常压下,71g氯气中含有的氯原子数为NA D、标准状况下,22.4LCCl4中含有的分子数为NA24. 下列说法错误的是( )A、常温常压下,3.2 g O2和O3的混合气体中含有氧原子的数目约为0.2×6.02×1023 B、1 L 0.5 mol·L−1 CH3COONa溶液中含有CH3COOH和CH3COO−的总数约为0.5×6.02×1023 C、标准状况下,1.12 L HCl气体中含有电子的数目约为0.9×6.02×1023 D、0.1mol环氧乙烷(
)中含有的碳碳双键数为NA
22. 用NA表示阿伏加德罗常数的值,下列叙述正确的是( )A、1 mol铁粉与1 mol氯气充分反应,转移电子数为3NA B、标准状况下,1.12 L HCHO所含的原子数是0.2NA C、1 L 0.5 mol·L-1 Na2CO3溶液中含有的CO32-数目为0.5NA D、16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA23. NA为阿伏加德罗常数,下列叙述正确的是( )A、18g水中含有的质子数为9NA B、0.1molNa+含有的电子数为NA C、常温常压下,71g氯气中含有的氯原子数为NA D、标准状况下,22.4LCCl4中含有的分子数为NA24. 下列说法错误的是( )A、常温常压下,3.2 g O2和O3的混合气体中含有氧原子的数目约为0.2×6.02×1023 B、1 L 0.5 mol·L−1 CH3COONa溶液中含有CH3COOH和CH3COO−的总数约为0.5×6.02×1023 C、标准状况下,1.12 L HCl气体中含有电子的数目约为0.9×6.02×1023 D、0.1mol环氧乙烷(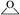 )中含有共价键的总数约为0.3×6.02×1023
25. 用NA代表阿伏加德罗常数的数值。下列说法正确的是( )A、7.8 g Na2O2中含有的离子数为0.3 NA B、1 mol NO2与水完全反应转移的电子数为NA C、标准状况下,22.4 L NH3含有的质子数为5NA D、1 L 0.1mol·L-1 NH4Cl溶液中含有的NH4+数为0.1NA26. 潜艇中氧气来源之一的反应是:2Na2O2+2H2O=4NaOH+O2↑。用NA表示阿伏加德罗常数,下列说法正确的是( )A、22.4LO2含2NA个O原子 B、1.8gH2O含有的质子数为NA C、1molNa2O2含共价键的总数为2NA D、上述反应,每生成1molO2转移4mol电子27. 设N为阿伏加德罗常数的值。下列说法正确的是( )A、密闭容器中 和 催化反应后原子总数小于 B、 的浓盐酸与足量 共热,电子转移的数目为 C、向 溶液中滴加氨水至溶液呈中性混合液中 的数目为 D、在标准状况下, 二氯乙烷( )中含有极性键的数目为28. 用NA表示阿伏加德罗常数的数值,下列说法中错误的是( )A、标准状况下,22.4LCl2通入足量NaOH溶液中,完全反应时转移的电子数为2NA B、20gD2O含有的电子数为10NA C、1L0.1mol•L-1NH4NO3溶液中的氮原子数为0.2NA D、25℃时,1.0LpH=12的NaClO溶液中由水电离出OH-的数目为0.01NA29. 设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )A、常温常压下,等物质的量浓度的Na2CO3与Na2S溶液中阳离子的数目相等 B、标准状况下,22.4LHF所含有的分子数目为NA C、常温常压下,NO2与N2O4的混合气体46g,原子总数为3NA D、0.1mol-NH2(氨基)中所含有的电子数为NA
)中含有共价键的总数约为0.3×6.02×1023
25. 用NA代表阿伏加德罗常数的数值。下列说法正确的是( )A、7.8 g Na2O2中含有的离子数为0.3 NA B、1 mol NO2与水完全反应转移的电子数为NA C、标准状况下,22.4 L NH3含有的质子数为5NA D、1 L 0.1mol·L-1 NH4Cl溶液中含有的NH4+数为0.1NA26. 潜艇中氧气来源之一的反应是:2Na2O2+2H2O=4NaOH+O2↑。用NA表示阿伏加德罗常数,下列说法正确的是( )A、22.4LO2含2NA个O原子 B、1.8gH2O含有的质子数为NA C、1molNa2O2含共价键的总数为2NA D、上述反应,每生成1molO2转移4mol电子27. 设N为阿伏加德罗常数的值。下列说法正确的是( )A、密闭容器中 和 催化反应后原子总数小于 B、 的浓盐酸与足量 共热,电子转移的数目为 C、向 溶液中滴加氨水至溶液呈中性混合液中 的数目为 D、在标准状况下, 二氯乙烷( )中含有极性键的数目为28. 用NA表示阿伏加德罗常数的数值,下列说法中错误的是( )A、标准状况下,22.4LCl2通入足量NaOH溶液中,完全反应时转移的电子数为2NA B、20gD2O含有的电子数为10NA C、1L0.1mol•L-1NH4NO3溶液中的氮原子数为0.2NA D、25℃时,1.0LpH=12的NaClO溶液中由水电离出OH-的数目为0.01NA29. 设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )A、常温常压下,等物质的量浓度的Na2CO3与Na2S溶液中阳离子的数目相等 B、标准状况下,22.4LHF所含有的分子数目为NA C、常温常压下,NO2与N2O4的混合气体46g,原子总数为3NA D、0.1mol-NH2(氨基)中所含有的电子数为NA二、综合题
-
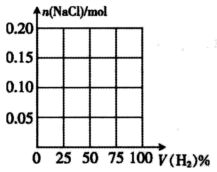
30. 某兴趣小组探究H2和Cl2反应后的气体与氢氧化钠溶液反应。在标准状况下,H2和Cl2的混合气体共2.24 L,光照充分反应后,用NaOH溶液充分吸收。(1)、消耗NaOH物质的量的最大值为mol。(2)、请在下图中画出NaCl的物质的量随H2的体积分数的变化图像。(横坐标表示原混合气体中H2的体积分数,纵坐标表示充分反应后NaCl的物质的量。)