贵州省毕节市威宁县2019-2020学年高一下学期化学期末考试试卷
试卷更新日期:2021-05-17 类型:期末考试
一、单选题
-
1. 某物质在组成元素上与其他三种不同,该物质是( )A、蔗糖 B、果糖 C、蛋白质 D、油脂2. 下列过程一定发生放热反应的是( )A、核能释放 B、浓硫酸遇水放热 C、生石灰投入冷水中 D、气球爆炸3. 从“绿色化学”和经济效益角度考虑,大量制取硝酸铜宜采用的方法是( )A、Cu与浓硝酸反应 B、Cu与稀硝酸反应 C、Cu先与空气反应制取氧化铜,再与稀硝酸反应 D、Cu与硝酸银溶液反应4. 下列说法正确的是( )A、石油常压蒸馏所得各种产品都为纯净物 B、石油裂化的主要目的是为了获得芳香烃 C、煤的干馏、液化或气化均为化学变化 D、乙酸、乙醇都可与Na反应生成氢气,均可电离出H+5. 下列有关能量变化的说法错误的是( )A、液氨作制冷剂是利用了氨挥发时会吸收周围环境的热量 B、旧化学键断裂后一定有新化学键的形成 C、中和反应是放热反应,水的分解一定是吸热反应 D、化学反应都伴随着能量的变化,多为热量的变化6. 已知 2H2S(g) + 3O2(g) 2SO2(g) + 2H2O(g),若反应速率分别用 v(H2S)、v(O2)、v(SO2)、v(H2O)表示,则正确的关系式为( )A、2v(H2S)=3v(O2) B、2v(O2)=3v(SO2) C、3v(O2)=2v(SO2) D、3v(O2)=2v(H2O)7. 下列关于糖类、油脂、蛋白质的说法中正确的是( )A、蛋白质、植物油、纤维素、淀粉都属于高分子化合物 B、牛油可以使溴的四氯化碳溶液褪色,也可以与氢气发生加成反应 C、油脂在酸性条件下水解与在碱性条件下水解产物完全相同 D、纤维素在人体消化过程中起着重要作用,但纤维素不能作为人类的营养物质8. 下列性质的比较或反应与S、Cl的非金属性强弱无关的是( )A、稳定性:H2S<HCl B、酸性:H2SO4<HClO4 C、水溶性:S<Cl2 D、Fe分别与S、Cl2反应生成FeS、FeCl39. 下列叙述中,错误的是( )A、在共价化合物分子内,一定不存在离子键 B、HBr、CO2、H2O、CS2都只含极性共价键 C、NH3分子中所有原子均满足8e-稳定结构 D、CaO和NaCl晶体熔化时要破坏离子键10. 下列说法正确的是( )A、元素周期表里金属元素和非金属元素分界线附近的元素可能用于制新农药 B、1H35Cl、2H37Cl两种气体的化学性质相同,但物理性质可能不同 C、氯化铵中无金属元素,故氯化铵属于共价化合物 D、Na2O2中既含离子键,又含非极性键,阴阳离子个数比1:111. 有关原电池的下列说法中正确的是( )A、2H2O 2H2↑+O2↑可设计成原电池 B、Al、Mg作原电池电极时,Al一定作正极 C、原电池工作时,阳离子向正极方向移动 D、原电池中氧化物不能作电极12. 下列叙述错误的是( )A、CH4与C4H10互为同系物 B、所有烷烃中均有碳碳单键 C、甲烷、苯、乙酸都不能与酸性高锰酸钾溶液反应 D、甲烷和乙烯都可以与氯气反应13. 下列有关卤素参与的变化中描述正确的是( )A、1mol甲烷与1mol氯气在光照下充分反应可生成1mol一氯甲烷 B、乙烯通入溴水中可得到1,1-二溴乙烷 C、四氯化碳可萃取出溴水中的溴单质 D、苯、铁屑和浓溴水混合反应可生成溴苯14. 有机物M的结构简式如图所示。下列有关M的叙述错误的是( )
 A、M的分子式为C10H18O3 B、M中含有两种官能团 C、可使酸性高锰酸钾溶液或溴水褪色 D、能发生加成反应、取代反应、氧化反应15. 反应CO(g)+H2O(g) CO2(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,不能够成立的是( )A、升高体系温度,v正、v逆一定同时增大 B、反应达平衡状态时:v(CO)正=v(H2O)逆 C、使用合适的催化剂也可加快反应速率 D、当n(CO)=n(CO2)时,反应必定处于平衡状态16. 下列说法中正确的是( )A、乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 B、油脂和氨基酸在一定条件下均可以与氢氧化钠溶液反应 C、CH3CH2CH2Cl与CH3CH2Br互为同系物 D、分子式为C4H8的烯烃有4种同分异构体(不考虑立体异构)17. 某小组为研究Fe、Cu与稀硫酸间的反应,设计如图装置。下列叙述正确的是( )
A、M的分子式为C10H18O3 B、M中含有两种官能团 C、可使酸性高锰酸钾溶液或溴水褪色 D、能发生加成反应、取代反应、氧化反应15. 反应CO(g)+H2O(g) CO2(g)+H2(g)在一定容积的密闭容器中进行,则下列说法或结论中,不能够成立的是( )A、升高体系温度,v正、v逆一定同时增大 B、反应达平衡状态时:v(CO)正=v(H2O)逆 C、使用合适的催化剂也可加快反应速率 D、当n(CO)=n(CO2)时,反应必定处于平衡状态16. 下列说法中正确的是( )A、乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 B、油脂和氨基酸在一定条件下均可以与氢氧化钠溶液反应 C、CH3CH2CH2Cl与CH3CH2Br互为同系物 D、分子式为C4H8的烯烃有4种同分异构体(不考虑立体异构)17. 某小组为研究Fe、Cu与稀硫酸间的反应,设计如图装置。下列叙述正确的是( ) A、a和b不连接时,铜片上发生还原反应 B、无论a和b是否连接,铁片均会溶解 C、a和b用导线连接时,电子按Fe→稀硫酸→Cu方向流动 D、a和b用导线连接时,铜片上会有气泡冒出,则铜可与稀硫酸反应18. 主链含5个碳原子,有一个乙基支链的一氯代烷有(不考虑立体异构)( )A、2种 B、3种 C、4种 D、5种19. 在一定温度下,容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示。下列表述错误的是( )
A、a和b不连接时,铜片上发生还原反应 B、无论a和b是否连接,铁片均会溶解 C、a和b用导线连接时,电子按Fe→稀硫酸→Cu方向流动 D、a和b用导线连接时,铜片上会有气泡冒出,则铜可与稀硫酸反应18. 主链含5个碳原子,有一个乙基支链的一氯代烷有(不考虑立体异构)( )A、2种 B、3种 C、4种 D、5种19. 在一定温度下,容器内某一反应中X、Y的物质的量随反应时间变化的曲线如图所示。下列表述错误的是( ) A、0~t1时间段内, (X): (Y)=2:1 B、该反应属于可逆反应 C、t1时正反应速率大于逆反应速率 D、反应达到平衡时,X、Y的物质的量肯定相等20. 位于前三周期的四种主族元素W、X、Y、Z的原子序数依次增大、且总和为25。由这四种元素组成的某化合物的结构如图所示。下列有关叙述错误的是( )
A、0~t1时间段内, (X): (Y)=2:1 B、该反应属于可逆反应 C、t1时正反应速率大于逆反应速率 D、反应达到平衡时,X、Y的物质的量肯定相等20. 位于前三周期的四种主族元素W、X、Y、Z的原子序数依次增大、且总和为25。由这四种元素组成的某化合物的结构如图所示。下列有关叙述错误的是( ) A、该化合物中,W、X、Y之间均为共价键 B、Z的单质与水反应不如与乙醇反应剧烈 C、常温下,Y的最高价氧化物对应的水化物可溶解铜 D、X的氟化物XF4中原子均为8电子稳定结构
A、该化合物中,W、X、Y之间均为共价键 B、Z的单质与水反应不如与乙醇反应剧烈 C、常温下,Y的最高价氧化物对应的水化物可溶解铜 D、X的氟化物XF4中原子均为8电子稳定结构二、综合题
-
21. 人类的生产、生活离不开化学。(1)、铝粉与某些金属氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如:2Al+Fe2O3 2Fe+Al2O3 , 反应发生时放出大量的热。
①“铝热反应”属于四种基本反应类型中的反应。
②信息中的“某些”指(填“比铝活泼”“比铝不活泼”或“任意”)。
③试写出铝粉与MnO2发生的铝热反应方程式:。
(2)、从海水中提取溴的工业流程如图:
①步骤I中发生反应的离子方程式为。
②步骤II用热空气吹出的Br2被纯碱溶液吸收时,则被氧化和被还原的Br2的物质的量之比为。
(3)、海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:
①若操作I用H2O2溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程为。
②操作II的名称为、 , 此过程中可以选用的有机溶剂是(填一种)。
22. 已知:A是最简单的烯烃,D为一日常调味品的有效成分。如图是有机物A~G之间的转化关系。
请回答下列问题:
(1)、E的官能团名称为 , F的名称为。(2)、G属于高分子化合物,其结构简式为。(3)、写出对应③的化学方程式: , 反应类型为。(4)、写出反应④的化学方程式: , 反应类型为。(5)、试剂X可能为(填试剂名称)。(6)、如图,在试管a中先加入3mL95%的物质B,边摇动边缓缓加入2mL浓H2SO4并充分摇匀,冷却后再加入2mL纯净物质D,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
①加入浓H2SO4的作用是催化剂、。
②实验中球形干燥管除起冷凝作用外,另一个重要作用是。
23. A、B、C、D、E五种短周期元素,原子序数依次增大,A、E同主族。A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:(1)、元素C和D的原子半径大小关系为(填元素符号和“>”),元素D和E的简单离子半径大小关系为(填具体离子符号和“>”)。(2)、试写出E2D2的电子式为。(3)、将E的单质投入水中,发生反应的离子方程式为 , 该反应的氧化产物与还原产物的物质的量之比为。(4)、实验室用固体混合物加热法制取C元素的简单气态氢化物的化学方程式为 , 两种固体反应物中都含有的化学键为(填“离子键”“共价键”或“离子键和共价键”)。(5)、化合物C2A4可被H2O2氧化,产物为N2和液态水、则反应的化学方程式为。24.(1)、如图甲所示,在锥形瓶里放置装有水的小试管。往小试管中分别加入下列物质时:①烧碱固体,②浓硫酸,③硝酸铵固体,④NaCl固体。其中能使a溶液面高于b溶液面的是(填序号)。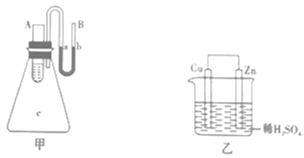 (2)、如图乙是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,记录如下:
(2)、如图乙是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,记录如下:①Zn为正极,Cu为负极;
②H+向负极移动;
③电子的流动方向,从Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生H2为0.5mol;
⑥正极的电极反应式为Zn-2e-=Zn2+。
以上描述合理的是(填序号)。
(3)、试解决下列有关化学反应速率的问题。①若图乙的烧杯中最初装入的是500mL2mol·L-1的稀硫酸,当原电池工作2min时共收集到11.2L氢气(标准状况),则这2min内H2SO4的反应速率v(H2SO4)=。2min末,烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=、c(ZnSO4)=。
②若要使反应Zn+H2SO4=ZnSO4+H2↑的速率加快,下列措施可行的是(填序号)。
a.改锌片为锌粉
b.改稀H2SO4为98%的浓硫酸
c.升高温度
d.滴加少量CuSO4溶液