上海市长宁区2021年中考化学二模试卷
试卷更新日期:2021-05-17 类型:中考模拟
一、单选题
-
1. 上海市为确保在 2025 年前实现“碳达峰”(二氧化碳排放不再增长),相关做法错误的是( )A、培育氢燃料电池汽车产业 B、使用乙醇汽油 C、发展风力发电 D、发展光伏发电2. 元素符号书写正确的是( )A、氮 N B、氮 Ne C、氖 N D、氖NE3. “含氟牙膏”中“氟”指的是( )A、原子 B、分子 C、元素 D、单质4. 笑气的化学式为N2O,它属于( )A、单质 B、氧化物 C、碱 D、盐5. N2O 中氮元素的化合价是( )A、+1 B、+2 C、+3 D、+46. N2O 的性质中属于化学性质的是( )A、无色有甜味的气体 B、微溶于水 C、相同条件下,密度与二氧化碳接近 D、在一定条件下能支持燃烧7. 属于同素异形体的是( )A、石墨和 C60 B、银粉和水银 C、铂金和黄金 D、火碱和烧碱8. 取少量食盐进行焰色反应,火焰的颜色为( )A、蓝色 B、紫色 C、黄色 D、红色9. 具有还原性的气体是( )A、氧气 B、氦气 C、一氧化碳 D、二氧化碳10. 探究氢氧化钠溶液性质的实验中,有明显现象的是( )A、向大理石中滴加氢氧化钠溶液 B、向氢氧化钠溶液通入少量二氧化碳 C、向硝酸钾溶液中滴加氢氧化钠溶液 D、向硫酸铁溶液中滴加氢氧化钠溶液11. 取少量酸雨,12 小时内每隔一小时测一次该酸雨的 pH,发现数值不断变小,说明该酸雨酸性( )A、不断减弱 B、不断增强 C、变为中性 D、变为碱性12. 柠檬酸晶体的水溶液呈酸性,关于柠檬酸晶体的说法正确的是( )A、柠檬酸晶体是混合物 B、柠檬酸晶体能与镁带反应 C、柠檬酸晶体能与石灰水反应 D、柠檬酸晶体能使 pH 试纸变色13. 无法证明镁的金属活泼性强于铜的实验事实是( )A、镁带能溶于稀盐酸,铜片不能 B、镁带能与氯化铜溶液反应 C、铜片不能与氯化镁溶液反应 D、取等质量的镁带和铜片,加入硝酸银溶液中,一段时间后,镁带置换出的银更多14. 关闭启普发生器的活塞后,能表示装置内大理石上方压强变化的图像是( )A、
 B、
B、 C、
C、 D、
D、 15. 一定属于置换反应的是( )A、将长铁丝伸入氯化银中 B、将长铁丝伸入硫酸铜溶液中 C、一种单质和一种化合物的反应 D、生成一种单质和一种化合物的反应
15. 一定属于置换反应的是( )A、将长铁丝伸入氯化银中 B、将长铁丝伸入硫酸铜溶液中 C、一种单质和一种化合物的反应 D、生成一种单质和一种化合物的反应二、多选题
-
16. 在 100mL 烧杯中加入 20g0.4%的氢氧化钠溶液,滴加 2~3 滴酚酞试液,再逐滴滴加 0.365%的稀盐酸, 关于反应过程中的说法正确的是( )A、溶液由无色变为红色 B、溶液可能不变色 C、产生大量热,烧杯变烫,形成大量水雾 D、当溶液为无色时,溶质的质量分数为 0.3%17. 20℃时,向一定量水中分批加入KNO3 固体,充分搅拌并冷却至室温,现象如图所示:

坐标图中,符合实验结果的描点可能是( )
A、 B、
B、 C、
C、 D、
D、
三、填空题
-
18. 尿素是一种优良的化肥。
①尿素的化学式为 ,它属于化肥中的(选填“氮肥”、“磷肥”或“钾肥”)同时它还属于(选填“有机物”或“无机物”)。它的摩尔质量为 , 1mol 中约含有个碳原子,含有g 氮元素。
②1828 年维特首次使用无机物氰酸铵与 人工合成了 , 是由铵根和组成的,无机物氰酸铵中氰酸根一定含有元素。
四、简答题
-
19. 表为不同温度下KNO3 的溶解度。
温度(℃)
0
10
20
30
40
50
KNO3的溶解度(g/100g 水)
13.3
20.9
31.6
45.8
63.9
85.5
(1)、由上表可知:20℃时,KNO3的溶解度是g/100g 水,KNO3的溶解度随温度升高而(选填“升高”、“下降”或“几乎不变”)。(2)、①配置一定温度下KNO3 的饱和溶液,进行如下实验操作:I分别取 20.0gKNO3 固体和 10.0mL 蒸馏水,放入烧杯中,充分搅拌,并冷却至室温。
II观察固体是否完全溶解,若还有固体剩余,可进行操作去除不溶物,并称量剩余溶液的质量;若没有固体剩余,直接称量溶液的质量。
②III为了使固体完全溶解,依次将操作 I 中蒸馏水的体积由 10mL 改为 20.0mL、30.0mL、40.0mL……,重复上述操作 I、II,直至固体完全溶解。记录实验数据,绘制图。

A点对应的溶液中KNO3的质量为g,此时 KNO3的溶解度为g/100g 水,此时温度的范围是(选填字母)。
a.0~10℃ b.10~20℃ c.20~30℃ d.30~40℃
③A、B、C、D、E五点对应的溶液中,属于不饱和溶液的是(选填字母)。
五、实验题
-
20. 氢气是一种还原性气体。
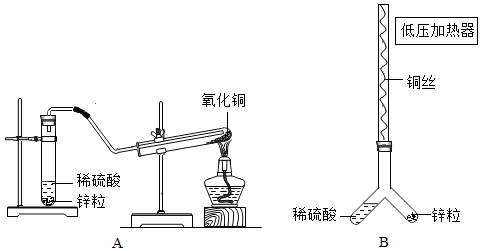
①装置A 开始反应,锌粒表面的现象为 , 该反应的化学方程式为。充分反应后,可以观察到氧化铜表面的现象为 , 说明氢气具有还原性,该反应的化学方程式为。
②装置 B 的实验操作顺序如下:
I.制氧化铜:打开低压加热器,加热铜丝,发现铜丝表面变黑后停止加热,此时铜丝表面反应的化学方程式为。
II.制氢气:必须待铜丝冷却至室温,才能倾斜装置使稀硫酸流入锌粒,开始反应,理由是。
III.反应:应先对产生的气体进行操作后,再打开低压加热器,加热铜丝,直至铜丝表面黑色物质消失后停止加热,取出铜丝,停止反应。
③请选择一套合适的装置 , 并从实验装置和药品的角度阐述你的理由。
六、综合应用题
-
21. 胆矾的化学式为CuSO
4·5H2O,它是一种结晶水合物。①取少量胆矾于蒸发皿中,用酒精灯充分加热,现象为。
求 0.02mol 胆矾完全反应后,蒸发皿中剩余的固体的质量(请根据化学方程式列式计算)。
②测量 t℃时,饱和硫酸铜溶液的质量分数,进行如下实验操作: I 称量空蒸发皿的质量(m1g)。
II取一定量饱和硫酸铜溶液于蒸发皿中,称量饱和硫酸铜溶液与蒸发皿的质量(m2g)。
III用酒精灯充分加热,直至蒸发皿中固体完全变白。
IV待蒸发皿冷却至室温后,称量剩余固体与蒸发皿的质量(m3g)。实验结果及 CuSO4 的溶解度如表:
t
m1
m2
m3
实验数据
18℃
36.7g
97.1g
47.1g
温度(℃)
10
20
CuSO4 的溶解度(g/100g 水)
17.4
20.7
上述实验方案与结果是否合理,若合理,请计算该饱和硫酸铜溶液的质量分数;若不合理,请阐述你的理由。
-
-
-