河北省承德市2021年中考化学一模试卷
试卷更新日期:2021-05-17 类型:中考模拟
一、单选题
-
1. 下列金属制品中,利用金属导电性的是( )A、黄金首饰
 B、铝蒸锅
B、铝蒸锅  C、铜导线
C、铜导线  D、金属乐器
D、金属乐器  2. 下列物质不属于合金的是( )A、青铜 B、铝 C、不锈钢 D、生铁3. 把少量下列物质放入水中,充分搅拌,能形成溶液的是( )A、汽油 B、蔗糖 C、冰块 D、泥土4. 下图所示实验操作正确的是( )A、测定溶液的pH
2. 下列物质不属于合金的是( )A、青铜 B、铝 C、不锈钢 D、生铁3. 把少量下列物质放入水中,充分搅拌,能形成溶液的是( )A、汽油 B、蔗糖 C、冰块 D、泥土4. 下图所示实验操作正确的是( )A、测定溶液的pH B、称量固体氢氧化钠
B、称量固体氢氧化钠  C、稀释浓硫酸
C、稀释浓硫酸  D、移取灼热的蒸发皿
D、移取灼热的蒸发皿  5. 下列物质的俗名与化学式相对应正确的是( )A、生石灰Ca(OH)2 B、熟石灰CaO C、食盐NaOH D、纯碱Na2CO36. 航母“山东舰”作为首艘国产航母,其制造过程中使用了大量的金属材料,下列关于金属材料的说法中正确的是( )A、金属铝的化学性质比铁活泼,因此也更容易锈蚀 B、钢的含碳量比生铁高,所以应用更广泛 C、“真金不怕火炼”说明黄金的熔点非常高 D、金属资源的回收利用既保护了环境,又节约了金属资源7. 下列物质加入水中,所得溶液pH可能为10的是( )A、熟石灰 B、白醋 C、橘子汁 D、食盐8. 下列物质露置于空气中,质量会减小的是( )A、浓硫酸 B、浓盐酸 C、氢氧化钠 D、氯化钠9. 下列事实不能证明甲的金属活动性比乙强的是( )A、自然界中甲元素只以化合物形式存在,乙元素有单质形式存在 B、甲能与盐酸反应而乙不能 C、甲能从乙的盐溶液中置换出乙 D、化合物中甲元素显+2价而乙元素显+3价10. 科学使用化肥是农业增产的重要手段。下列化肥属于复合肥的是( )A、尿素CO(NH2)2 B、硝酸铵NH4NO3 C、硫酸钾K2SO4 D、硝酸钾KNO311. 生活中一些常见物质的近似pH如下,其中碱性最强的是( )A、肥皂9.5~10.5 B、厕所清洁剂1.2~2.0 C、炉具清洁剂12.0~13.0 D、牙膏8.2~8.912. 下列关于溶液的说法正确的是( )A、溶液一定是混合物 B、饱和溶液的浓度一定比不饱和溶液的浓度大 C、医用碘酒是碘的水溶液 D、凡是均一的、稳定的液体一定是溶液13. 中和反应在生活中有广泛应用。下列应用不属于中和反应的是( )A、土壤酸化后加入熟石灰改良 B、用氢氧化钠溶液洗涤石油产品中的残余硫酸 C、服用含氢氧化镁的药物治疗胃酸过多 D、金属表面锈蚀后,可用稀盐酸进行清洗14. 下列物质所对应的用途错误的是( )A、氧化钙:干燥剂 B、氢氧化钠:治疗胃酸过多 C、碳酸氢钠:焙制糕点 D、氯化钠:医疗上配制生理盐水15. 将一根洁净的铜丝放入AgNO3溶液中,一段时间后,溶液从无色变为蓝色,铜丝表面生长出如图所示的白色“树枝”,下列叙述错误的是( )
5. 下列物质的俗名与化学式相对应正确的是( )A、生石灰Ca(OH)2 B、熟石灰CaO C、食盐NaOH D、纯碱Na2CO36. 航母“山东舰”作为首艘国产航母,其制造过程中使用了大量的金属材料,下列关于金属材料的说法中正确的是( )A、金属铝的化学性质比铁活泼,因此也更容易锈蚀 B、钢的含碳量比生铁高,所以应用更广泛 C、“真金不怕火炼”说明黄金的熔点非常高 D、金属资源的回收利用既保护了环境,又节约了金属资源7. 下列物质加入水中,所得溶液pH可能为10的是( )A、熟石灰 B、白醋 C、橘子汁 D、食盐8. 下列物质露置于空气中,质量会减小的是( )A、浓硫酸 B、浓盐酸 C、氢氧化钠 D、氯化钠9. 下列事实不能证明甲的金属活动性比乙强的是( )A、自然界中甲元素只以化合物形式存在,乙元素有单质形式存在 B、甲能与盐酸反应而乙不能 C、甲能从乙的盐溶液中置换出乙 D、化合物中甲元素显+2价而乙元素显+3价10. 科学使用化肥是农业增产的重要手段。下列化肥属于复合肥的是( )A、尿素CO(NH2)2 B、硝酸铵NH4NO3 C、硫酸钾K2SO4 D、硝酸钾KNO311. 生活中一些常见物质的近似pH如下,其中碱性最强的是( )A、肥皂9.5~10.5 B、厕所清洁剂1.2~2.0 C、炉具清洁剂12.0~13.0 D、牙膏8.2~8.912. 下列关于溶液的说法正确的是( )A、溶液一定是混合物 B、饱和溶液的浓度一定比不饱和溶液的浓度大 C、医用碘酒是碘的水溶液 D、凡是均一的、稳定的液体一定是溶液13. 中和反应在生活中有广泛应用。下列应用不属于中和反应的是( )A、土壤酸化后加入熟石灰改良 B、用氢氧化钠溶液洗涤石油产品中的残余硫酸 C、服用含氢氧化镁的药物治疗胃酸过多 D、金属表面锈蚀后,可用稀盐酸进行清洗14. 下列物质所对应的用途错误的是( )A、氧化钙:干燥剂 B、氢氧化钠:治疗胃酸过多 C、碳酸氢钠:焙制糕点 D、氯化钠:医疗上配制生理盐水15. 将一根洁净的铜丝放入AgNO3溶液中,一段时间后,溶液从无色变为蓝色,铜丝表面生长出如图所示的白色“树枝”,下列叙述错误的是( ) A、白色“树枝”的主要成分是银 B、溶液变为蓝色,表明Cu转变为Cu2+ C、该反应为置换反应 D、银的金属活动性比铜的强16. 下列物质不能用来鉴别氢氧化钠溶液和稀盐酸的是( )A、CO2 B、碳酸钠溶液 C、铁粉 D、紫色石蕊试液17. 如图是氢氧化钠和稀盐酸反应的微观示意图,以下有关说法错误的是( )
A、白色“树枝”的主要成分是银 B、溶液变为蓝色,表明Cu转变为Cu2+ C、该反应为置换反应 D、银的金属活动性比铜的强16. 下列物质不能用来鉴别氢氧化钠溶液和稀盐酸的是( )A、CO2 B、碳酸钠溶液 C、铁粉 D、紫色石蕊试液17. 如图是氢氧化钠和稀盐酸反应的微观示意图,以下有关说法错误的是( ) A、该反应属于复分解反应 B、该反应的微观实质是H+和OH-结合生成H2O C、反应前后数量没有变化的粒子是Na+、Cl-和H2O D、该反应符合质量守恒定律18. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、酸能使紫色石蕊溶液变红,向紫色石蕊溶液中通入CO2后变红,则CO2是酸 B、碱性溶液的pH大于7,若测得某溶液的pH=9,则该溶液一定是某种碱的溶液 C、浓硫酸具有吸水性,所以,浓硫酸可以作某些气体的干燥剂 D、溶液中有晶体析出时,溶质的质量分数一定减小19. 利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )
A、该反应属于复分解反应 B、该反应的微观实质是H+和OH-结合生成H2O C、反应前后数量没有变化的粒子是Na+、Cl-和H2O D、该反应符合质量守恒定律18. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、酸能使紫色石蕊溶液变红,向紫色石蕊溶液中通入CO2后变红,则CO2是酸 B、碱性溶液的pH大于7,若测得某溶液的pH=9,则该溶液一定是某种碱的溶液 C、浓硫酸具有吸水性,所以,浓硫酸可以作某些气体的干燥剂 D、溶液中有晶体析出时,溶质的质量分数一定减小19. 利用如图所示实验装置模拟工业炼铁。下列说法正确的是( )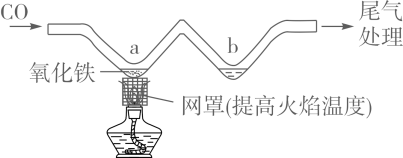 A、实验时应先点燃酒精灯后通CO B、充分加热,a处固体由黑色变为红色 C、b处可用澄清石灰水检验生成的CO2 D、可用NaOH溶液吸收尾气中的CO20. 如图所示实验,要使装置中的小气球鼓起来,则使用的固体和液体不可能是( )
A、实验时应先点燃酒精灯后通CO B、充分加热,a处固体由黑色变为红色 C、b处可用澄清石灰水检验生成的CO2 D、可用NaOH溶液吸收尾气中的CO20. 如图所示实验,要使装置中的小气球鼓起来,则使用的固体和液体不可能是( ) A、锌和稀硫酸 B、石灰石和稀盐酸 C、固体氢氧化钠和水 D、硝酸铵和水
A、锌和稀硫酸 B、石灰石和稀盐酸 C、固体氢氧化钠和水 D、硝酸铵和水二、填空题
-
21. 如图是A、B、C三种物质的溶解度曲线图,请回答下列问题:
 (1)、P点的意义是。(2)、t3℃时,A,B,C三种物质溶解度最大的是。(3)、将某温度下C的不饱和溶液变成饱和溶液的方法是。(写出一种方法即可)(4)、A固体中含有少量的物质B,可用方法提纯物质A(A与B溶于水时不发生化学反应)。(5)、在t3℃时,将A、B、C的等质量饱和溶液分别降温到t1℃,析出晶体最多的是 , 所得溶液中溶质的质量分数由大到小的顺序是。22. 实验是化学研究的重要手段。请分析下列实验回答相关问题:
(1)、P点的意义是。(2)、t3℃时,A,B,C三种物质溶解度最大的是。(3)、将某温度下C的不饱和溶液变成饱和溶液的方法是。(写出一种方法即可)(4)、A固体中含有少量的物质B,可用方法提纯物质A(A与B溶于水时不发生化学反应)。(5)、在t3℃时,将A、B、C的等质量饱和溶液分别降温到t1℃,析出晶体最多的是 , 所得溶液中溶质的质量分数由大到小的顺序是。22. 实验是化学研究的重要手段。请分析下列实验回答相关问题: (1)、图甲实验中能证明铁钉生锈需要水的实验组合是(填字母编号)。实验①中植物油的作用是。为了防止铁制品生锈,可以采取的合理措施是(写出一种措施即可)。(2)、图乙实验为了证明锌、铁、铜的金属活动性顺序,其中实验没有必要进行。写出实验⑥中发生反应的化学方程式。(3)、图丙为粗盐提纯实验中的两步操作,如果做完实验⑦后,滤液仍然浑浊,原因可能是;在实验⑧中,当观察到时,再停止加热。23. 配制一定溶质质量分数的氯化钠溶液的过程如下图所示:
(1)、图甲实验中能证明铁钉生锈需要水的实验组合是(填字母编号)。实验①中植物油的作用是。为了防止铁制品生锈,可以采取的合理措施是(写出一种措施即可)。(2)、图乙实验为了证明锌、铁、铜的金属活动性顺序,其中实验没有必要进行。写出实验⑥中发生反应的化学方程式。(3)、图丙为粗盐提纯实验中的两步操作,如果做完实验⑦后,滤液仍然浑浊,原因可能是;在实验⑧中,当观察到时,再停止加热。23. 配制一定溶质质量分数的氯化钠溶液的过程如下图所示: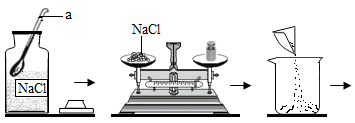
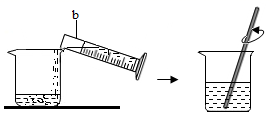 (1)、写出图中有标号的仪器名称:a , b。(2)、欲配制50g质量分数为15%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠g,水g。(3)、称量氯化钠时,氯化钠应放在托盘天平的盘(填“左”或“右”)。量取所需水的体积时应选用的量筒规格为(填写“50mL”或“100mL”)。(4)、溶解过程中玻璃棒的作用是。(5)、对所配制的溶液进行检测发现溶质质量分数偏小,其原因可能是(写出一种可能的原因)。24. 利用以下装置对酸的化学性质进行研究。
(1)、写出图中有标号的仪器名称:a , b。(2)、欲配制50g质量分数为15%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠g,水g。(3)、称量氯化钠时,氯化钠应放在托盘天平的盘(填“左”或“右”)。量取所需水的体积时应选用的量筒规格为(填写“50mL”或“100mL”)。(4)、溶解过程中玻璃棒的作用是。(5)、对所配制的溶液进行检测发现溶质质量分数偏小,其原因可能是(写出一种可能的原因)。24. 利用以下装置对酸的化学性质进行研究。 (1)、实验Ⅰ中,在点滴板的a、b穴中滴入酸溶液后,溶液变红的是(填“a”或“b”)。使用点滴板的优点之一是。(2)、实验Ⅱ中,为了验证石灰石中含有碳酸根离子,试剂X的名称是。(3)、实验Ⅲ中,在仪器①、②中均可观察到的现象是、。写出仪器①中发生反应的化学方程式。(4)、稀盐酸和稀硫酸具有相似的化学性质,主要原因是。
(1)、实验Ⅰ中,在点滴板的a、b穴中滴入酸溶液后,溶液变红的是(填“a”或“b”)。使用点滴板的优点之一是。(2)、实验Ⅱ中,为了验证石灰石中含有碳酸根离子,试剂X的名称是。(3)、实验Ⅲ中,在仪器①、②中均可观察到的现象是、。写出仪器①中发生反应的化学方程式。(4)、稀盐酸和稀硫酸具有相似的化学性质,主要原因是。三、流程题
-
25. 已知A、B、C、D、E分别为初中化学常见的物质,其主要成分分别为金属单质、氧化物、酸、碱、盐中的一种。A是赤铁矿的主要成分,D为蓝色溶液,E俗称烧碱。它们的部分反应和转化关系如图所示。(“-”表示两种物质能发生反应,“→”表示一种物质能转化成另一种物质,且省略部分反应物或生成物及反应条件)。
 (1)、写出下列物质的化学式:A、E。(2)、C物质的类别是(填:酸、碱、盐或氧化物)。(3)、写出A→B的化学反应方程式。(4)、写出物质D与E反应的的化学方程式 , 该反应的基本反应类型是。
(1)、写出下列物质的化学式:A、E。(2)、C物质的类别是(填:酸、碱、盐或氧化物)。(3)、写出A→B的化学反应方程式。(4)、写出物质D与E反应的的化学方程式 , 该反应的基本反应类型是。四、实验题
-
26. 为了探究碱的化学性质,同学们进行了如图所示的实验。
 (1)、(实验操作)
(1)、(实验操作)夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中、锥形瓶中发生反应的化学方程式为。
(2)、反应一段时间后(氢氧化钠过量,CO2完全反应),打开弹簧夹,观察到的现象为 , 锥形瓶底部有白色沉淀生成。此时锥形瓶中发生的反应的化学方程式为。(3)、(废液处理)将反应后锥形瓶内的物质全部倒入烧杯B中,然后滴入几滴无色酚酞溶液,充分混合后,烧杯内的液体为色。
(4)、再向烧杯中加入一定量的稀盐酸,充分反应后,烧杯内得到无色澄清溶液,则该无色溶液中一定含有的溶质是、。请写出该烧杯内发生中和反应的化学方程式(写一个)。(5)、最后烧杯内的无色溶液能否直接排放,请阐述你的观点并说明理由。(6)、(反思交流)碱溶液易与空气中的二氧化碳发生反应,所以碱溶液应该保存。
五、计算题
-
27. 实验室有一瓶放置多年的浓盐酸(如图所示),为了测定它实际的溶质质量分数,实验员将20g40%的氢氧化钠溶液放于烧杯中,利用pH测定仪逐滴滴入该盐酸,并绘制出了所加盐酸的质量与烧杯中溶液pH的关系图。
 (1)、两者恰好完全反应时,消耗盐酸的质量为g。(2)、请你计算该浓盐酸的实际质量分数。
(1)、两者恰好完全反应时,消耗盐酸的质量为g。(2)、请你计算该浓盐酸的实际质量分数。
-
-