上海市浦东新区2020-2021学年九年级下学期化学期中考试试卷
试卷更新日期:2021-05-08 类型:期中考试
一、选择题(20分)【1~14题只有1个正确答案】
-
1. 属于化学变化的是( )A、缝制衣服 B、切割石块 C、狩猎捕鱼 D、钻木取火2. 碳元素仅以游离态形式存在的物质是( )A、大理石 B、干冰 C、金刚石 D、碳酸3. 属于氮肥的是( )A、K2CO3 B、Na2SO4 C、NH4HCO3 D、Ca(H2PO4)24. 下列符号中只表示微观意义的是( )A、H2 B、Fe C、CO D、3H2O5. 属于碱的是( )A、醋酸 B、熟石灰 C、纯碱 D、生石灰6. 物质的用途错误的是( )A、氢气冶炼金属 B、氧气用作燃料 C、稀硫酸除铁锈 D、熟石灰中和土壤酸性7. 下列物质的化学式书写正确的是( )A、氯化铵一NH3Cl B、氧化铁—FeO C、甲烷一CH4 D、纯碱一NaOH8. 关于水的净化过程描述错误的是( )A、加入明矾使小颗粒凝聚 B、通入氯气杀菌消毒 C、通过沙滤装置除去可溶性杂质 D、通过活性炭吸附部分有害物质9. 镁在二氧化碳中燃烧的化学方程式是: ,其中氧化剂是( )A、Mg B、CO2 C、MgO D、C10. 甲烷和水反应可以制备水煤气(混和气体),其反应的微观示意图如下所示:
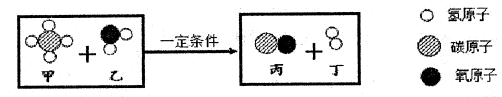
根据以上微观示意图得出的结论中,正确的是( )
A、该反应是置换反应 B、反应中氢元素由化合态变为游离态 C、反应前后,分子、原子种类均不变 D、反应中丙、丁的分子个数比为1:111. 运用图示法可以帮助我们巧学化学.下列化学知识用相应图示表示正确的是( )
A、 B、
B、 C、
C、 D、
D、 12. 各组物质能在pH=1.5的溶液中大量共存,且形成无色溶液的是( )A、NaCl BaCl2 Na2SO4 B、Na2SO4 HCl KCl C、CuSO4 NaCl NaNO3 D、Na2CO3 NaCl Na2SO413. 实验现象或实验原理正确的是( )A、白磷始终不燃烧
12. 各组物质能在pH=1.5的溶液中大量共存,且形成无色溶液的是( )A、NaCl BaCl2 Na2SO4 B、Na2SO4 HCl KCl C、CuSO4 NaCl NaNO3 D、Na2CO3 NaCl Na2SO413. 实验现象或实验原理正确的是( )A、白磷始终不燃烧 B、小气球变瘪
B、小气球变瘪  C、U型管内液面左低右高
C、U型管内液面左低右高  D、验证Fe、Cu、Ag的金属活动性强弱
D、验证Fe、Cu、Ag的金属活动性强弱  14. 3.2克某物质X在氧气中完全燃烧生成0.1mol二氧化碳和0.2mol水,该物质可能是( )A、CH3OH B、C2H6O C、CH4 D、C2H415. 下列基本不含有机物的是( )A、牛奶 B、矿泉水 C、啤酒 D、鲜榨果汁16. 能将氢氧化钠、氯化钠、硫酸三种溶液鉴别出来的试剂是( )A、石蕊试剂 B、氯化钡溶液 C、硝酸银溶液 D、酚酞试液17. 向含有少量硝酸银的废液中加入一定量的铁屑,充分反应后过滤。有关滤渣和滤液成分判断,不可能出现的组合是( )
14. 3.2克某物质X在氧气中完全燃烧生成0.1mol二氧化碳和0.2mol水,该物质可能是( )A、CH3OH B、C2H6O C、CH4 D、C2H415. 下列基本不含有机物的是( )A、牛奶 B、矿泉水 C、啤酒 D、鲜榨果汁16. 能将氢氧化钠、氯化钠、硫酸三种溶液鉴别出来的试剂是( )A、石蕊试剂 B、氯化钡溶液 C、硝酸银溶液 D、酚酞试液17. 向含有少量硝酸银的废液中加入一定量的铁屑,充分反应后过滤。有关滤渣和滤液成分判断,不可能出现的组合是( ) 选项成分
选项成分A
B
C
D
滤渣
Fe
Fe、Ag
Ag
Ag、Fe
滤液
Fe(NO3)2
Fe(NO3)2
AgNO3、Fe(NO3)2
AgNO3、Fe(NO3)2
A、A B、B C、C D、D二、简答题(30分)
-
18. 水是生命之源,水是发展之本。
①电解水可证明水由氢、氧两种元素组成,该反应的化学方程式为。
②高铁酸钾(化学式K2FeO4)目前被广泛应用于自来水净化处理领域。高铁酸钾中铁元素的化合价为 , 该物质中铁元素处于(填“游离态”或“化合态”)。
③水是重要的溶剂。配制6%的氯化钠溶液50g,不需要用到的仪器是。
A.酒精灯 B.玻璃棒 C.烧杯 D.量筒
④水在化学实验中的作用不可忽视。下列实验中水起吸收热量作用的是。

⑤“84消毒液”主要成分是次氯酸钠( NaClO),制取的化学方程式为:
,则X的化学式。次氯酸钠(NaClO)的摩尔质量为 , 1.5 mol NaClO中约含氯原子个,其中氧元素的质量是g。
19. 根据表中NaCl和KNO3溶解度数据,回答下列问题。温度/℃
0
20
40
60
80
100
NaCl溶解度(g/100g水)
35.7
36.0
36.6
37.3
38.4
39.8
KNO3溶解度(g/100g水)
13.3
31.6
63.9
110
169
246
①40℃时,NaCl的溶解度是。
②20℃时,将等质量KNO3和NaCl固体,分别加入到盛有100g的烧杯中,充分搅拌后现象如图1,加热到60℃时现象如图2(不考虑水分蒸发)。

根据图1和图2现象判断:甲烧杯中的固体是;将图2中的两溶液降温至40℃时,对两种溶液的分析正确的是。
A.甲一定是饱和溶液 B.两溶液中溶质质量分数一定相等
C.甲一定会析出晶体 D.甲溶液浓度一定大于乙溶液浓度
③如果60℃时KNO3饱和溶液中混有少量NaCl时提纯KNO3可采用方法。
④将等质量KNO3的饱和溶液和NaCl的饱和溶液从60℃降温到20℃后,所得溶液中溶质质量分数大的
是溶液。
20. 某含铁和炭的黑色粉末,为测定其中铁粉的质量分数,进行以下实验:称量10.0g样品放入50.0g的锥形瓶中,再加入过量稀硫酸100g(如图一)立即开始记录读数(如图二),回答下列问题:
①图一中a的仪器名称是。取该样品需要使用的仪器是。
②写出锥形瓶中发生反应的化学方程式。反应生成氢气的物质的量是mol。
③样品中铁粉的质量分数是。(根据化学方程式进行列式计算)
④根据锥形瓶中的反应绘制的图像正确的是。
 21. 小明发现生物老师将一勺白色粉末加入鱼缸后,水中有气泡产生,奄奄一息的鱼很快就活蹦乱跳,于是对这种“白色粉末”产生兴趣,与小刚一起进行了相关探究。(1)、实验准备
21. 小明发现生物老师将一勺白色粉末加入鱼缸后,水中有气泡产生,奄奄一息的鱼很快就活蹦乱跳,于是对这种“白色粉末”产生兴趣,与小刚一起进行了相关探究。(1)、实验准备①查阅资料:白色粉末的主要成分是过碳酸钠(Na2CO4),常温下与水反应生成氧气。
②用一定溶质质量分数的NaOH和Na2CO3两种溶液进行如下实验。
NaOH溶液
Na2CO3溶液
滴加酚酞溶液
溶液变红色
溶液变红色
加入稀盐酸
无明显现象
现象Ⅰ
加入澄清石灰水
无明显现象
现象Ⅱ
加入1%的CaCl2溶液
溶液变浑浊
溶液变浑浊
加入0.1%的CaCl2溶液
无明显现象
溶液变浑浊
表中的现象Ⅰ为 , 现象Ⅱ对应的化学反应方程式为。
(2)、实验过程实验1:检验气体
小明用白色粉末和水反应制取并收集产生的气体时,应选用的装置是(填序号)。
经检验该气体是氧气,该装置中检验氧气是否已经收集满的方法及现象为。
 (3)、实验2:检验反应后溶液中的溶质成分
(3)、实验2:检验反应后溶液中的溶质成分【猜想假设】小明猜想:Na2CO3;小刚猜想:Na2CO3和NaOH
【进行实验】小明取实验1反应后的溶液于试管中,滴加1%的CaCl2溶液,观察到有白色沉淀生成,认为自己的猜想正确。
【表达交流】
①小刚对小明的实验方案提出质疑,他的理由是。
②为了证明小明的猜想是否正确,你的实验方案是。(请写出实验步骤、现象及结论)
(4)、反思拓展根据上述探究可知,保存该白色粉末时应注意。