高中化学人教版(2019)必修第二册 第六章第一节 化学反应与能量变化
试卷更新日期:2021-04-26 类型:同步测试
一、单选题
-
1. 开发和使用新型能源,有利于节约资源、保护环境。下列能量转化过程中,会大量排放温室气体的是( )A、太阳能发电 B、燃煤发电 C、水力发电 D、氢氧燃料电池放电2. 下列属于吸热的氧化还原反应的是( )A、Zn与稀盐酸反应制备氢气 B、铵盐和碱反应生成氨气 C、碳与二氧化碳高温反应生成一氧化碳 D、铝热反应3. 下列说法正确的是( )A、铅蓄电池放电时,正极与负极质量均增加 B、手机、电脑中使用的锂电池属于一次电池 C、二次电池充电时,正极与外接电源的负极相连 D、燃料电池工作时,燃料在电池中燃烧,热能转化为电能4. 下列生活中的常见电池,属于一次电池的是( )A、普通锌锰干电池 B、镍氢电池 C、手机锂电池 D、铅蓄电池5. 2019年诺贝尔化学奖授予三位对锂电池研究作出杰出贡献的科学家。一种锂-空气电池如图所示。当电池工作时, 与 在多孔碳材料电极处生成 ( 或1)。下列说法正确的是( )
 A、锂电极发生氧化反应 B、多孔碳材料电极为负极 C、电池工作时外电路电子由多孔碳材料电极流向锂电极 D、正极的电极反应式为:6. 如图所示,电流计G发生偏转,同时A极逐渐变细,B极逐渐变粗,C为电解质溶液,则A、B、C应是下列各组中的( )
A、锂电极发生氧化反应 B、多孔碳材料电极为负极 C、电池工作时外电路电子由多孔碳材料电极流向锂电极 D、正极的电极反应式为:6. 如图所示,电流计G发生偏转,同时A极逐渐变细,B极逐渐变粗,C为电解质溶液,则A、B、C应是下列各组中的( ) A、A是Zn、B是Cu、C为稀硫酸 B、A是Cu、B是Zn、C为稀硫酸 C、A是Fe、B是Ag、C为AgNO3溶液 D、A是Ag、B是Fe、C为AgNO3溶液7. 下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中错误的是( )A、石墨比金刚石稳定
A、A是Zn、B是Cu、C为稀硫酸 B、A是Cu、B是Zn、C为稀硫酸 C、A是Fe、B是Ag、C为AgNO3溶液 D、A是Ag、B是Fe、C为AgNO3溶液7. 下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中错误的是( )A、石墨比金刚石稳定 B、白磷转变为红磷是放热反应
B、白磷转变为红磷是放热反应 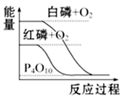 C、S(g)+O2(g)=SO2(g)△H1 , S(s)+O2(g)=SO2(g)△H2 , 则△H1>△H2
C、S(g)+O2(g)=SO2(g)△H1 , S(s)+O2(g)=SO2(g)△H2 , 则△H1>△H2 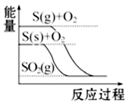 D、CO(g)+H2O(g)=CO2(g)+H2(g)△H<0
D、CO(g)+H2O(g)=CO2(g)+H2(g)△H<0 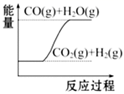 8. 某反应由两步反应 构成,它的反应能量曲线如图 、 、 、 表示活化能 。下列有关叙述正确的是
8. 某反应由两步反应 构成,它的反应能量曲线如图 、 、 、 表示活化能 。下列有关叙述正确的是 A、相同条件下 反应的速率小于 的速率 B、两步反应均为吸热反应 C、A,B,C中物质B最稳定 D、整个反应的9. 下列说法正确的是( )A、吸热反应一定需要加热才能进行 B、已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定 C、已知2CO2(g)=2CO(g)+O2(g) △H=+566 kJ/mol则CO的燃烧热△H=-283.0 kJ/mol D、已知C(s)+O2(g)=CO2(g) △H0;C(s)+ O2(g)=CO(g) △H2 , 则△H1>△H210. 如图所示是一位同学在测试水果电池,下列有关说法错误的是( )
A、相同条件下 反应的速率小于 的速率 B、两步反应均为吸热反应 C、A,B,C中物质B最稳定 D、整个反应的9. 下列说法正确的是( )A、吸热反应一定需要加热才能进行 B、已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定 C、已知2CO2(g)=2CO(g)+O2(g) △H=+566 kJ/mol则CO的燃烧热△H=-283.0 kJ/mol D、已知C(s)+O2(g)=CO2(g) △H0;C(s)+ O2(g)=CO(g) △H2 , 则△H1>△H210. 如图所示是一位同学在测试水果电池,下列有关说法错误的是( ) A、若金属片A是正极,则该金属片上会产生H2 B、水果电池的化学能转化为电能 C、此水果发电的原理是电磁感应 D、金属片A、B可以一个是铜片,另一个是铁片
A、若金属片A是正极,则该金属片上会产生H2 B、水果电池的化学能转化为电能 C、此水果发电的原理是电磁感应 D、金属片A、B可以一个是铜片,另一个是铁片二、填空题
-
11. 在银锌原电池中,以硫酸铜为电解质溶液:
锌为极,电极上发生的是反应(“氧化”或“还原”)电极反应式为;银电极电极反应式是;银片上观察到的现象是。
 12. 甲烷燃料电池是常见的燃料电池之一,该电池在正极通入氧气,在负极通入甲烷,电解质溶液通常是KOH溶液,请写出该电池的负极反应式。以该燃料电池为电源,用石墨电极电解一定物质的量浓度的CuSO4溶液,写出其阴极电极反应方程式;阳极电极反应方程式。通电一段时间后,溶液颜色变浅,需要加入一定量的使其恢复原来的浓度。当某一石墨电极的质量增加0.64g,则装置中消耗的甲烷的体积为(标准状况)。
12. 甲烷燃料电池是常见的燃料电池之一,该电池在正极通入氧气,在负极通入甲烷,电解质溶液通常是KOH溶液,请写出该电池的负极反应式。以该燃料电池为电源,用石墨电极电解一定物质的量浓度的CuSO4溶液,写出其阴极电极反应方程式;阳极电极反应方程式。通电一段时间后,溶液颜色变浅,需要加入一定量的使其恢复原来的浓度。当某一石墨电极的质量增加0.64g,则装置中消耗的甲烷的体积为(标准状况)。三、综合题
-
13. 依据氧化还原反应Zn(s)+Cu2+(aq)=Zn2+(aq)+Cu(s)设计的原电池如下图所示。

请回答下列问题:
(1)、电极X的材料是;电解质溶液Y是。(2)、铜电极为电池的极,发生的电极反应为 X极上发生的电极反应为。(3)、外电路中的电子是从极流向极(填名称)。(4)、盐桥中的Cl-向极移动,如将盐桥撤掉,电流计的指针将偏转。14.(1)、某甲醇 空气燃料电池的工作原理如图1所示 ( 箭头丧示物质的进入或排出 ) :
①甲电极为该燃料电池的 选填“正极”或“负极” ,该电极的电极反应方程式为 。
②用该电池作供电电源,用情性电极电解足量的 溶液,若阴极增重 ,则理论上消耗甲醇 g。
(2)、尿素树脂生产过程中所排放的废水中往在含有甲醇,这种含甲醇的废水会对环境造成污染。向该废水中加入一定量的酸性 溶液,然后采用图2所示装贸进行电解即可除去甲醇,除甲醇的原理:电解产物 将废水中的甲醇氧化为 。①阳极反应式为 。
②请用离子方程式表示该法除甲醇的原理为 。
③排放该电解后的废水的铁质管道易被腐蚀,除与 发生置换反应外,还发生电化学腐蚀,发生还原反应的电极反应式为 。