辽宁省辽阳市2019-2020学年高二下学期化学期末考试试卷
试卷更新日期:2021-04-25 类型:期末考试
一、单选题
-
1. “有机”一词译自“Organic”,词源解释为“属于、关于或者源自生物的”。下列关于有机化学的说法错误的是( )A、3D打印技术用于有机合成,可以促进工艺的精准化和简易化 B、1828年,维勒用氰酸铵合成了尿素,实现了实验室中无机物到有机物的转化 C、宣德青花瓷所用青料“苏麻离青”属于低锰高铁类钴料,是纯天然有机材料 D、我国非遗中以板蓝根、蓝靛等为染料的扎染工艺是经验性利用有机化合物的典范2. 下列烷烃的系统命名正确的是( )A、1-甲基丁烷 B、2,3-甲基丁烷 C、3-甲基丁烷 D、3-乙基戊烷3. 下列有机物的分类错误的是( )
选项
物质
类别
A
CH2=CH2
烯烃
B
CH3OH
醇
C
CH3COCH3
醛
D
CH3COOH
羧酸
A、A B、B C、C D、D4. 下列物质中一定互为同系物的是( )A、C2H4与C3H6 B、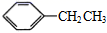 与
与  C、CH3CH2OH与CH3CH2OCH3
D、HCHO与CH3(CH2)4CHO
5. 科学研究表明,医用酒精可以有效杀灭新型冠状病毒,下列说法错误的是( )A、医用酒精中乙醇的体积分数为75% B、乙醇可以使人体产生新型冠状病毒抗体 C、乙醇与水能以任意比例互溶 D、乙醇可以使酸性高锰酸钾溶液褪色6. 下列说法错误的是( )A、每一个能层中电子的填充顺序都为ns→np→nd→nf B、用n表示电子层数,则每个电子层最多可容纳的电子数为2n2 C、元素周期表中,p区所含元素种类最多 D、电子的运动状态可从电子层、能级、原子轨道、电子的自旋状态四个方面进行描述7. 为检验氯代烃分子中的氯原子,进行了下列实验,该实验中操作步骤的排列顺序正确的是( )
C、CH3CH2OH与CH3CH2OCH3
D、HCHO与CH3(CH2)4CHO
5. 科学研究表明,医用酒精可以有效杀灭新型冠状病毒,下列说法错误的是( )A、医用酒精中乙醇的体积分数为75% B、乙醇可以使人体产生新型冠状病毒抗体 C、乙醇与水能以任意比例互溶 D、乙醇可以使酸性高锰酸钾溶液褪色6. 下列说法错误的是( )A、每一个能层中电子的填充顺序都为ns→np→nd→nf B、用n表示电子层数,则每个电子层最多可容纳的电子数为2n2 C、元素周期表中,p区所含元素种类最多 D、电子的运动状态可从电子层、能级、原子轨道、电子的自旋状态四个方面进行描述7. 为检验氯代烃分子中的氯原子,进行了下列实验,该实验中操作步骤的排列顺序正确的是( )①取少量氯代烃②加热③加入新制AgNO3溶液④加入几滴桸HNO3⑤加入氢氧化钠溶液⑥加入氢氧化钠的乙醇溶液
A、①②⑤⑥④③ B、①⑤④②③⑥ C、①②③④⑤ D、①⑤②④③8. 羧酸和醇发生酯化反应的过程如下图所示:
可见酯化反应不是简单的取代反应,步骤①和②的有机反应类型为( )
A、①为加成反应,②为消去反应 B、①为氧化反应,②为还原反应 C、①为取代反应,②为消去反应 D、①为加成反应,②为氧化反应9. 利用下列实验不能达到实验目的的是( )


 A、装置甲:制备溴苯 B、装置乙:实验室制备乙烯 C、装置丙:实验室制备硝基苯 D、装置丁:证明碳酸的酸性强于苯酚10. 已知短周期元素的离子aA2+、bB+、cC3-、dD-具有相同的电子层结构。则下列叙述正确的是( )A、金属性:A>B;非金属性:C>D B、元素的第一电离能:D>C>A>B C、C、D的最高价氧化物对应的水化物均为强酸 D、原子序数:d>c>b>a11. 下列反应方程式书写正确的是( )A、用对苯二甲酸与乙二醇合成涤纶,n
A、装置甲:制备溴苯 B、装置乙:实验室制备乙烯 C、装置丙:实验室制备硝基苯 D、装置丁:证明碳酸的酸性强于苯酚10. 已知短周期元素的离子aA2+、bB+、cC3-、dD-具有相同的电子层结构。则下列叙述正确的是( )A、金属性:A>B;非金属性:C>D B、元素的第一电离能:D>C>A>B C、C、D的最高价氧化物对应的水化物均为强酸 D、原子序数:d>c>b>a11. 下列反应方程式书写正确的是( )A、用对苯二甲酸与乙二醇合成涤纶,n +n
+n 
 +2nH2O
B、由丙烯合成聚丙烯:nCH2=CHCH3
+2nH2O
B、由丙烯合成聚丙烯:nCH2=CHCH3  C、实验室用液溴和苯在催化剂作用下制溴苯:2
C、实验室用液溴和苯在催化剂作用下制溴苯:2  +Br2 2
+Br2 2  D、用银氨溶液检验乙醛中的醛基:CH3CHO+2 +2OH- CH3COO-+ +3NH3+2Ag↓+H2O
12. 下列不能形成配位键的组合的是( )A、Cu2+、NH3 B、BF3、NH3 C、CH4、Ag+ D、Co3+、CO13. W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其高最价含氧酸反应生成离子化合物。由此可知,下列说法错误的是( )
D、用银氨溶液检验乙醛中的醛基:CH3CHO+2 +2OH- CH3COO-+ +3NH3+2Ag↓+H2O
12. 下列不能形成配位键的组合的是( )A、Cu2+、NH3 B、BF3、NH3 C、CH4、Ag+ D、Co3+、CO13. W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其高最价含氧酸反应生成离子化合物。由此可知,下列说法错误的是( ) A、W、X、Y、Z的最简单氢化物中X的氢化物沸点最高 B、含Z的化合物都不能被人直接饮用 C、W、X、Z形成的常见单质中,W的单质最稳定 D、X与Y、Z均能形成具有漂白性的物质,但漂白原理不同14. 光气(COCl2)是一种很重要的有机中间体。下列关于光气分子的几何构型和中心原子(C)的杂化方式说法正确的是( )A、平面三角形、sp2 B、V形、sp3 C、三角锥形、sp3 D、三角锥形、sp215. 某有机物的结构简式如图所示,下列关于该有机物的性质说法正确的是( )
A、W、X、Y、Z的最简单氢化物中X的氢化物沸点最高 B、含Z的化合物都不能被人直接饮用 C、W、X、Z形成的常见单质中,W的单质最稳定 D、X与Y、Z均能形成具有漂白性的物质,但漂白原理不同14. 光气(COCl2)是一种很重要的有机中间体。下列关于光气分子的几何构型和中心原子(C)的杂化方式说法正确的是( )A、平面三角形、sp2 B、V形、sp3 C、三角锥形、sp3 D、三角锥形、sp215. 某有机物的结构简式如图所示,下列关于该有机物的性质说法正确的是( ) A、可与银氨溶液反应,不与FeCl3溶液发生显色反应 B、可与H2反应,1mol该物质最多消耗6molH2 C、1mol该物质与NaHCO3溶液反应,最多消耗1molNaHCO3 D、1mol该物质与NaOH溶液反应,最多消耗3molNaOH16. 下列实验操作能达到实验目的的是( )
A、可与银氨溶液反应,不与FeCl3溶液发生显色反应 B、可与H2反应,1mol该物质最多消耗6molH2 C、1mol该物质与NaHCO3溶液反应,最多消耗1molNaHCO3 D、1mol该物质与NaOH溶液反应,最多消耗3molNaOH16. 下列实验操作能达到实验目的的是( )选项
实验操作
实验目的
A
向盛有2mL10%硫酸铜溶液的试管中滴加0.5mL 10%氢氧化钠溶液,混合均匀,滴入待检液,加热
检验某溶液中是否含有醛基
B
向混有少量乙酸的乙酸乙酯中加入足量饱和Na2CO3溶液,振荡、静置、分液,取出上层液体
除去乙酸乙酯中混有的少量乙酸
C
向高锰酸钾溶液中通入含乙烯的SO2
检验乙烯并除去乙烯
D
将氯乙烷与氢氧化钠溶液共热一段间时.再向冷却后的混合溶液中滴加硝酸银溶液
检验水解产物中的氯离子
A、A B、B C、C D、D17. 具有芳香气味的有机物A可发生下列变化,则A的可能结构有( ) A、2种 B、3种 C、4种 D、5种18. 储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料,如镧(La)镍(Ni)合金,它吸收氢气可结合成金属氢化物。某镧镍储氢合金晶胞结构如图,该材料中镧、镍、氢的原子个数比为( )
A、2种 B、3种 C、4种 D、5种18. 储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料,如镧(La)镍(Ni)合金,它吸收氢气可结合成金属氢化物。某镧镍储氢合金晶胞结构如图,该材料中镧、镍、氢的原子个数比为( ) A、8:9:10 B、1:5:6 C、1:5:3 D、1:5:5
A、8:9:10 B、1:5:6 C、1:5:3 D、1:5:5二、综合题
-
19. 第三周期元素的化合价与原子序数的关系如图所示,请回答下列问题:
 (1)、B的一种单质为浅黄色或白色半透明性固体,暴露在空气中易自燃,则该单质为(用化学式表示);其分子的空间构型为。(2)、X、Y、Z的原子半径从大到小的顺序为(用元素符号表示);比较R、W两种元素对应氢化物稳定性的大小:(用化学式表示)。(3)、写出X、R两种元素最高价氧化物对应的水化物反应的离子方程式:。(4)、A的最高价氧化物属于晶体。20. 世界上最早发现并使用锌的是中国,明朝末年《天工开物》一书中有关于炼锌技术的记载。回答下列问题:(1)、Zn在元素周期表中位于区。(2)、硫酸锌溶于过量的氨水可形成配合物[Zn(NH3)4]SO4。
(1)、B的一种单质为浅黄色或白色半透明性固体,暴露在空气中易自燃,则该单质为(用化学式表示);其分子的空间构型为。(2)、X、Y、Z的原子半径从大到小的顺序为(用元素符号表示);比较R、W两种元素对应氢化物稳定性的大小:(用化学式表示)。(3)、写出X、R两种元素最高价氧化物对应的水化物反应的离子方程式:。(4)、A的最高价氧化物属于晶体。20. 世界上最早发现并使用锌的是中国,明朝末年《天工开物》一书中有关于炼锌技术的记载。回答下列问题:(1)、Zn在元素周期表中位于区。(2)、硫酸锌溶于过量的氨水可形成配合物[Zn(NH3)4]SO4。① 中,中心原子轨道的杂化类型为。
②NH3极易溶于水,除了因为它们都是极性分子外,还因为。
(3)、Zn2+的4s和4p轨道可以形成sp3型杂化轨道,那么[ZnCl4]2-的空间构型为。(4)、氧化锌的结构有多种其中一种立方闪锌矿的结构如图所示,若该晶胞的边长为anm,NA为阿伏加德罗常数的值,则立方闪锌矿晶体的密度为(列出计算式即可)g•cm-3。 21. 正丁醚常用作有机合成反应的溶剂.某实验小组利用如图装置(夹持和加热装置均省略)合成正丁醚,其反应原理如下:
21. 正丁醚常用作有机合成反应的溶剂.某实验小组利用如图装置(夹持和加热装置均省略)合成正丁醚,其反应原理如下:2CH3CH2CH2CH2OH CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
反应物和产物的相关数据如表:
化合物名称
密度(g•mL-1)
熔点(℃)
沸点(℃)
水中溶解性
正丁醇
0.810
-89.8
118.0
微溶
正丁醚
0.769
-95.3
142.0
不溶于水
备注:正丁醚微溶于饱和氯化钙溶液

实验步骤:
①将14.80g正丁醇、2.5mL浓硫酸加入两口烧瓶中,再加入几粒碎瓷片,摇匀
②装好分水器和温度计
③控制反应温度在134~136℃之间,回流1.5h
④将分水器中的下层水层从下口放出,上层液体倒回两口烧瓶中
⑤将反应液冷却到室温后倒入盛有25mL水的分液漏斗中,经过分离、洗涤后再分离提纯,收集称重得正丁醚7.15g
回答下列问题:
(1)、实验中冷凝管的进水口为(填“a”或“b”)。(2)、在该实验中两口烧瓶的容积最适合的是______(填字母)。A、200mL B、150mL C、100mL D、50mL(3)、实验中温度过高则发生分子内脱水生成烃类化合物,写出生成烃类化合物反应的化学方程式:。(4)、有机层粗产物需依次用水洗、氢氧化钠溶液洗涤、水洗和饱和氯化钙溶液洗涤。用氢氧化钠溶液洗涤的目的是。(5)、洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是(填字母)。
A.蒸馏 B.加入无水CaCl2 C.过滤(6)、本实验所得正丁醚的产率为。22. 磷酸氯喹是一种抗疟疾的药物,已在临床上使用多年。同时临床上还发现它对新冠肺炎有一定疗效,且未发现和药物有关的严重不良反应。 是合成磷酸氯喹(的中间体,可由苯在一定条件下合成,其合成路线如图:
是合成磷酸氯喹(的中间体,可由苯在一定条件下合成,其合成路线如图: 
已知:①CH3CH2OH CH3CH2Cl
②RNH2+R'X RNHR'+HX(X为卤素原子)
③
 +NaOH→
+NaOH→  +H2O
+H2O回答下列问题:
(1)、E中含氧官能团的名称为。(2)、C→D的反应类型为。(3)、F的结构简式为。(4)、E→F反应分两步进行,先与氢氧化钠反应,再酸化。请写出E与氢氧化钠反应的化学方程式:。(5)、由D转化成E的过程中需要使用丙二酸二乙酯,其分子式为C7H12O4。M与丙二酸二乙酯互为同分异构体,符合下列条件的M的结构有种;其中核磁共振氢谱显示只有3组峰,且峰面积之比为9:2:1的结构简式为。①分子中含有三个甲基;②1molM能与足量的碳酸氢钠溶液反应生成标准状况下的气体44.8L。