辽宁省葫芦岛市2019-2020学年高二下学期化学期末考试试卷
试卷更新日期:2021-04-25 类型:期末考试
一、单选题
-
1. 关于晶体的叙述中,正确的是( )A、原子晶体中,共价键的键能越大,熔、沸点越高 B、分子晶体中,分子间的作用力越大,该分子越稳定 C、金属晶体中,原子半径越大,金属键越强 D、某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体2. 下列化合物命名正确的是( )A、
 2-乙基丁烷
B、
2-乙基丁烷
B、 2-甲基-2-氯丙烷
C、
2-甲基-2-氯丙烷
C、 2-甲基-1-丙醇
D、
2-甲基-1-丙醇
D、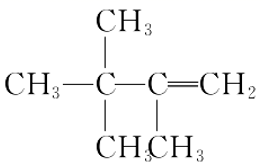 2,2,3-三甲基-3-丁烯
3. 下列实验事实能说明苯酚属于弱酸的是( )A、苯酚溶液的pH<7 B、苯酚能与NaOH溶液反应 C、将CO2通入苯酚钠溶液出现浑浊 D、常温下苯酚在水中的溶解度不大4. 下列说法正确的是( )A、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 B、天然纤维、人造纤维的主要成分都是纤维素 C、蛋白质和氨基酸都是两性分子,既能与酸反应又能与碱反应 D、若两种二肽互为同分异构体,则二者的水解产物一定相同5. 以下实验能获得成功的是( )A、用酸性KMnO4溶液鉴别乙烯和乙炔 B、将铁屑、溴水、苯混合制溴苯 C、在苯和硝基苯采用分液的方法分离 D、将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色6. 除去下列物质中少量杂质(括号内为杂质),所选试剂和分离方法能达到实验目的的是( )
2,2,3-三甲基-3-丁烯
3. 下列实验事实能说明苯酚属于弱酸的是( )A、苯酚溶液的pH<7 B、苯酚能与NaOH溶液反应 C、将CO2通入苯酚钠溶液出现浑浊 D、常温下苯酚在水中的溶解度不大4. 下列说法正确的是( )A、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 B、天然纤维、人造纤维的主要成分都是纤维素 C、蛋白质和氨基酸都是两性分子,既能与酸反应又能与碱反应 D、若两种二肽互为同分异构体,则二者的水解产物一定相同5. 以下实验能获得成功的是( )A、用酸性KMnO4溶液鉴别乙烯和乙炔 B、将铁屑、溴水、苯混合制溴苯 C、在苯和硝基苯采用分液的方法分离 D、将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色6. 除去下列物质中少量杂质(括号内为杂质),所选试剂和分离方法能达到实验目的的是( )混合物
试剂
分离方法
A
苯(苯酚)
溴水
过滤
B
乙醇(溴乙烷)
蒸馏水
分液
C
乙酸乙酯(乙酸)
氢氧化钠溶液
蒸馏
D
苯(甲苯)
酸性高锰酸钾溶液、氢氧化钠溶液
分液
A、A B、B C、C D、D7. 青蒿素一般是从青蒿中提取,也可进行化学合成,其中的一种合成方法如下:








① ② ③ ④
下列说法正确的是( )
A、化合物①的分子式为C10H17O B、化合物②和③互为同分异构体 C、化合物④中含有3种含氧官能团 D、利用青蒿研究青蒿素结构的基本步骤为:元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式8. 下列有关离子晶体的数据大小比较错误的是( )A、熔点:NaF>MgF2>AlF3 B、晶格能:NaF>NaCl>NaBr C、阴离子的配位数:CsCl>NaCl>CaF2 D、硬度:MgO>CaO>BaO9. 某有机物M的结构简式为 ,下列说法正确的是( ) A、M名称为2,4,4-三甲基-3-乙基-3-戊醇 B、M的消去反应产物有3种 C、M的一氯代物有5种 D、M不能发生氧化反应10. 下列数据是对应物质的熔点,有关的判断错误的是( )
,下列说法正确的是( ) A、M名称为2,4,4-三甲基-3-乙基-3-戊醇 B、M的消去反应产物有3种 C、M的一氯代物有5种 D、M不能发生氧化反应10. 下列数据是对应物质的熔点,有关的判断错误的是( )Na2O
Na
AlF3
AlCl3
Al2O3
BCl3
CO2
SiO2
920℃
97.8℃
1291℃
190℃
2073℃
-107℃
-57℃
1723℃
A、同族元素的氧化物可形成不同类型的晶体 B、含有金属阳离子的晶体不一定是离子晶体 C、在共价化合物分子中各原子都形成8电子结构 D、金属晶体的熔点不一定比分子晶体的高11. 如图为甲、乙、丙三种晶体的晶胞:
下列说法正确的是( )
A、甲晶体化学式(X为阳离子)为XY B、乙晶体中A,B,C三种微粒的个数比是1:2:1 C、丙晶体中每个D周围结合E的个数是4 D、乙晶体中每个A周围结合B的个数为1212. 有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( ) A、①为简单立方堆积,②为六方最密堆积,③为体心立方堆积,④为面心立方最密堆积 B、每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个 C、晶胞中原子的配位数分别为:①6,②8,③8,④12 D、空间利用率的大小关系为:①<②<③<④13. 下列化合物中,核磁共振氢谱只出现三组峰且峰面积之比为3∶2∶2的是( )A、
A、①为简单立方堆积,②为六方最密堆积,③为体心立方堆积,④为面心立方最密堆积 B、每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个 C、晶胞中原子的配位数分别为:①6,②8,③8,④12 D、空间利用率的大小关系为:①<②<③<④13. 下列化合物中,核磁共振氢谱只出现三组峰且峰面积之比为3∶2∶2的是( )A、 B、
B、 C、
C、 D、
D、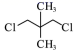 14. 已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是( )
14. 已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是( ) A、若A的化学式为C2H6O,则其结构简式为CH3-O-CH3 B、由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子 C、由红外光谱可知,该有机物中至少含有三种不同的化学键 D、仅由其核磁共振氢谱无法得知其分子中的氢原子总数15. 下列有关有机物同分异构体说法中错误的是( )A、三联苯(
A、若A的化学式为C2H6O,则其结构简式为CH3-O-CH3 B、由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子 C、由红外光谱可知,该有机物中至少含有三种不同的化学键 D、仅由其核磁共振氢谱无法得知其分子中的氢原子总数15. 下列有关有机物同分异构体说法中错误的是( )A、三联苯( )的一氯代物有4种
B、立方烷(
)的一氯代物有4种
B、立方烷(  )经硝化可得到六硝基立方烷,其可能的结构有3种
C、β-月桂烯(
)经硝化可得到六硝基立方烷,其可能的结构有3种
C、β-月桂烯(  )与溴发生1:1加成反应,产物(不考虑顺反异构)有3种
D、酯类化合物C4H8O2在酸性条件下水解得到的醇可能有4种不同结构
16. 化合物Y能用于高性能光学树脂的合成,可由化合物X与2-甲基丙烯酰氯在一定条件下反应制得:
)与溴发生1:1加成反应,产物(不考虑顺反异构)有3种
D、酯类化合物C4H8O2在酸性条件下水解得到的醇可能有4种不同结构
16. 化合物Y能用于高性能光学树脂的合成,可由化合物X与2-甲基丙烯酰氯在一定条件下反应制得: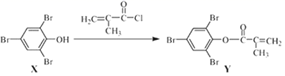
下列有关化合物X、Y的叙述正确的是( )
A、X分子中所有原子一定在同一平面上 B、X→Y的反应为加成反应 C、X、Y均能使Br2的四氧化碳溶液褪色 D、1mol Y与足量氢氧化钠溶液共热最多可消耗8 mol NaOH二、综合题
-
17. 下表是A、B、X、D、E五种有机物的有关信息。
A
A的结构简式
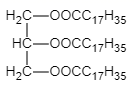
B
①能使溴的四氯化碳溶液褪色;②比例模型为
 ;③能与水在一定条件下反应生成D
;③能与水在一定条件下反应生成DX
①由C、H两种元素组成;②球棍模型为

D
①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应
E
①由C、H、O三种元素组成;②球棍模型为
 (1)、B与溴的四氧化碳溶液反应的生成物的名称是。(2)、写出在浓硫酸作用下,X与浓硝酸反应的化学方程式。(3)、A与足量NaOH溶液共热发生皂化反应的化学方程式是。(4)、若以B为主要原料合成乙酸,其合成路线如图所示:
(1)、B与溴的四氧化碳溶液反应的生成物的名称是。(2)、写出在浓硫酸作用下,X与浓硝酸反应的化学方程式。(3)、A与足量NaOH溶液共热发生皂化反应的化学方程式是。(4)、若以B为主要原料合成乙酸,其合成路线如图所示:
①F的结构简式为。
②反应②的反应类型为。
③工业上以B为原料可以合成一种有机高分子。写出反应的化学方程式。
(5)、写出D与E反应的化学方程式。18. 已知:通常羟基与碳碳双键相连时不稳定,易发生下列变化: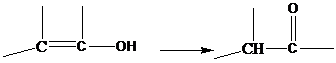
依据如下图所示的转化关系,回答问题:
 (1)、写出A分子中含有的官能团(填名称);(2)、B的结构简式是。(3)、①的化学方程式是;(4)、F是芳香族化合物且苯环上只有一个侧链,③的化学方程式是。(5)、G是F的同分异构体,有关G的描述;①能发生水解,②苯环上有三个取代基,③苯环上一溴代物有2种。据此推测G的结构简式可能是(写出其中一种)。19. 为了研究有机物A的组成与结构,某同学进行如下实验。
(1)、写出A分子中含有的官能团(填名称);(2)、B的结构简式是。(3)、①的化学方程式是;(4)、F是芳香族化合物且苯环上只有一个侧链,③的化学方程式是。(5)、G是F的同分异构体,有关G的描述;①能发生水解,②苯环上有三个取代基,③苯环上一溴代物有2种。据此推测G的结构简式可能是(写出其中一种)。19. 为了研究有机物A的组成与结构,某同学进行如下实验。i.将9.0 g A在足量氧气中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4 g和13.2 g。
ii.通过质谱法测得其相对分子质量为90。
iii.通过红外光谱法测得A中含有-OH和-COOH。
请回答下列问题。
(1)、9.0 g A完全燃烧生成水的物质的量是mol。(2)、A的分子式是。(3)、在一定条件下,若两个A分子可以反应得到一个六元环的分子,还能发生缩聚反应,写出A发生缩聚反应的方程式。(4)、试写出由与A含有相同C原子数的烯烃为原料(无机试剂及催化剂任用)合成A的合成路线。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。20. 下图为几种晶体或晶胞的示意图: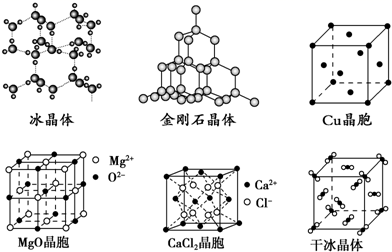
请回答下列问题:
(1)、上述晶体中,粒子之间以共价键结合形成的晶体是。(2)、冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为。(3)、NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能(填“大于”或“小于”)MgO晶体,原因是。(4)、每个Cu晶胞中实际占有个Cu原子,CaCl2晶体中Ca2+的配位数为。(5)、冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是。(6)、MgO晶胞密度为d g/cm3 , 则MgO晶胞的边长为。21. 如图所示是完成1,2-二氯乙烷某些性质的实验装置。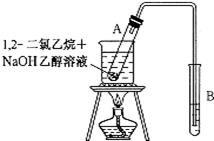 (1)、按图所示连接好仪器后,首先应进行的操作是。(2)、在试A里加入2 mL 1,2-二氧乙烷和5 mL 10%的NaOH乙醇溶液,再向试管里加入几小块碎瓷片。加入碎瓷片的作用是。(3)、用水浴加热试管A里的混合物(其主要生成物仍为卤代烃),试管A中发生反应的化学方程式是 , 其反应类型是。(4)、为检验产生的气体,可在试管B中盛放 , 现象是;向反应后试管A中的溶液里加入足量的稀硝酸,再加入几滴AgNO3溶液,现象是。
(1)、按图所示连接好仪器后,首先应进行的操作是。(2)、在试A里加入2 mL 1,2-二氧乙烷和5 mL 10%的NaOH乙醇溶液,再向试管里加入几小块碎瓷片。加入碎瓷片的作用是。(3)、用水浴加热试管A里的混合物(其主要生成物仍为卤代烃),试管A中发生反应的化学方程式是 , 其反应类型是。(4)、为检验产生的气体,可在试管B中盛放 , 现象是;向反应后试管A中的溶液里加入足量的稀硝酸,再加入几滴AgNO3溶液,现象是。