辽宁省大连市2019-2020学年高二下学期化学期末考试试卷
试卷更新日期:2021-04-25 类型:期末考试
一、单选题
-
1. 化学与生活、生产密切相关,下列有关说法错误的是( )A、“一带一路”是“丝绸之路经济带”和“21 世纪海上丝绸之路”的简称。丝绸的主要成 分是蛋白质,属于高分子化合物 B、新型冠状病毒是一种致病性很强的病毒,可用“乙醇、84 消毒液”消毒,让病毒蛋 白质变性死亡 C、3M 防颗粒物口罩均使用 3M 专有高效过滤材料——聚丙烯材质,聚丙烯是通 过丙烯发生缩聚反应制得,属于混合物 D、压缩天然气(CNG)、液化石油气(LPG)主要成分是烃类,是城市推广的清洁燃料2. 下列表述正确的是( )A、羟基的电子式:
 B、聚丙烯的结构简式:
B、聚丙烯的结构简式:  C、2-丁烯的顺式结构:
C、2-丁烯的顺式结构: 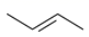 D、2-丙醇的结构简式:
D、2-丙醇的结构简式:  3. 下列离子中,中心原子的杂化方式与其它三种不同的是( )A、 B、 C、 D、4. 《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3) 经常用来修改错字,其结构如图所示。下列说法错误的是( )
3. 下列离子中,中心原子的杂化方式与其它三种不同的是( )A、 B、 C、 D、4. 《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。在中国古代,雌黄(As2S3) 经常用来修改错字,其结构如图所示。下列说法错误的是( ) A、As、S 原子的杂化方式均为 sp3 B、AsH3 的沸点比 NH3 的低 C、As 的价电子排布式为 3d104s24p3 D、已知 As2F2 分子中各原子均满足 8 电子结构,分子中σ键和π键的个数比为 3:15. 下列说法正确的是( )A、
A、As、S 原子的杂化方式均为 sp3 B、AsH3 的沸点比 NH3 的低 C、As 的价电子排布式为 3d104s24p3 D、已知 As2F2 分子中各原子均满足 8 电子结构,分子中σ键和π键的个数比为 3:15. 下列说法正确的是( )A、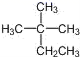 的系统命名为 2−甲基−2−乙基丙烷
B、用溴水可以确定CH2=CH−CHO中含有 C=C 双键
C、可以用裂化汽油萃取溴水中的溴
D、聚乳酸 (
的系统命名为 2−甲基−2−乙基丙烷
B、用溴水可以确定CH2=CH−CHO中含有 C=C 双键
C、可以用裂化汽油萃取溴水中的溴
D、聚乳酸 (  )的降解过程中会发生取代反应
6. 已知X,Y,Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面表示该化合物的化学式正确的( )
)的降解过程中会发生取代反应
6. 已知X,Y,Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面表示该化合物的化学式正确的( ) A、ZXY3 B、ZX2Y6 C、ZX4Y8 D、ZX8Y127. 下列实验内容能达到实验目的的是( )
A、ZXY3 B、ZX2Y6 C、ZX4Y8 D、ZX8Y127. 下列实验内容能达到实验目的的是( )实验目的
实验内容
A
鉴别乙醇与乙醛

B
比较乙酸、碳酸、苯酚的酸性
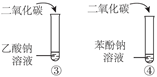
C
说明烃基对羟基上氢原子活性的影响

D
说明苯环对取代基上氢原子活性的影响
 A、A B、B C、C D、D8. 下列有关晶体的叙述中错误的是( )A、石墨的层状结构中碳碳键键长比金刚石中碳碳键键长短 B、氯化钠晶体中每个 Na+周围紧邻的有6个Cl- C、CsCl 晶体中,与每个 Cs+周围紧邻的有 8 个Cl-和 8 个 Cs+ D、在面心立方最密堆积的金属晶体中,每个金属原子周围紧邻的有 12 个金属原子9. 关于如图结构的化合物,说法错误的是( )
A、A B、B C、C D、D8. 下列有关晶体的叙述中错误的是( )A、石墨的层状结构中碳碳键键长比金刚石中碳碳键键长短 B、氯化钠晶体中每个 Na+周围紧邻的有6个Cl- C、CsCl 晶体中,与每个 Cs+周围紧邻的有 8 个Cl-和 8 个 Cs+ D、在面心立方最密堆积的金属晶体中,每个金属原子周围紧邻的有 12 个金属原子9. 关于如图结构的化合物,说法错误的是( ) A、分子中既有σ键又有π键 B、分子中碳原子有三种杂化方式且存在顺反异构现象 C、1mol 该分子与足量的浓溴水反应,最多可消耗 4mol Br2 D、羟基中氧原子采取 sp3 杂化,VSEPR 模型为四面体形10. 下列化合物中同分异构体数目最少的是( )A、C5H11Cl B、C5H12O C、C5H10 D、C4H8O211. 有5种元素X、Y、Z、Q、T。X原子的价电子排布式为(n+2)sn;Y原子的特征电子构型为3d64s2;Z原子的核外电子总数等于Q原子的最外层电子数;Q原子的L电子层的p能级上只有一对成对电子;T原子有1个3p空轨道。下列叙述错误的是( )A、元素Y和 Q可形成化合物Y2Q3 B、气态氢化物的稳定性:Q>T>Z C、X和Q结合生成的化合物晶体类型为离子晶体 D、T和Z的最高价氧化物晶体类型不同12. 用 NA 表示阿伏加德罗常数的值,下列叙述错误的是( )A、12 g 金刚石中含有的共价键数为 2NA B、14 g 乙烯和丁烯的混合物中含有的原子总数为 3NA C、标准状况下,22.4 L 乙醇含有的氧原子数目为 NA D、乙醇催化氧化生成 1mol 乙醛转移的电子数为 2NA13. 我国自主研发的对二甲苯绿色合成项目取得新进展,其合成过程如图所示。
A、分子中既有σ键又有π键 B、分子中碳原子有三种杂化方式且存在顺反异构现象 C、1mol 该分子与足量的浓溴水反应,最多可消耗 4mol Br2 D、羟基中氧原子采取 sp3 杂化,VSEPR 模型为四面体形10. 下列化合物中同分异构体数目最少的是( )A、C5H11Cl B、C5H12O C、C5H10 D、C4H8O211. 有5种元素X、Y、Z、Q、T。X原子的价电子排布式为(n+2)sn;Y原子的特征电子构型为3d64s2;Z原子的核外电子总数等于Q原子的最外层电子数;Q原子的L电子层的p能级上只有一对成对电子;T原子有1个3p空轨道。下列叙述错误的是( )A、元素Y和 Q可形成化合物Y2Q3 B、气态氢化物的稳定性:Q>T>Z C、X和Q结合生成的化合物晶体类型为离子晶体 D、T和Z的最高价氧化物晶体类型不同12. 用 NA 表示阿伏加德罗常数的值,下列叙述错误的是( )A、12 g 金刚石中含有的共价键数为 2NA B、14 g 乙烯和丁烯的混合物中含有的原子总数为 3NA C、标准状况下,22.4 L 乙醇含有的氧原子数目为 NA D、乙醇催化氧化生成 1mol 乙醛转移的电子数为 2NA13. 我国自主研发的对二甲苯绿色合成项目取得新进展,其合成过程如图所示。
下列说法错误的是( )
A、异戊二烯所有碳原子可能共平面 B、可用高锰酸钾鉴别 M 和对二甲苯 C、对二甲苯的一氯代物有 2 种 D、M的同分异构体中不可能含有苯环二、多选题
-
14. 下列图中结构是从不同晶体中分割出来的一部分,其中是从NaCl晶体中分割出来的是( )A、
 B、
B、 C、
C、 D、
D、 15. 中成药连花清瘟胶囊在对抗新冠病毒中发挥重大作用,从金银花提取的有效成分绿 原酸的结构简式如图,下列有关说法错误的是( )
15. 中成药连花清瘟胶囊在对抗新冠病毒中发挥重大作用,从金银花提取的有效成分绿 原酸的结构简式如图,下列有关说法错误的是( ) A、1mol 绿原酸与 Na 反应放出H2的体积134.4L B、绿原酸属于芳香族化合物,分子式C16H18O9 C、1mol 绿原酸最多可消耗 5mol NaOH D、绿原酸中含有 4 个手性碳原子
A、1mol 绿原酸与 Na 反应放出H2的体积134.4L B、绿原酸属于芳香族化合物,分子式C16H18O9 C、1mol 绿原酸最多可消耗 5mol NaOH D、绿原酸中含有 4 个手性碳原子三、综合题
-
16. 有下列八种晶体:A 水晶(SiO2)、B 冰醋酸、C 氧化镁、D 白磷(P4)、E 干冰(CO2)、F氯化铵、G 铝、H 金刚石。回答下列问题:(1)、属于原子晶体的化合物是(填字母,下同),受热熔化后化学键不发生变化的是。(2)、1mol SiO2 含有mol Si—O 键,1mol 白磷(P4)含有mol P—P 键。(3)、从原子半径大小角度解释,同一主族的 C 与 Si,形成 CO2 和 SiO2 时,C、O 原子间 能形成π键,而 Si、O 之间不能的原因。(4)、升高温度,金属铝的电导率(填“升高”、“降低”或“不变”)。17. 实验室用少量的溴和足量的乙醇制备 1,2-二溴乙烷的装置如图所示:
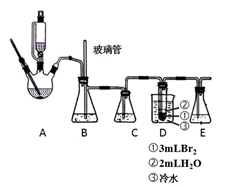
已知:
乙醇
1,2-二溴乙烷
乙醚
状态
无色液体
无色液体
无色液体
密度/g·cm-3
0.79
2.2
0.71
沸点/℃
78.5
132
34.6
熔点/℃
-130
9
-116
回答下列问题
(1)、组装仪器后进行该实验前必须进行的操作是。(2)、装置B的作用是。(3)、在装置 C 中最佳加入试剂为 , C内发生的主要反应的离子方程式为。(4)、装置D中发生主要反应的化学方程式为。(5)、反应过程中应用冷水冷却装置D,其主要目的是;下列冷却剂合适的为A 冰水混合物 B 5℃的水 C 10℃的水
(6)、判断反应结束的现象是。将 1,2-二溴乙烷粗产品 置于分液漏斗中加水,振荡后静置,产物应在层 ( 填“上”或“下” )(7)、在装置 E 中应加入 , 作用是。(8)、下列操作中,不会导致产物产率降低的是(填正确答案的标号)a 乙烯通入溴水时速率太快 b 装置 C 中的溶液用水代替
c D 中试管内液溴上不加水 d 实验时没有 E 装置
18. 水杨酸配合物在医药、农业等方面有重要的用途,一种水杨酸铜配合物(E) 的合成如下:
回答下列问题:
(1)、同周期第一电离能比氧大的元素有种。(2)、圈出如图醋酸酐分子中采取 sp3 杂化的原子。 (3)、邻甲基苯酚(A)在热水中的溶解度比冷水显著增大的主要原因是:。(4)、Cu(NO3)2中的化学键,除了σ键外,还存在。(5)、配离子中,Cu2+的配位数为 , 价电子的电子排布式为。(6)、写出反应③的离子方程式:。19. 氟及锗其化合物用途非常广泛。回答下列问题:(1)、聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过方法区分晶体、准晶体和非晶体。(2)、[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+ , 该离子的空间构型为;(3)、NH4BF4是合成氮化硼纳米管的原料之一,1mol NH4BF4含有mol配位键。(4)、向[Cu(H2O)4]2+溶液(天蓝色)中加入过量氨水将生成更稳定的[Cu(NH3)4]2+溶液(深蓝色),原因是;向深蓝色溶液中逐滴加入足量的稀硫酸,观察到的现象是。(5)、Ge 单晶具有金刚石型的结构,如图为晶胞结构,其中原子坐标参数 A 为(0,0,0),B 为( ,0, ),C 为( , ,0),D 原子的坐标参数为;晶体 Ge 的半径为 r,则计算其空间利用率的表达式为(用含有 r 的表达式表示,不必化简)。若晶胞参数为 a nm,Ge 的相对原子质量为 M,NA表示阿伏加德罗常数,则其晶胞密度为g/cm3(列出计算式即可)。
(3)、邻甲基苯酚(A)在热水中的溶解度比冷水显著增大的主要原因是:。(4)、Cu(NO3)2中的化学键,除了σ键外,还存在。(5)、配离子中,Cu2+的配位数为 , 价电子的电子排布式为。(6)、写出反应③的离子方程式:。19. 氟及锗其化合物用途非常广泛。回答下列问题:(1)、聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过方法区分晶体、准晶体和非晶体。(2)、[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+ , 该离子的空间构型为;(3)、NH4BF4是合成氮化硼纳米管的原料之一,1mol NH4BF4含有mol配位键。(4)、向[Cu(H2O)4]2+溶液(天蓝色)中加入过量氨水将生成更稳定的[Cu(NH3)4]2+溶液(深蓝色),原因是;向深蓝色溶液中逐滴加入足量的稀硫酸,观察到的现象是。(5)、Ge 单晶具有金刚石型的结构,如图为晶胞结构,其中原子坐标参数 A 为(0,0,0),B 为( ,0, ),C 为( , ,0),D 原子的坐标参数为;晶体 Ge 的半径为 r,则计算其空间利用率的表达式为(用含有 r 的表达式表示,不必化简)。若晶胞参数为 a nm,Ge 的相对原子质量为 M,NA表示阿伏加德罗常数,则其晶胞密度为g/cm3(列出计算式即可)。 20. 盐酸普鲁卡因是临床广泛使用的局部麻醉药,具有良好的局部麻醉作用,毒性小的特点。由浓盐酸与普鲁卡因化合而成,利用常见原料制备盐酸普鲁卡因的合成路线如下:
20. 盐酸普鲁卡因是临床广泛使用的局部麻醉药,具有良好的局部麻醉作用,毒性小的特点。由浓盐酸与普鲁卡因化合而成,利用常见原料制备盐酸普鲁卡因的合成路线如下:
已知:
Ⅰ.苯环上的取代基为-NH2、-OH、-CH3等时,在取代反应中,新取代基大多进入邻位或 对位;苯环上的取代基为-NO2、-COOH、-CN 等时,在取代反应中,新取代基大多进入 间位。
Ⅱ.
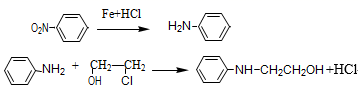
回答下列问题:
(1)、C的名称为;E中含氮的官能团名称为;A →B的反应条件为;A → B的反应类型为。(2)、D→E步骤的目的是。(3)、D生成高聚物的化学方程式:。(4)、普鲁卡因在血浆中能被酯酶水解,写出其在氢氧化钠溶液中水解的化学方程式:。(5)、符合下列条件的D的同分异构体有种(不考虑立体异构)。①苯环上只有两个取代基,②能发生银镜反应,③不含N-O键;其中核磁共振氢谱为四组峰,且峰面积之比为1:2:2:2的结构简式为。