浙教版科学八下第三章 第3节化学方程式(基础巩固)
试卷更新日期:2021-04-23 类型:同步测试
一、单选题
-
1. 把6g碳在24g氧气中充分燃烧,生成二氧化碳的质量是( )A、30g B、22g C、32g D、44g2. 甲醛是室内装修时产生的主要污染物质。用下面化学反应可检测室内甲醛含量是否超标:4KMnO4+5R+6H2SO4=2K2SO4+4MnSO4+5CO2+11H2O,根据质量守恒定律确定R的化学式为( )A、CH2O B、C2H4O2 C、CH4 D、CHO23. 植物光合作用可表示为CO2+H2O 淀粉+O2 , 下列说法中正确的是( )A、淀粉中一定含C,H两种元素 B、淀粉中一定只含C,H两种元素 C、淀粉中可能含有三种以上的元素 D、淀粉可能是一种单质或一种化合物4. 水通电分解成氢气和氧气的反应前后,发生改变的是( )A、元素种类 B、原子种类 C、分子种类 D、原子数量5. 在化学方程式“A+B=C+D”中,若12g A与一定量的B恰好完全反应,生成28g C和2g D,则参加反应的B的质量为( )A、8g B、18g C、28g D、30g6. 同学们对化学反应方程式:C+O2=CO2 , 有下面的四种说法,其中错误的是( )A、
 B、
B、 C、
C、 D、
D、 7. 对化学方程式“ ”的叙述正确的是( )A、氢气加氧气在点燃的条件下反应生成水 B、两个氢气和一个氧气在点燃的条件下反应生成两个水 C、两份质量的氢气和一份质量的氧气在点燃的条件下反应生成两份质量的水 D、氢气和氧气在点燃的条件下反应生成水8. “丹砂烧之成水银”中的“丹砂”指的是硫化汞,该反应的微观示意图如下。有关说法错误的是( )
7. 对化学方程式“ ”的叙述正确的是( )A、氢气加氧气在点燃的条件下反应生成水 B、两个氢气和一个氧气在点燃的条件下反应生成两个水 C、两份质量的氢气和一份质量的氧气在点燃的条件下反应生成两份质量的水 D、氢气和氧气在点燃的条件下反应生成水8. “丹砂烧之成水银”中的“丹砂”指的是硫化汞,该反应的微观示意图如下。有关说法错误的是( )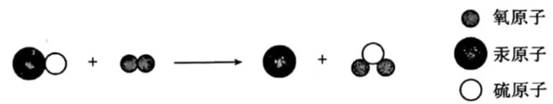 A、
A、 是一种氧化物
B、此反应遵循质量守恒定律
C、反应前后分子的种类发生改变
D、反应前后各元素的化合价都不变
9. 下列化学方程式,书写正确的是( )A、P+O2 PO2 B、2P+5O2 P2O5 C、4P+5O2=P2O5 D、4P+5O2 2P2O510. 工业用盐亚硝酸钠(NaNO2)有毒,其外观与食盐极为相似,在隔绝空气和强热条件下,亚硝酸钠能分解放出一种红棕色气体,该气体可能是( )A、N2 B、CO C、NO2 D、O211. 由质量守恒定律可知,下列各项:①分子种类;②原子种类;③分子数目;④原子数目;⑤元素种类;⑥原子质量。在化学反应前后一定不变的是( )A、①③⑤ B、②④⑥ C、②④⑤⑥ D、③④⑤⑥12. NH4ClO4(高氯酸铵)可用作火箭推进剂,当它发生分解反应时,不能生成的物质是( )A、CO2 B、Cl2 C、O2 D、N213. 在化学反应A+B=C+D中,若有5克的A与11克的B恰好完全反应,生成7克的C和一定质量的D,则D的质量为( )A、5克 B、16克 C、9克 D、23克14. 化学方程式:2N2H4+X=3N2+ 4H2O是发射通讯卫星的火箭发生的化学反应。X的化学式是( )A、NO2 B、N2O C、N2O3 D、N2O415. 同学们对化学反应方程式:C+O2 CO2 , 有下面的四种说法,其中错误的是( )A、
是一种氧化物
B、此反应遵循质量守恒定律
C、反应前后分子的种类发生改变
D、反应前后各元素的化合价都不变
9. 下列化学方程式,书写正确的是( )A、P+O2 PO2 B、2P+5O2 P2O5 C、4P+5O2=P2O5 D、4P+5O2 2P2O510. 工业用盐亚硝酸钠(NaNO2)有毒,其外观与食盐极为相似,在隔绝空气和强热条件下,亚硝酸钠能分解放出一种红棕色气体,该气体可能是( )A、N2 B、CO C、NO2 D、O211. 由质量守恒定律可知,下列各项:①分子种类;②原子种类;③分子数目;④原子数目;⑤元素种类;⑥原子质量。在化学反应前后一定不变的是( )A、①③⑤ B、②④⑥ C、②④⑤⑥ D、③④⑤⑥12. NH4ClO4(高氯酸铵)可用作火箭推进剂,当它发生分解反应时,不能生成的物质是( )A、CO2 B、Cl2 C、O2 D、N213. 在化学反应A+B=C+D中,若有5克的A与11克的B恰好完全反应,生成7克的C和一定质量的D,则D的质量为( )A、5克 B、16克 C、9克 D、23克14. 化学方程式:2N2H4+X=3N2+ 4H2O是发射通讯卫星的火箭发生的化学反应。X的化学式是( )A、NO2 B、N2O C、N2O3 D、N2O415. 同学们对化学反应方程式:C+O2 CO2 , 有下面的四种说法,其中错误的是( )A、 B、
B、 C、
C、 D、
D、
二、填空题
-
16. 火电厂发电需要燃烧大量的煤,由于煤中含有硫元素,未经脱硫的煤燃烧后,产生的气体会导致严重的大气污染,进入水体,也会加剧水污染。硫能在空气中燃烧,燃烧后生成的气体排放到空气中,会形成酸雨。写出硫燃烧的化学方程式:。17. 植物的光合作用可表示为水+二氧化碳 淀粉+氧气,由此可推断淀粉一定含有元素,可能含元素。18. 水体中氮元素含量过高是河道水污染的主要原因之一。人造水草中的硝化细菌将污水中的含氮化合物最终转化为无污染物质,该过程涉及的化学反应之一是2NH3+3O2 2HNO2+2X,则X的化学式为。19. 配平化学方程式。
(1)、KClO3 KCl+O2↑(2)、CH4+O2 CO2+H2O(3)、N2+H2 NH3(4)、Na+H2O=NaOH+H2↑20. 二氧化硫是大气的主要污染物,严禁直接排放,工业上常用 NaOH溶液来吸收。(1)、写出NaOH溶液吸收SO2的化学方程式。
(2)、图中小球分别表示NaOH溶液及吸收SO2后所得溶液中溶质的微粒,其中“
 ”表示的微粒是。
”表示的微粒是。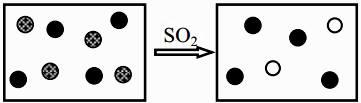 21. 1800年的一天,英国化学家戴维在实验室里制得一种气体,为弄清其物理性质,他凑近瓶口闻了闻,突然大笑起来。戴维让助手也凑近瓶口闻了闻,结果他的助手也忍俊不禁!于是戴维便发现了“笑气”,即一氧化二氮,其分子式为N2O. “笑气”可由NH4NO3微热分解产生,产物除N2O外,还有水,此反应的化学方程式为。22. 已知镁条在点燃条件下可以在二氧化碳中燃烧生成氧化镁和黑色的碳粒,此反应的化学方程式为 , 该燃烧反应中的助燃剂是。
21. 1800年的一天,英国化学家戴维在实验室里制得一种气体,为弄清其物理性质,他凑近瓶口闻了闻,突然大笑起来。戴维让助手也凑近瓶口闻了闻,结果他的助手也忍俊不禁!于是戴维便发现了“笑气”,即一氧化二氮,其分子式为N2O. “笑气”可由NH4NO3微热分解产生,产物除N2O外,还有水,此反应的化学方程式为。22. 已知镁条在点燃条件下可以在二氧化碳中燃烧生成氧化镁和黑色的碳粒,此反应的化学方程式为 , 该燃烧反应中的助燃剂是。
23. 能源、环境与人类的生活和社会发展密切相关.酒精(C2H5OH)是一种可再生能源,请写出酒精充分燃烧的化学方程式:.
24.1879年10月,经过对1600多种材料进行几千次试验后,爱迪生制成了第一个可供实用的碳丝灯泡(灯丝由竹丝炭化后制成)。
碳丝通电后产生高温,在空气中立即烧断,这是因为 (用化学反应方程式表示),所以碳丝灯泡必须抽成真空。
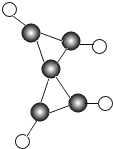
 25.
25.科学家最近在低温下合成了一种化合物,其分子模型如图所示,其中“
 ”代表碳原子,“
”代表碳原子,“ ”代表氢原子.
”代表氢原子.请补充该物质燃烧的化学方程式: .
三、解答题
-
26. 某学习小组用KClO3和MnO2的混合物加热制取O2 , 收集到4.8gO2后停止加热,称得剩余固体的质量为28.0g,继续加热至不再产生O2 , 最终剩余固体质量为23.2g,试计算(不考虑O2的损耗);(1)、两次生成O2的总质量为 g.(2)、理论上可回收到MnO2的质量(写出计算过程)27. 实验室有不纯的氯酸钾样品12.5g,把该样品与少量二氧化锰混合加热制取氧气(杂质不参加反应),充分反应后,固体混合物质量变化如下所示:
反应前固体总质量
反应后固体总质量
13.5g
8.7g
(1)、生成氧气的质量为 g.(2)、氯酸钾在样品中的质量分数是多少?四、实验探究题
-
28. 小科同学为了探究质量守恒定律,设计了如图“白磷燃烧前后质量测定”的实验(实验前天平已达到平衡)。请回答下列有关问题:
 (1)、白磷燃烧的化学方程式为。(2)、实验前要在锥形瓶底部铺一层细沙,其作用是防止。(3)、实验过程中,可看到气球的变化情况是。(4)、实验后发现天平指针偏向右边,造成这种结果的原因可能是(只回答一种可能)。(5)、白磷燃烧(填“遵循”、“不遵循”)质量守恒定律。29. 利用加热高锰酸钾的方法,验证化学反应中质量守恒定律。如图,小科将适量高锰酸钾装入试管,塞入一团棉花并测出试管、棉花与药品的总质量为m。加热使之充分反应后,测得量筒中气体体积为V,再次测得反应装置与物质总质量为m2,已知常温常压下氧气密度为p。据此请回答:
(1)、白磷燃烧的化学方程式为。(2)、实验前要在锥形瓶底部铺一层细沙,其作用是防止。(3)、实验过程中,可看到气球的变化情况是。(4)、实验后发现天平指针偏向右边,造成这种结果的原因可能是(只回答一种可能)。(5)、白磷燃烧(填“遵循”、“不遵循”)质量守恒定律。29. 利用加热高锰酸钾的方法,验证化学反应中质量守恒定律。如图,小科将适量高锰酸钾装入试管,塞入一团棉花并测出试管、棉花与药品的总质量为m。加热使之充分反应后,测得量筒中气体体积为V,再次测得反应装置与物质总质量为m2,已知常温常压下氧气密度为p。据此请回答: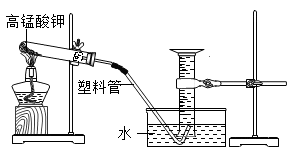 (1)、实验中用量筒收集气体的好处是。(2)、实验中,试管口内壁附着紫红色小液滴,请解释产生该现象的原因。(3)、根据实验数据计算发现: ,与质量守恒定律不符。造成这一实验结果的原因分析正确的是A、试管中高锰酸钾没有完全分解 B、导管口连续均匀冒气泡时才收集气体 C、未调节量筒内外液面相平就读数 D、停止加热时,先将导管移出水面,再熄灭酒精灯
(1)、实验中用量筒收集气体的好处是。(2)、实验中,试管口内壁附着紫红色小液滴,请解释产生该现象的原因。(3)、根据实验数据计算发现: ,与质量守恒定律不符。造成这一实验结果的原因分析正确的是A、试管中高锰酸钾没有完全分解 B、导管口连续均匀冒气泡时才收集气体 C、未调节量筒内外液面相平就读数 D、停止加热时,先将导管移出水面,再熄灭酒精灯