河南省南阳市邓州市2020年中考化学二模试卷
试卷更新日期:2021-04-20 类型:中考模拟
一、单选题
-
1. 下列著名诗句中未隐含化学变化的是( )A、忽如一夜春风来,千树万树梨花开 B、春风又绿江南岸,明月何时照我还 C、何当共剪西窗烛,却话巴山夜雨时 D、煮豆燃豆萁,豆在釜中泣2. “绿水青山就是金山银山”下列做法与该理念不相符的是( )A、合理使用化肥农药 B、生活垃圾分类处理 C、工业废水灌溉农田 D、推广秸秆综合利用3. 下列图示的实验操作中正确的是()A、
 点燃酒精灯
B、
点燃酒精灯
B、 稀释浓硫酸
C、
稀释浓硫酸
C、 测溶液的pH
D、
测溶液的pH
D、 制取氧气
4. 下列实验现象的描述正确的是( )A、镁条在空气中燃烧:发出耀眼的白光,放出热量,生成一种白色的固体 B、硫粉在氧气中燃烧:发出淡蓝色火焰,放出热量,生成有刺激性气味气体 C、打开浓盐酸试剂瓶:瓶口会出现白烟 D、铁粉与稀盐酸反应:固体表面产生气泡,溶液由无色变为黄色5. 下列关于水或溶液的说法正确的是( )A、过滤操作可以除去水中的钙镁离子 B、电解水实验得到的结论:水是由氢原子和氧原子构成 C、将食盐、蔗糖溶于水后,所得溶液中的溶质均以分子的形式存在 D、配制一定质量分数的氯化钠溶液,量取水时仰视读数会导致结果偏小6. 锌是人体必需的元素之一、如图为锌在元素周期表中的相关信息及其原子结构示意图,下列说法错误的是( )
制取氧气
4. 下列实验现象的描述正确的是( )A、镁条在空气中燃烧:发出耀眼的白光,放出热量,生成一种白色的固体 B、硫粉在氧气中燃烧:发出淡蓝色火焰,放出热量,生成有刺激性气味气体 C、打开浓盐酸试剂瓶:瓶口会出现白烟 D、铁粉与稀盐酸反应:固体表面产生气泡,溶液由无色变为黄色5. 下列关于水或溶液的说法正确的是( )A、过滤操作可以除去水中的钙镁离子 B、电解水实验得到的结论:水是由氢原子和氧原子构成 C、将食盐、蔗糖溶于水后,所得溶液中的溶质均以分子的形式存在 D、配制一定质量分数的氯化钠溶液,量取水时仰视读数会导致结果偏小6. 锌是人体必需的元素之一、如图为锌在元素周期表中的相关信息及其原子结构示意图,下列说法错误的是( ) A、锌原子的质子数为30 B、锌的相对原子质量为65.38 C、锌原子在化学反应中容易失去2个电子形成阴离子 D、锌元素位于元素周期表中第四周期7. 中医文化博大精深,中草药金银花中的绿原酸具有抗菌、消炎解毒等功效,绿原酸的化学式是C6H18O9 , 下列有关绿原酸的说法正确的是( )A、属于氧化物 B、其中氢元素的质量分数最大 C、碳、氢、氧三种元素的质量比为16:18:9 D、1个绿原酸分子中含有33个原子8.
A、锌原子的质子数为30 B、锌的相对原子质量为65.38 C、锌原子在化学反应中容易失去2个电子形成阴离子 D、锌元素位于元素周期表中第四周期7. 中医文化博大精深,中草药金银花中的绿原酸具有抗菌、消炎解毒等功效,绿原酸的化学式是C6H18O9 , 下列有关绿原酸的说法正确的是( )A、属于氧化物 B、其中氢元素的质量分数最大 C、碳、氢、氧三种元素的质量比为16:18:9 D、1个绿原酸分子中含有33个原子8.下列各组转化中,一定条件下均能一步实现的组合是( )
 A、①② B、①③ C、②③ D、①②③9. 除去下列物质中的杂质,所选方法正确的是( )
A、①② B、①③ C、②③ D、①②③9. 除去下列物质中的杂质,所选方法正确的是( )选项
物质
杂质
除去杂质的方法
A
C
CuO
加入足量稀硫酸,过滤、洗涤、干燥
B
NaCl
Na2CO3
加入足量稀硫酸,蒸发结晶
C
CO2
CO
通过氢氧化钠溶液
D
MnO2
NaCl
加水溶解、过滤、蒸发
A、A B、B C、C D、D10. 在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中两个时刻各物质的质量如图所示,图中a、b、c、d分别表示相应物质的质量。下列说法正确的是()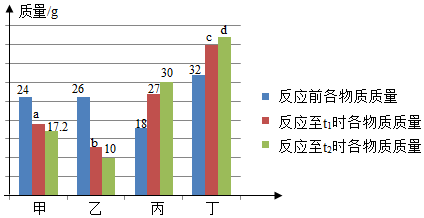 A、b的数值为14 B、该反应为复分解反应 C、反应过程中乙与丁发生改变的质量比为5:6 D、充分反应后生成丙的质量为37.5g11. 下 列各组物质在给定pH的溶液中能大量共存并形成无色透明溶液的是( )A、pH为3: KNO3、Na2SO4、ZnCl2 B、pH为12: MgSO4、 BaCl2、NaCl C、pH为1: NaCl、Na2CO3、KCl D、pH为11: CuSO4、KCl、NH4Cl12. 分析推理是化学学习中的常用方法。下列推理正确的是( )A、单质只含有一种元素,则只含有一种元素组成的物质一定是单质 B、离子是带电的一种微粒,所以带电的微粒一定是离子 C、溶液中有晶体析出,其溶质质量减小,则溶质的质量分数不一定减小 D、置换反应中有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应13. 下列图像不能正确反映对应变化关系的是( )A、
A、b的数值为14 B、该反应为复分解反应 C、反应过程中乙与丁发生改变的质量比为5:6 D、充分反应后生成丙的质量为37.5g11. 下 列各组物质在给定pH的溶液中能大量共存并形成无色透明溶液的是( )A、pH为3: KNO3、Na2SO4、ZnCl2 B、pH为12: MgSO4、 BaCl2、NaCl C、pH为1: NaCl、Na2CO3、KCl D、pH为11: CuSO4、KCl、NH4Cl12. 分析推理是化学学习中的常用方法。下列推理正确的是( )A、单质只含有一种元素,则只含有一种元素组成的物质一定是单质 B、离子是带电的一种微粒,所以带电的微粒一定是离子 C、溶液中有晶体析出,其溶质质量减小,则溶质的质量分数不一定减小 D、置换反应中有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应13. 下列图像不能正确反映对应变化关系的是( )A、 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量
B、
向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量
B、 向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量
C、
向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量
C、 向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D、
向盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量
D、 向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
14. 在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入等质量、等质量分数的稀盐酸,此时天平平衡;然后向左、右两烧杯中分别加入等质量下列各组物质,充分反应后,天平一定不平衡的是( )A、Fe和Zn B、Mg和MgO C、MgCO3和NaHCO3 D、CuO和Al2O3
向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量
14. 在托盘天平的两盘上各放一只质量相同的烧杯,在两只烧杯里分别加入等质量、等质量分数的稀盐酸,此时天平平衡;然后向左、右两烧杯中分别加入等质量下列各组物质,充分反应后,天平一定不平衡的是( )A、Fe和Zn B、Mg和MgO C、MgCO3和NaHCO3 D、CuO和Al2O3二、填空题
-
15. 开封“桶子鸡”是中华名吃,其主要食材鸡肉中富含的营养素为;卤制过程中需要加入一定量的加碘盐,人体中缺碘会导致的疾病是;焙制糕点所用发酵粉的主要成分之一的盐是(填写化学式)。16. 要使燃料充分燃烧,应考虑的因素是(写出一条即可);酒精灯是实验室常用的加热仪器,酒精完全燃烧的化学方程式为 , 酒精灯使用完毕后要用灯帽盖灭,其原理是。17. 化学源于生活,生活离不开化学。请用所学知识回答下列问题:(1)、生活中将硬水转化为软水常用的方法是。(2)、氢化镁(MgH2)可用来储氢,氢化镁与水反应生成一种单质和一种碱。写出该反应的化学方程式:。18. 将80gM物质加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示。A、B、C三点所对应的落液中,一定为不饱和溶液的为点处的溶液,20℃时,M物质的溶解度为g,将60℃时的130gM溶液稀释到20%,需加水的质量为g。
 19. 初中化学中,我们学习了酸和碱发生中和反应的实质是 。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式,难溶的物质、气体和水等仍用化学式表示,写出稀盐酸滴在石灰石上所发生反应的离子方程式;将足量盐酸溶液逐渐加入到100g硫酸钡和碳酸钡组成的固体混合物中,直到气体不再产生为止,蒸干后称量所得固体质量增加1.1克,则原混合物中硫酸钡的质量分数为。20. 从微观角度认识和观察物质世界是学习化学的重要思维方法。如图是某反应的微观示意图。(资料:已知HClO为一种酸)
19. 初中化学中,我们学习了酸和碱发生中和反应的实质是 。像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式,难溶的物质、气体和水等仍用化学式表示,写出稀盐酸滴在石灰石上所发生反应的离子方程式;将足量盐酸溶液逐渐加入到100g硫酸钡和碳酸钡组成的固体混合物中,直到气体不再产生为止,蒸干后称量所得固体质量增加1.1克,则原混合物中硫酸钡的质量分数为。20. 从微观角度认识和观察物质世界是学习化学的重要思维方法。如图是某反应的微观示意图。(资料:已知HClO为一种酸) (1)、写出氯元素在反应前和反应后的化合价。(2)、以上反应生成的酸能与碱发生中和反应。如果将氯气通入氢氧化钠溶液中可制取 NaClO(84消毒液的主要成分),请写出该反应的化学方程式。21. 如图是实验室制取和收集气体的常见实验装置图,请根据图示回答下列问题:
(1)、写出氯元素在反应前和反应后的化合价。(2)、以上反应生成的酸能与碱发生中和反应。如果将氯气通入氢氧化钠溶液中可制取 NaClO(84消毒液的主要成分),请写出该反应的化学方程式。21. 如图是实验室制取和收集气体的常见实验装置图,请根据图示回答下列问题: (1)、某气体只能用装置B和D来制取,且制取时发生复分解反应,请写出化学方程式。(2)、若用装置E干燥该气体,气体从a端通入,请在E图中将该装置补画完整。22. 向盐酸和氯化钙的混合液中逐滴滴入碳酸钠溶液,并用pH传感器连续监测,得到pH随时间的变化曲线如图所示。(注:碳酸钠溶液显碱性)
(1)、某气体只能用装置B和D来制取,且制取时发生复分解反应,请写出化学方程式。(2)、若用装置E干燥该气体,气体从a端通入,请在E图中将该装置补画完整。22. 向盐酸和氯化钙的混合液中逐滴滴入碳酸钠溶液,并用pH传感器连续监测,得到pH随时间的变化曲线如图所示。(注:碳酸钠溶液显碱性) (1)、所在原混合溶液中滴入少量紫色石蕊溶液,则AB段溶液颜色变化。(2)、图中C点溶液所含的溶质为。(3)、图中DE段pH上升的原因是。23. 铁是目前世界上使用最多的金属。(1)、钢和生铁都是铁的合金,二者的性能不同,其主要原因是;工业上经常用稀硫酸除铁锈的化学方程式为。(2)、将5.6g铁粉样品(杂质是锌或镁的一种)与足量的盐酸反应,可生成0.19g氢气。现向Al(NO3)3和AgNO3的混合溶液中加入一定质量的该铁粉样品充分反应。混合溶液中一定发生的化学方程式为;反应前后溶液的质量将(填写“变大”“不变”“变小”)。24. 如图是实验室制取CO并模拟炼铁的微型实验装置图。实验室制取CO的原理是甲酸(HCOOH)在浓硫酸催化下受热分解生成一氧化碳和水。已知甲酸具有挥发性,请据此回答下列问题:
(1)、所在原混合溶液中滴入少量紫色石蕊溶液,则AB段溶液颜色变化。(2)、图中C点溶液所含的溶质为。(3)、图中DE段pH上升的原因是。23. 铁是目前世界上使用最多的金属。(1)、钢和生铁都是铁的合金,二者的性能不同,其主要原因是;工业上经常用稀硫酸除铁锈的化学方程式为。(2)、将5.6g铁粉样品(杂质是锌或镁的一种)与足量的盐酸反应,可生成0.19g氢气。现向Al(NO3)3和AgNO3的混合溶液中加入一定质量的该铁粉样品充分反应。混合溶液中一定发生的化学方程式为;反应前后溶液的质量将(填写“变大”“不变”“变小”)。24. 如图是实验室制取CO并模拟炼铁的微型实验装置图。实验室制取CO的原理是甲酸(HCOOH)在浓硫酸催化下受热分解生成一氧化碳和水。已知甲酸具有挥发性,请据此回答下列问题: (1)、氢氧化钠固体的作用是什么?(2)、写出B装置中Fe3O4发生反应的化学方程式。(3)、使用该装置的优点有哪些?(写出一条即可)
(1)、氢氧化钠固体的作用是什么?(2)、写出B装置中Fe3O4发生反应的化学方程式。(3)、使用该装置的优点有哪些?(写出一条即可)三、推断题
-
25. 有A、B、C、D、E是初中五种常见的物质,它们的部分反应和转化关系如图所示(“一”表示反应关系,“→”表示转化关系)。其中B是胃酸的主要成分;C广泛应用于玻璃、造纸、纺织等的生产;A和E都属于碱。

写出D的一种用途;写出A物质的一种俗称;D转化C的化学方程式为。
四、流程题
