福建省三明市永安市2020年中考化学一模试卷
试卷更新日期:2021-04-20 类型:中考模拟
一、单选题
-
1. 福建省景色秀美,保护环境,人人有责。下列做法中,不会造成环境污染的是( )A、武夷山上扔塑料袋 B、大金湖中排工业污水 C、九龙江水里养鱼虾 D、鼓浪屿上烧生活垃圾2. 如下图所示实验操作中,正确的是()A、
 取用粉末状固体
B、
取用粉末状固体
B、 塞紧橡皮塞
C、
塞紧橡皮塞
C、 测溶液酸碱性
D、
测溶液酸碱性
D、 过滤操作
3. 下列四种粒子的结构示意图中,说法正确的是()
过滤操作
3. 下列四种粒子的结构示意图中,说法正确的是() A、它们表示四种不同的元素 B、①③④表示的元素都是非金属元素 C、②表示的元素在化合物中通常显+2价 D、①④表示的是阳离子4. 英国《独立报》说,中国“龙江二号”卫星拍摄的地月照片,可能是迄今为止最棒的地月同框合影。月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛元素的化合价为( )A、+5 B、+4 C、+3 D、+25. 苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为Cl9Hl9N7O6。下列有关叶酸的说法中正确的是( )A、叶酸的相对分子质量为441 g B、叶酸中氮元素的质量分数大于氧元素的质量分数 C、叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6 D、叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成6. 下列关于物质性质与用途的叙述,错误的是( )A、纯碱与火碱反应,可用于工业制食盐 B、二氧化碳用于灭火,是利用它的物理性质和化学性质 C、“洗洁精”有乳化作用,可用来洗涤餐具上的油污 D、铜具有优良的导电性能,可用于制作电器元件7. 下列物质不属于有机化合物的是( )A、
A、它们表示四种不同的元素 B、①③④表示的元素都是非金属元素 C、②表示的元素在化合物中通常显+2价 D、①④表示的是阳离子4. 英国《独立报》说,中国“龙江二号”卫星拍摄的地月照片,可能是迄今为止最棒的地月同框合影。月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。钛铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛元素的化合价为( )A、+5 B、+4 C、+3 D、+25. 苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为Cl9Hl9N7O6。下列有关叶酸的说法中正确的是( )A、叶酸的相对分子质量为441 g B、叶酸中氮元素的质量分数大于氧元素的质量分数 C、叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6 D、叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成6. 下列关于物质性质与用途的叙述,错误的是( )A、纯碱与火碱反应,可用于工业制食盐 B、二氧化碳用于灭火,是利用它的物理性质和化学性质 C、“洗洁精”有乳化作用,可用来洗涤餐具上的油污 D、铜具有优良的导电性能,可用于制作电器元件7. 下列物质不属于有机化合物的是( )A、 乙烯(C2H4)
B、
乙烯(C2H4)
B、 足球烯(C60)
C、
足球烯(C60)
C、 甲烷(CH4)
D、
甲烷(CH4)
D、 丙氨酸(C3H7O2N)
8. 如图,若要使红墨水倒吸,则锥形瓶中加入的固体和液体可能是( )
丙氨酸(C3H7O2N)
8. 如图,若要使红墨水倒吸,则锥形瓶中加入的固体和液体可能是( ) A、蔗糖和水 B、锌和稀盐酸 C、生石灰和水 D、铁粉和食盐水9. 下列实验方法不能达到实验目的的是( )
A、蔗糖和水 B、锌和稀盐酸 C、生石灰和水 D、铁粉和食盐水9. 下列实验方法不能达到实验目的的是( )选项
实验目的
实验方法
A
证明NaOH溶液中含有Na2CO3
滴加无色酚酞试剂
B
除去 CO2中少量CO
将混合气体通过足量灼热的CuO
C
鉴别石灰水和NaOH溶液
加入适量的碳酸钠溶液
D
比较 Fe、Cu、Ag的金属活动性
将 Fe和 Ag分别放入 CuSO4溶液中
A、A B、B C、C D、D10. 常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌。如图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见表)。下列实验与图象对应关系合理的是( )
M
N
y
A
水
浓硫酸
溶液的温度
B
水
氢氧化钠溶液
溶液的pH
C
饱和氯化钠溶液
氯化钠
溶液的溶质质量分数
D
硫酸铜
铁粉
溶液的质量
A、A B、B C、C D、D二、填空题
-
11. 化学与生活息息相关。
 (1)、自热米饭是一种快餐食品。请根据上图及表信息,回答下列问题:
(1)、自热米饭是一种快餐食品。请根据上图及表信息,回答下列问题:①从“自热米饭的营养成分表”看,表中没有标出的人体必须的营养素是;
②图1包装材料一般是铝箔。铝可以压制成铝箔,说明铝具有良好的性。
③该自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反应的化学方程式为。
(2)、良好的家居环境带来美好的生活。
①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲醛、苯等有毒气体,这是利用活性炭的性。
②如图,“火立熄” 是一种新型的家用灭火用品。“火立熄” 接触到火焰3- 5秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使火焰熄灭。“火立 熄”的灭火原理是。
12. 如图是A、B、C三种固体物质的溶解度曲线图。请结合图示回答下列问题: (1)、t2℃ 时,A,B,C三种物质的溶解度由大到小的关系是。(2)、将A的不饱和溶液转变成饱和溶液的方法是(写一种)。(3)、A中含有少量B,分离得到较纯的A的步骤是溶解、、过滤、洗涤、干燥。(4)、t3℃ 时,将30 g A物质加入到50 g水中,充分溶解后,所得溶液中溶质的质量分数是。(5)、将t1℃ 时A和C的饱和溶液同时升高一定温度后,所得溶液中溶质的质量分数的大小关系是。13. 当前,世界已经迈向了“低碳”时代,选择“低碳”既是一种生活方式也是一种生存责任。福州市公交系统适应形势发展,推广使用节能减排的双燃料公交车,这种公交车是以天然气为主要燃料。下图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图。请根据示意图回答下列问题:
(1)、t2℃ 时,A,B,C三种物质的溶解度由大到小的关系是。(2)、将A的不饱和溶液转变成饱和溶液的方法是(写一种)。(3)、A中含有少量B,分离得到较纯的A的步骤是溶解、、过滤、洗涤、干燥。(4)、t3℃ 时,将30 g A物质加入到50 g水中,充分溶解后,所得溶液中溶质的质量分数是。(5)、将t1℃ 时A和C的饱和溶液同时升高一定温度后,所得溶液中溶质的质量分数的大小关系是。13. 当前,世界已经迈向了“低碳”时代,选择“低碳”既是一种生活方式也是一种生存责任。福州市公交系统适应形势发展,推广使用节能减排的双燃料公交车,这种公交车是以天然气为主要燃料。下图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图。请根据示意图回答下列问题: (1)、上述反应的物质中,属于氧化物的是(填序号)。(2)、上述反应前后,保持不变的微粒是。(3)、写出上述反应的化学方程式。(4)、上述反应属于反应(填“分解”“化合”“氧化”之一)。
(1)、上述反应的物质中,属于氧化物的是(填序号)。(2)、上述反应前后,保持不变的微粒是。(3)、写出上述反应的化学方程式。(4)、上述反应属于反应(填“分解”“化合”“氧化”之一)。三、流程题
-
14. 海水晒制得到的粗盐中除NaCl外,还含有Na2SO4、MgCl2、CaCl2、泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
 (1)、步骤Ⅰ和步骤Ⅱ除加入必要的试剂之外都还涉及相同的实验操作,该操作所需的玻璃仪器是漏斗、烧杯、。(2)、为了除去混合液1中的可溶性杂质Na2SO4、MgCl2、CaCl2 , 应按顺序依次加入过量的BaCl2、NaOH、Na2CO3 , 分别写出除去杂质Na2SO4、MgCl2的化学方程式、。(3)、步骤Ⅱ中加入过量Na2CO3溶液的目的是。(4)、混合液2中主要成分是NaCl,请设计实验检验该溶液中含有的另外两种溶质。(简要写出实验步骤及现象)(5)、步骤Ⅲ中应加入过量(填药品名称),其目的是 , 写出有关反应的化学方程式(任写一个即可)。(6)、将已配好的50 g质量分数为9%的氯化钠溶液变成质量分数为0.9%的生理盐水,需要加水的质量是g。
(1)、步骤Ⅰ和步骤Ⅱ除加入必要的试剂之外都还涉及相同的实验操作,该操作所需的玻璃仪器是漏斗、烧杯、。(2)、为了除去混合液1中的可溶性杂质Na2SO4、MgCl2、CaCl2 , 应按顺序依次加入过量的BaCl2、NaOH、Na2CO3 , 分别写出除去杂质Na2SO4、MgCl2的化学方程式、。(3)、步骤Ⅱ中加入过量Na2CO3溶液的目的是。(4)、混合液2中主要成分是NaCl,请设计实验检验该溶液中含有的另外两种溶质。(简要写出实验步骤及现象)(5)、步骤Ⅲ中应加入过量(填药品名称),其目的是 , 写出有关反应的化学方程式(任写一个即可)。(6)、将已配好的50 g质量分数为9%的氯化钠溶液变成质量分数为0.9%的生理盐水,需要加水的质量是g。四、推断题
-
15. 已知甲、乙、丙、丁分别是初中化学中常见的四种不同类别的物质,相邻两种物质可发生化学反应,生成A、B、C、D四种物质(部分生成物已略)。其中乙是应用最广的金属,丙是蓝色溶液,丁中含有钠离子,B是气体,D是不溶性碱。
 (1)、写出乙的化学式 ;(2)、若C是一种盐,则其溶液的颜色为 ;(3)、甲所属的物质类型为 (填“酸”“碱”“盐”或“氧化物”);(4)、若丙由三种元素组成,试写出丙与丁反应的化学方程式 ;
(1)、写出乙的化学式 ;(2)、若C是一种盐,则其溶液的颜色为 ;(3)、甲所属的物质类型为 (填“酸”“碱”“盐”或“氧化物”);(4)、若丙由三种元素组成,试写出丙与丁反应的化学方程式 ;五、实验题
-
16. 根据下列装置图,回答有关问题:
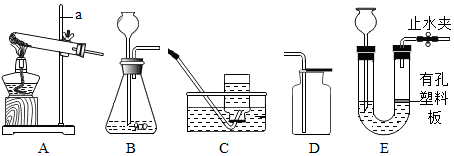 (1)、写出标号仪器的名称:a。(2)、实验室制取较纯净的氧气时可以选择的装置是(填字母),其化学方程式为。检验气体是否收集满的方法是。(3)、实验室用B、D装置组合来制取二氧化碳,其化学方程式为。若将发生装置由B改为E,其优点是。17. 为探究工业上制硫酸接触室中的反应,了解酸雨形成的原理,设计如下图所示装置。
(1)、写出标号仪器的名称:a。(2)、实验室制取较纯净的氧气时可以选择的装置是(填字母),其化学方程式为。检验气体是否收集满的方法是。(3)、实验室用B、D装置组合来制取二氧化碳,其化学方程式为。若将发生装置由B改为E,其优点是。17. 为探究工业上制硫酸接触室中的反应,了解酸雨形成的原理,设计如下图所示装置。(查阅资料)
三氧化硫会与水反应生成硫酸,在室温下会产生酸雾,类似浓盐酸挥发时产生的白雾。二氧化硫与二氧化碳具有某些相似的化学性质,如能与氢氧化钠溶液反应、能使澄清石灰水变浑浊等。
 (1)、装置①中浓硫酸的作用有:能通过观察气泡,调节气体的流速;能使二氧化硫与氧气充分混合;同时还能起到的作用。(2)、装置②中发生反应的化学方程式为。(3)、实验过程中,观察到装置③中的锥形瓶内有白色沉淀生成,试写出装置③中锥形瓶内发生的有关反应的化学方程式、。装置③中锥形瓶浸入冰水浴的原因是。(4)、装置⑤中石灰水没有变浑浊,说明。(5)、反应结束后还需通入N2的原因是。(6)、一定条件下,已知通入SO2的体积和密度,若要测定该条件下有多少克的SO2转化成H2SO4 , 实验时还需要测定的数据是。
(1)、装置①中浓硫酸的作用有:能通过观察气泡,调节气体的流速;能使二氧化硫与氧气充分混合;同时还能起到的作用。(2)、装置②中发生反应的化学方程式为。(3)、实验过程中,观察到装置③中的锥形瓶内有白色沉淀生成,试写出装置③中锥形瓶内发生的有关反应的化学方程式、。装置③中锥形瓶浸入冰水浴的原因是。(4)、装置⑤中石灰水没有变浑浊,说明。(5)、反应结束后还需通入N2的原因是。(6)、一定条件下,已知通入SO2的体积和密度,若要测定该条件下有多少克的SO2转化成H2SO4 , 实验时还需要测定的数据是。六、计算题
-
18. 过氧化钙(CaO2)是一种环境友好的化工原料,工农业生产中用作漂白剂、种子消毒剂及鱼类运输时的制氧剂等。过氧化钙与水反应方程式为:2CaO2+2H2O=2Ca(OH)2+O2↑。某同学把20g不纯的过氧化钙样品(杂质不与水反应)加入到盛有50g水(足量)的烧杯中,完全反应后,称量烧杯内物质的总质量为66.8g。请计算:(1)、生成氧气g;(2)、该样品中过氧化钙的质量分数。(根据化学方程式计算)
-
-