初中化学人教版全真模拟试卷二
试卷更新日期:2021-04-16 类型:中考模拟
一、单选题
-
1. 下列关于物质的变化或性质的描述中,对应正确的是( )A、牛奶变酸——物理变化 B、H2CO3容易分解——化学性质 C、西瓜榨汁——化学变化 D、铅笔芯的导电性——化学性质2. 绿色化学”是21世纪化学发展的主导方向。“绿色化学”要求从根本上消灭污染,是一门能彻底阻止污染产生的科学。它包括“绿色生产”和“绿色销毁”等内容。2008年某地在整顿音像市场的活动中查获了一批盗版光盘,并进行了“绿色销毁”。下列属于“绿色销毁”的是( )A、泼上汽油焚烧 B、倾倒入江中 C、碾压粉碎后回收再利用 D、深埋于土中3. 下列图标属于节约用水标志的是( )A、
 B、
B、 C、
C、 D、
D、 4. 有机合成材料让人类的发展前进了一大步,下列物品的材质不属于有机合成材料的是( )A、天然橡胶为原料制成的乳胶枕芯 B、富有弹性的尼龙丝袜 C、“不碎玻璃”中的聚醋酸乙烯酯夹层 D、可降解塑料手术缝合线5. 利用如图所示装置,能完成实验室制取气体的是( )
4. 有机合成材料让人类的发展前进了一大步,下列物品的材质不属于有机合成材料的是( )A、天然橡胶为原料制成的乳胶枕芯 B、富有弹性的尼龙丝袜 C、“不碎玻璃”中的聚醋酸乙烯酯夹层 D、可降解塑料手术缝合线5. 利用如图所示装置,能完成实验室制取气体的是( )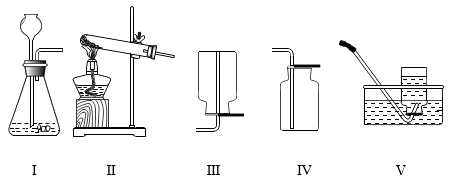 A、用Ⅱ、Ⅲ制取氧气 B、用Ⅱ、Ⅳ制取氢气 C、用Ⅰ、Ⅳ制取氧气 D、用Ⅰ、Ⅲ制取二氧化碳6. 能源问题是当今世界三大问题之一,下列有关能源的叙述中不正确的是( )A、乙醇汽油中添加的乙醇(C2H5OH)属于可再生能源 B、人类通过化石燃料获得能量的过程是物理变化 C、将煤球制成“蜂窝煤”是为了增大与空气的接触面积,使其燃烧更充分 D、我国南海海底储藏了大量“可燃水”,它将成为替代化石燃料的新能源7. 下图是某密闭容器中物质变化过程的微观示意图(“
A、用Ⅱ、Ⅲ制取氧气 B、用Ⅱ、Ⅳ制取氢气 C、用Ⅰ、Ⅳ制取氧气 D、用Ⅰ、Ⅲ制取二氧化碳6. 能源问题是当今世界三大问题之一,下列有关能源的叙述中不正确的是( )A、乙醇汽油中添加的乙醇(C2H5OH)属于可再生能源 B、人类通过化石燃料获得能量的过程是物理变化 C、将煤球制成“蜂窝煤”是为了增大与空气的接触面积,使其燃烧更充分 D、我国南海海底储藏了大量“可燃水”,它将成为替代化石燃料的新能源7. 下图是某密闭容器中物质变化过程的微观示意图(“ ”代表碳原子,“
”代表碳原子,“  "代表氧原孔)。有关说法正确的是( )
"代表氧原孔)。有关说法正确的是( ) 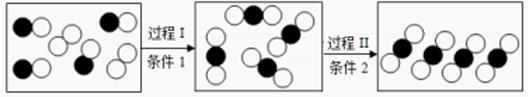 A、过程Ⅰ反应类型为化合反应 B、过程Ⅱ发生了化学变化 C、该反应中的物质均为氧化物 D、参加反应的物质分子个数比为1:18. 下列实验操作、现象或变化、结论对应关系正确的是( )
A、过程Ⅰ反应类型为化合反应 B、过程Ⅱ发生了化学变化 C、该反应中的物质均为氧化物 D、参加反应的物质分子个数比为1:18. 下列实验操作、现象或变化、结论对应关系正确的是( )选项
实验操作
现象或变化
结论
A
取少量井水,加入适量肥皂水,振荡
产生大量浮渣
井水为硬水
B
称量镁条在空气中燃烧前后质量
质量减少
不遵循质量守恒定律
C
把引燃的细铁丝伸进盛有氧气的集气瓶中
剧烈燃烧
氧气有可燃性
D
用拇指堵住收集了CH4的试管口,靠近火焰,移开拇指点火
发出尖锐爆鸣声
试管中CH4纯净
A、A B、B C、C D、D9. 如图是微信热传的“苯宝宝表情包”,苯(化学式C6H6)、六氯苯(化学式C6Cl6)都是重要的化工原料,下列有关说法正确的是( )。 A、六氯苯的含碳量比苯的含碳量高 B、六氯苯中碳、氯两种元素的质量比为1:1 C、苯由6个碳原子和6个氢原子构成 D、苯中氢元素的质量分数为7.7%10. 物质是由微粒构成的。从分子的角度解释下列事实错误的是( )
A、六氯苯的含碳量比苯的含碳量高 B、六氯苯中碳、氯两种元素的质量比为1:1 C、苯由6个碳原子和6个氢原子构成 D、苯中氢元素的质量分数为7.7%10. 物质是由微粒构成的。从分子的角度解释下列事实错误的是( )选项
事实
解释
A
1个氢分子的质量约为
分子的质量很小
B
把O2压缩到钢瓶中
分子的体积变小
C
H2与O2的化学性质不同
分子的种类不同
D
1滴水中大约有 个水分子
分子的体积很小
A、A B、B C、C D、D11. 除去下列物质中的少量杂质,选用的试剂及操作方法均正确的是( )选项
物质(括号内为杂质)
试剂
操作方法
A
CO2(HCl)
适量NaOH溶液
洗气
B
NaOH(Na2CO3)
适量CaCl2溶液
过滤、蒸发结晶
C
CO2(CO)
足量O2
点燃
D
KCl(MnO2)
足量H2O
溶解、过滤、蒸发
A、A B、B C、C D、D12. MgSO4和Na2CO3的溶解度表及溶解度曲线如下。下列说法错误的是( )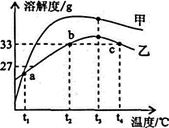
温度/℃
20
30
40
50
60
70
80
溶解度
MgSO4
25.1
28.2
30.8
32.9
34.3
35.0
34.9
S/g
Na2CO3
21.5
39.7
49.0
48.5
46.0
45.2
43.9
A、物质甲是Na2CO3 B、a点的溶解度在25.1g~27g之间 C、b点、c点对应的乙的溶液,溶质质量分数一定相等 D、可在t2℃配出溶质质量分数为33%的乙溶液.13. 如图是 A,B,C三种物质的溶解度曲线,下列叙述不正确的是( )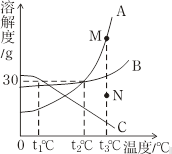 A、当温度为t3℃时,物质溶解度关系是 A>B>C B、将A,B,C的饱和溶液从t3℃降到t2℃,溶液中均有固体析出 C、若要将N点的A溶液转变为M点的A溶液,可在恒温条件下加入A物质 D、t1℃时65gC的饱和溶液中含有C物质15g14. 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
A、当温度为t3℃时,物质溶解度关系是 A>B>C B、将A,B,C的饱和溶液从t3℃降到t2℃,溶液中均有固体析出 C、若要将N点的A溶液转变为M点的A溶液,可在恒温条件下加入A物质 D、t1℃时65gC的饱和溶液中含有C物质15g14. 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )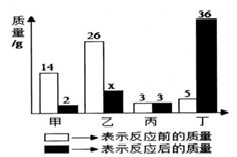 A、x的值是7 B、参加反应的甲和乙的质量比为7: 13 C、丁一定是化合物 D、丙可能是该反应的催化剂15. 下列图像不能正确反映对应变化关系的是( )A、装有定量氧气的密闭容器内燃烧木炭
A、x的值是7 B、参加反应的甲和乙的质量比为7: 13 C、丁一定是化合物 D、丙可能是该反应的催化剂15. 下列图像不能正确反映对应变化关系的是( )A、装有定量氧气的密闭容器内燃烧木炭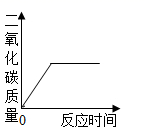 B、加热一定量高锰酸钾固体
B、加热一定量高锰酸钾固体 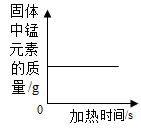 C、加热氯酸钾制氧气
C、加热氯酸钾制氧气 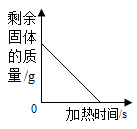 D、实验室利用双氧水制取氧气
D、实验室利用双氧水制取氧气 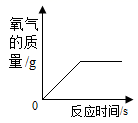
二、填空题
-
16. 新型冠状病毒蔓延期间,为做好自我保护,外出最重要的防护措施是佩戴符合要求的口罩。在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。(1)、①佩戴口罩预防病毒的原理相当于化学实验中的操作。
②活性炭口罩能有效阻隔空气中的氨、苯、甲醛等有害气体,其功能比普通口罩强大,原因是活性炭具有性。
③生产N95口罩的主要原料是聚丙烯,它属于材料。
(2)、在抗击新型冠状病毒肺炎期间做好消毒至关重要,常用的消毒剂有酒精、过氧乙酸和“84”消毒液等。①医用酒精是75%酒精溶液,其溶剂是 , 在室内不要喷洒高浓度的酒精,因为挥发出的酒精蒸汽遇到明火易发生燃烧和爆炸,酒精完全燃烧的化学方程式。
②过氧乙酸具有强氧化性,能让病毒表面的蛋白质外壳变质,致使病毒死亡。强氧化性属于(填物理或者化学)性质。要配制溶质质量分数为0.5%的过氧乙酸溶液1000g对教室进行消毒,需要质量分数为16%的过氧乙酸溶液g,配制好的溶液可以用
(填“塑料桶”或“铁桶”)盛装。
③ “84”消毒液的有效成分次氯酸钠(NaClO)属于(填序号)
A.酸 B.碱 C.盐 D.氧化物
17. 建立宏观、微观与化学符号的联系是化学学科的特点。(1)、写出电解水反应的化学方程式。(2)、一定条件下,水在密闭容器里冷却的过程中,温度和时间的关系如图所示。①、②、③表示水在不同时刻的存在状态,下列有关判断正确的是。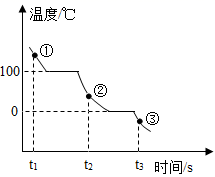
A水分子间的间隔:①>③
B水分子的运动速率:②>①
C状态③的水分子静止不动
D①→②发生了化学变化
(3)、2020年12月3日,我国“嫦娥五号”成功发射,显示我国科技实力的飞速发展。我国空间站“天宫”内的“空气”与地球上的空气组成基本一致,已知同温同压下,相同体积的气体含有相同数目的分子,“空气”中O2与N2的分子个数比约为。(4)、CO气体在空气中完全燃烧生成CO2气体,CO2气体在一定条件下会转变成干冰。①根据给出的O2和CO2气体的微观示意图,补充CO气体和干冰的微观示意图、。
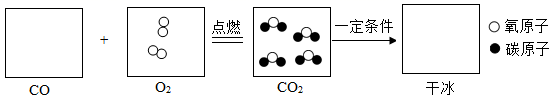
②参加反应的CO与O2的质量最简比为。
(5)、2020年5月,科学家在《Science》期刊上首次报道了原子与分子的“最简单”反应,存在两种路径,并用先进技术手段拍下了该反应的影像资料。其中一种路径如图所示。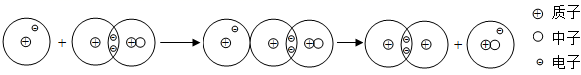
此“最简单”反应中,
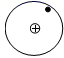 表示H原子,
表示H原子, 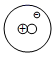 表示D原子,D原子核中有个质子,此反应中涉及的元素种类有种。该反应可表示为H+→ H2+。
表示D原子,D原子核中有个质子,此反应中涉及的元素种类有种。该反应可表示为H+→ H2+。三、实验探究题
-
18. 初步学习运用简单的装置和方法制取某些气体,是初中学生的化学实验技能应达到的要求。(1)、某学习小组将实验室制取常见气体的相关知识归纳如下:
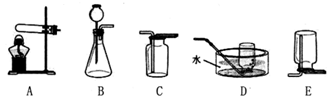
气体
方法(或原理)
发生装置
收集装置
O2
方法1:加热混有二氧化锰的氯酸钾固体。反应中二氧化锰所起的作用是。
均可选择A装置(可根据需要添加棉花)
均可选择装置(填标号)
方法2:加热(填化学式)
方法3:分解过氧化氢溶液,化学方程式为。
均可选择装置(填标号)
CO2
用稀盐酸和大理石反应来制取
(2)、该小组将制取的O2和CO2 (各一瓶)混淆了,设计了如下方案进行区分。方案
现象
结论
方案1:将带火星的木条分别伸入两个集气瓶中
若带火星的木条
则该瓶气体是O2
方案2:向两个集气瓶中分别滴入少量的溶液,振荡
若溶液变浑浊
则该瓶气体是CO2
方案3:向两个集气瓶中分别倒入少量的水,振荡后再滴加几滴紫色石蕊溶液
若紫色石蕊溶液变为色
则该瓶气体是CO2
……
……
……
(3)、制取气体的过程包括:a.选择制取装置;b.验证所得气体;c.明确反应原理。据此,该小组总结出实验室里制取气体的一般思路为 (填“甲”或“乙”或“丙”)。甲、a→b→c
乙、b→a→c
丙、c→a→b
19. 某实验小组将少量氢化钙(CaH2)溶于水,形成了无色透明的溶液,再向其中加入碳酸钠溶液,有沉淀产生,经过滤后得到滤渣和滤液。最后进行滤渣验证和滤液溶质成分的探究。(1)、[查阅资料]氢化钙在常温下能与水反应生成氢氧化钙和氢气,写出该反应的化学方程式:。(2)、[交流验证]滤渣只能是碳酸钙,用盐酸验证此滤渣的化学方程式为:。(3)、[提出问题]滤液中溶质的成分是什么?[猜想假设]猜想一:NaOH
猜想二:NaOH和Na2CO3
猜想三:NaOH和
猜想四:NaOH、Na2CO3和Ca(OH)2
[讨论分析]经过讨论认为最不合理的是猜想 , 原因是。
(4)、[实验与结论]实验步骤
现象
结论
步骤Ⅰ:取少量滤液,向其中加入足量盐酸
猜想二不成立
步骤Ⅱ:另取少量滤液,向其中滴入适量Na2CO3溶液现象
产生白色沉淀
猜想成立
(5)、[拓展延伸]在分析反应后所得物质的成分时,除考虑生成物外,还需考虑 。四、综合题
-
20.(1)、Ⅰ.高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:

操作Ⅰ和操作Ⅱ都要用到的玻璃棒,玻璃棒的作用是。
(2)、反应②的化学方程式是。(3)、反应③的基本反应类型是。(4)、检验滤液Ⅱ中阳离子的操作是:取样,滴加溶液,微热,将湿润的红色石蕊试纸放在试管口。(5)、Ⅱ.下图表示元素的化合价与物质类别的关系,“→”表示物质之间可以转化。A,B,C,D,E 是初中化学所学物质,分别由 Fe、H、O、Cl 中的一种、两种或三种元素组成,已知:难溶性碱加热时会生成对应的氧化物。

Ⅰ题中的产物Fe2O3是上图中的物质(填序号)。
(6)、B→A的转化对应Ⅰ题中的反应(填序号)。(7)、C→B的另一种生成物的化学式是。(8)、除了图中所示的转化关系外,还存在哪些转化关系,请写出其中一道对应的化学方程式。五、计算题
-
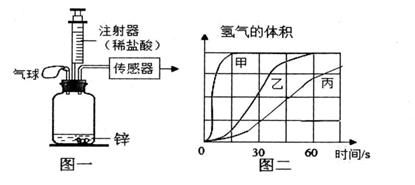
21. 某实验小组为了研究在其他条件相同时,反应物的接触面积对反应速率的影响。实验装置如图一所示, 他们用等质量不同形状的金属锌(所用金属锌均不含任何杂质)和稀盐酸反应(见下表),实验中使用传感器装置测算生成氢气的体积,绘制氢气体积随时间变化的曲线如图二所示。
实验编号
药品
Ⅰ
6.5g锌块、150g 含HCl7.3%足量的稀盐酸
Ⅱ
6.5g锌粒、150g 含HCl7.3%足量的稀盐酸
Ⅲ
6.5g锌粉、150g 含HCl7.3%足量的稀盐酸
(1)、小组按图一装置进行的三个实验中,实验(填实验编号)反应速率最慢;在图二中的曲线(填“甲”、“乙”或“丙”)代表的是实验Ⅲ,从曲线甲、乙、丙得出探究结论是:。(2)、分析表中锌和稀盐酸的用量可知:(填物质名称)反应消耗完;(3)、请计算以上任意一组实验中生成氢气的质量(写出具体计算过程)。(4)、分析上表数据,请在图三中画出在6.5g锌中加入0~150 g稀盐酸过程中,产生氢气质量对应的变化曲线图,并标注必要的数值。
-