初中化学人教版全真模拟试卷一
试卷更新日期:2021-04-16 类型:中考模拟
一、单选题
-
1. 下列实验室中的交流,属于化学变化的是( )A、试管:“同学们不爱我,碎了我的玻璃心!” B、铁架台:“我好难受啊!我在潮湿的空气中生锈了!” C、酒精灯:“帽子哪里去了?我的燃料越来越少了” D、滤纸:“过滤时为什么搅拌?我都被划破了!”2. 2020年5月12日是第十二个全国防灾减灾日,为预防森林火灾,应张贴的标志是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列对一些事实的解释正确的是( )
3. 下列对一些事实的解释正确的是( )选项
事实
解释
A
加热氯酸钾时误将高锰酸钾加入后,反应速率加快了
高锰酸钾是该反应的催化剂
B
600升氧气被压缩在40升的钢瓶中
分子之间有一定间隔
C
变瘪的乒乓球放入热水中能鼓起来
分子大小随温度改变而改变
D
二氧化碳不支持燃烧
二氧化碳的密度比空气大
A、A B、B C、C D、D4. 据悉,2020年8月4日发生的黎巴嫩大爆炸可能由港口库存的化学品硝酸铵(NH4NO3)引起。以下关于NH4NO3的说法正确的是( )A、NH4NO3中N、H、O三种元素的质量比为7:1:12 B、NH4NO3中含有NO3- , NO3-中氮元素化合价为+6价 C、NH4NO3中N元素质量分数的计算式为 ×100% D、NH4NO3受热发生分解反应,可能产生SO2气体5. 分类是化学学习和研究的重要方法之一,下列分类正确的是( )A、纯净物:洁净的空气、H2O2 溶液、冰水混合物…… B、构成物质的微粒有:分子、原子、离子…… C、可在酒精灯上加热的仪器:试管、烧杯、集气瓶…… D、物理性质包括:溶解性、挥发性、可燃性……6. 对于人体,铁是不可缺少的微量元素。铁元素的相关信息如下图所示,下列有关铁的说法正确的是( )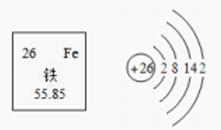 A、相对原子质量为55.85g B、铁原子的核电荷数、质子数都为26 C、在化学变化中容易失去最外层电子形成Fe+2 D、铁在氧气中燃烧生成氧化铁7. 如图是某化学反应的微观模型示意图。据此分析正确的是( )
A、相对原子质量为55.85g B、铁原子的核电荷数、质子数都为26 C、在化学变化中容易失去最外层电子形成Fe+2 D、铁在氧气中燃烧生成氧化铁7. 如图是某化学反应的微观模型示意图。据此分析正确的是( )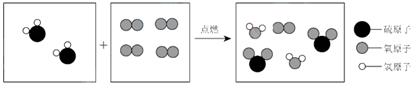 A、参加反应的两种物质的分子个数比1:2 B、生成物中有三种物质,既有单质又有化合物 C、化学变化过程中,分子的种类不一定发生改变 D、此反应不属于化合反应也不属于置换反应8. “见微知著”,研究微观是化学学习中重要的内容,有以下表述.其中正确的有( )
A、参加反应的两种物质的分子个数比1:2 B、生成物中有三种物质,既有单质又有化合物 C、化学变化过程中,分子的种类不一定发生改变 D、此反应不属于化合反应也不属于置换反应8. “见微知著”,研究微观是化学学习中重要的内容,有以下表述.其中正确的有( )①氯气:Cl2
②由三个氧原子构成的臭氧分子:3O;
③右图粒子结构示意图表示的粒子:S2+
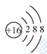
④两个铁离子: 2Fe2+;
⑤导电性最好的金属: Ag;
⑥+2价的镁元素:Mg+2
A、②④⑤ B、①⑤ C、①③⑤ D、①④⑥9. 归纳推理是学习化学的重要方法之一。下列有关事实的推理,以及结论合理的是( )A、铝制品的耐腐蚀性比铁制品强——铝的化学性质没有铁活泼 B、CO和CO2的化学性质有很大差异——CO2与CO的分子构成不同 C、金刚石和石墨均是由碳元素组成的单质——金刚石和石墨是同一种物质 D、用镁条测定空气中氧气含量,实验结果大于1/5——空气中氧气的含量大于1/510. 如图为a、b、c三种固体物质的溶解度曲线,下列说法中正确的是( ) A、将t2℃的a、b、c的饱和溶液降温到t1℃,溶液中溶质质量分数的关系是b>a=c B、t1℃时,将20 g c加入50 g水中充分溶解,得到70 g饱和溶液 C、a溶液中混有少量b , 提纯a物质最好的方法是降温结晶法 D、t2℃时,a溶液的溶质质量分数一定大于b溶液的溶质质量分数11. 某同学对下列4个实验都设计了两种方案,其中方案一、方案二都合理的是( )
A、将t2℃的a、b、c的饱和溶液降温到t1℃,溶液中溶质质量分数的关系是b>a=c B、t1℃时,将20 g c加入50 g水中充分溶解,得到70 g饱和溶液 C、a溶液中混有少量b , 提纯a物质最好的方法是降温结晶法 D、t2℃时,a溶液的溶质质量分数一定大于b溶液的溶质质量分数11. 某同学对下列4个实验都设计了两种方案,其中方案一、方案二都合理的是( )选项
A
B
C
D
实验目的
除去铜粉中少量的铁粉
检验某气体为CO2
鉴别水和过氧化氢(H2O2)溶液
鉴别黄铜(铜锌合金)和黄金
方案一
用磁铁吸引
带火星的木条复燃
看外观
看颜色
方案二
加足量的CuSO4溶液、过滤、干燥
加澄清石灰水
加入MnO2
加入稀盐酸(HCl)
A、A B、B C、C D、D12. 下列有关物质的鉴别、制取、除杂和分离所用的试剂或方法中,正确的是( )选项
实验目的
所用试剂或方法
A
除去CO2气体中少量的CO
点燃
B
实验室制取CO2
块状石灰石和稀硫酸
C
鉴别硬水和软水
加肥皂水,振荡
D
分离白糖和食盐的混合物
加水溶解,过滤
A、A B、B C、C D、D13. 向AgNO3和Mg(NO3)2的混合溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法正确的是( )A、向滤渣中加入稀盐酸,一定有气泡产生; B、滤渣中一定含有Ag、Fe,一定不含Al; C、滤渣中一定含有Ag,可能含有Fe,一定不含Al; D、滤液中一定含有Fe(NO3)2和Mg(NO3)2 , 一定不含AgNO3 , 可能含有Al(NO3)3。14. 下列各组物质不能实现如图所示的转化关系的是( )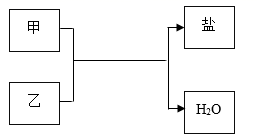
选项
甲
乙
A
Fe2O3
稀硫酸
B
SO3
NaOH溶液
C
稀盐酸
Ca(OH)2溶液
D
稀盐酸
AgNO3溶液
A、A B、B C、C D、D15. 下列图象正确反映对应变化关系的是( )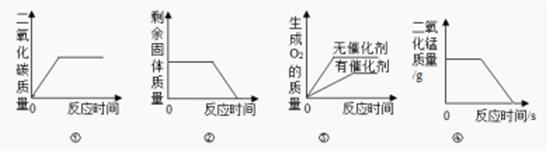 A、图①表示定质量红热木炭在足量氧气中燃烧 B、图②表示加热一定量的高锰酸钾制取氧气 C、图③表示用等量的氯酸钾来制取氧气 D、图④表示过氧化氢和二氧化锰制取氧气
A、图①表示定质量红热木炭在足量氧气中燃烧 B、图②表示加热一定量的高锰酸钾制取氧气 C、图③表示用等量的氯酸钾来制取氧气 D、图④表示过氧化氢和二氧化锰制取氧气二、填空题
-
16. 化学为宏观物质、微观粒子与符号之间构筑了联系的桥梁。请回答下列问题
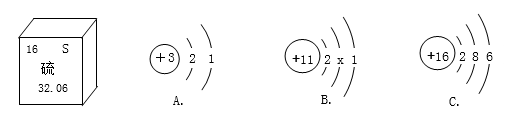 (1)、硫元素的相对原子质量是。(2)、原子结构示意图B中x的数值为 , 它与C粒子构成的物质(填化学式)。(3)、A和B两种粒子的化学性质相似,从原子结构上看是因相同。(4)、工业上使用一种国产低温催化剂生产氢气的反应过程如图所示
(1)、硫元素的相对原子质量是。(2)、原子结构示意图B中x的数值为 , 它与C粒子构成的物质(填化学式)。(3)、A和B两种粒子的化学性质相似,从原子结构上看是因相同。(4)、工业上使用一种国产低温催化剂生产氢气的反应过程如图所示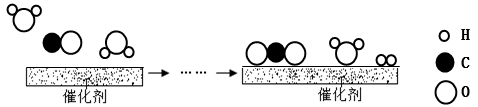
①写出该反的化学方程式。
②该反应的氧化剂是(填写物质的名称)。
(5)、一定条件下,水在密闭容器里的冷却过程中,温度和时间的关系如下图所示。①、②、③表示水在不同时刻的存在状态,下列有关判断正确的是 (填选项字母)。
 A、水分子间的间隔:①>③ B、水分子的运动速率:①>② C、状态③的水分子静止不动 D、①→③过程只发生物理变化17. 2020年6月23日,我国用长征三号乙运载火箭成功发射第55颗北斗导航卫星,化学材料在其中起到了重要作用。(1)、铝合金和钛合金被广泛用于航天工业。一般情况下,铝合金的强度和硬度比纯铝的(填“高”或“低”)。(2)、写出铝与稀盐酸反应的化学方程式 , 其反应类型是。(3)、室温下,钛与水、稀盐酸和稀硫酸均不反应,可判断钛的金属活动性比铝的(填“强”或“弱”)。(4)、卫星发射过程中使用偏二甲肼(C2H8N2)和四氧化二氮作为推进剂。在C2H8N2中,碳、氢元素的质量比为。
A、水分子间的间隔:①>③ B、水分子的运动速率:①>② C、状态③的水分子静止不动 D、①→③过程只发生物理变化17. 2020年6月23日,我国用长征三号乙运载火箭成功发射第55颗北斗导航卫星,化学材料在其中起到了重要作用。(1)、铝合金和钛合金被广泛用于航天工业。一般情况下,铝合金的强度和硬度比纯铝的(填“高”或“低”)。(2)、写出铝与稀盐酸反应的化学方程式 , 其反应类型是。(3)、室温下,钛与水、稀盐酸和稀硫酸均不反应,可判断钛的金属活动性比铝的(填“强”或“弱”)。(4)、卫星发射过程中使用偏二甲肼(C2H8N2)和四氧化二氮作为推进剂。在C2H8N2中,碳、氢元素的质量比为。三、实验探究题
-
18. 图1所示为实验室中常见的气体制备和收集装置。

请回答下列问题:
(1)、实验室用加热氯酸钾和二氧化锰固体制取氧气,应选用发生装置(填字母序号),反应的化学方程式为。若用装置D收集氧气,验满的方法是(2)、实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是(3)、欲使用装置E用排空气法收集二氧化碳,则气体应从(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从(填“a”或“b”)端通入。(4)、已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置(填字母序号)。(5)、将二氧化碳气体通入紫色石蕊试液中,石蕊试液变红色,反应原理用化学方程式表示为(6)、如图2所示,向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳具有的化学性质是19. 某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。这一现象激发起同学们的探究欲望,生成的是什么气体?【提出猜想】从物质组成元素的角度,放出的气体可能是SO2、O2、H2。
【查阅资料】SO2易溶于水,它能与NaOH反应,生成Na2SO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)、甲同学认为是O2 , 则检验方法是。(2)、乙同学认为是SO2 , 则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量。写出SO2与NaOH反应的化学方程式。(3)、实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。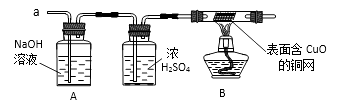
如果放出的是O2和H2 , 你认为方案中的安全隐患是。
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指 , 若不发出 , 方可采用上面的装置进行实验。
(4)、【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量无增减。
结论:铁粉与硫酸铜溶液反应时,产生的气体是。
(5)、【思维拓展】①由上述实验可以推出,硫酸铜溶液中可能含有物质。
②不通过称量,如何判断?有一同学设计了如图所示的装置进行实验:
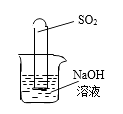
发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论。其他同学认为这一方案不严谨,理由是。要得到科学严谨的结论,仍利用该装置,补做的实验是。
(6)、假如6.4克SO2与119.6克NaOH溶液恰好完全反应,求反应后所得溶液的溶质质量分数。四、综合题
-
20. 某种手机电路板中含有Fe、Cu、Au、Ag、Ni (镍,银白色金属)等金属,以下是某工厂回收部分金属的流程图。
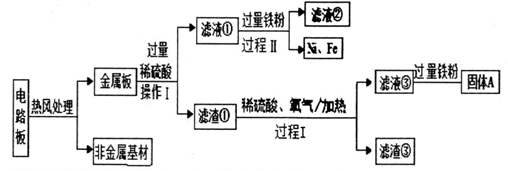
[资料]镍常见的化合价有+2、+3价,但在水溶液中通常只以+2价离子的形式存在。
(1)、过程I中会发生:2Cu+2H2SO4+O2 2CuSO4+2X,X的化学式为。(2)、滤液①中含有的三种物质的化学式为 , 过程Ⅱ反应生成Ni的化学方程式为。(3)、滤渣①的成分是 , 向滤渣①中加入稀硫酸和氧气后的现象是:固体部分溶解,溶液颜色变为色。(4)、滤液③和铁粉反应的化学方程式为 , 固体A的成分是。(5)、Cu、Fe、Ni在溶液中的活动性由强到弱的顺序依次是。五、计算题
-
21. 某同学春游带回几块石灰石样品,为测定样品中碳酸钙的含量,甲、乙两同学各取12.5g石灰石样品,用足量的浓度为10%的盐酸与其充分反应,测得数据如图所示。试回答下列问题:
 (1)、12.5g石灰石样品充分反应,产生的CO2的质量为g。(2)、由图像可知,化学反应的速率与反应物的接触面积的关系是。(3)、12.5g该样品中碳酸钙的质量是多少?(写出计算过程)(4)、在图中画出12.5g石灰石粉状样品与足量15%盐酸,充分反应的曲线c的大致位置及趋势。
(1)、12.5g石灰石样品充分反应,产生的CO2的质量为g。(2)、由图像可知,化学反应的速率与反应物的接触面积的关系是。(3)、12.5g该样品中碳酸钙的质量是多少?(写出计算过程)(4)、在图中画出12.5g石灰石粉状样品与足量15%盐酸,充分反应的曲线c的大致位置及趋势。
-